Полная версия
Фармакология может быть доступной. Иллюстрированное пособие для врачей и тех, кто хочет ими стать

Ренад Аляутдин
Фармакология может быть доступной. Иллюстрированное пособие для врачей и тех, кто хочет ими стать
© Аляутдинов Р. Н., текст, 2024
© ООО «Издательство «Эксмо», 2024
* * *Введение
При анализе зубных камней неандертальцев, живших в пещере Эль-Сидрон 50000 лет назад, выяснилось, что их диета включала тысячелистник и ромашку, горькие на вкус растения с небольшой питательной ценностью. По итогам более раннего исследования той же группы было определено, что у неандертальцев в Эль-Сидроне был ген вкуса горьких веществ. Неандертальцы сочли бы эти растения горькими, поэтому вполне вероятно, что эти травы были выбраны по причинам, отличным от вкуса. Невозможно точно сказать, с какой целью неандертальцы ели побеги тысячелистника и ромашки, но сегодня люди используют их как лекарственные растения.
Фармакология – это фундаментальная наука, которая вышла на передний план современной медицины за счет грандиозных успехов и достижений XX–XXI века в области сохранения здоровья и спасения жизней людей. Фармакология изучает лекарственные средства (ЛС) и их влияние на жизненные процессы. ЛС – это вещества или их комбинации, которые применяют для лечения, диагностики и профилактики заболеваний. К ЛС относятся фармацевтические субстанции и лекарственные препараты.
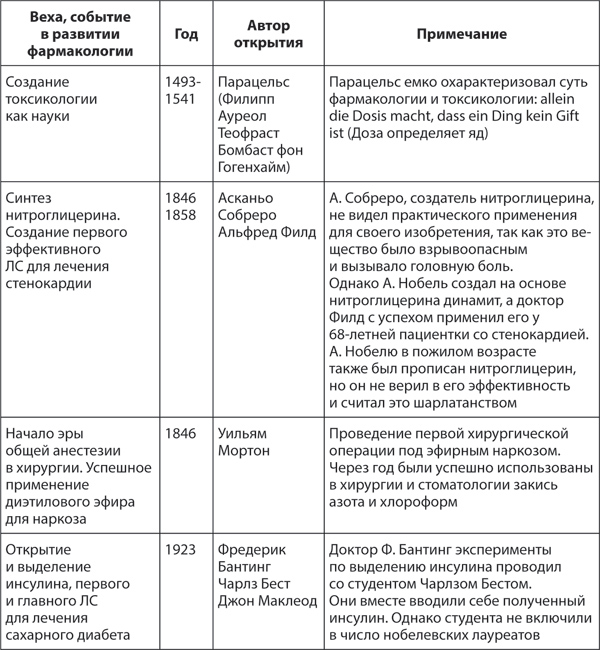
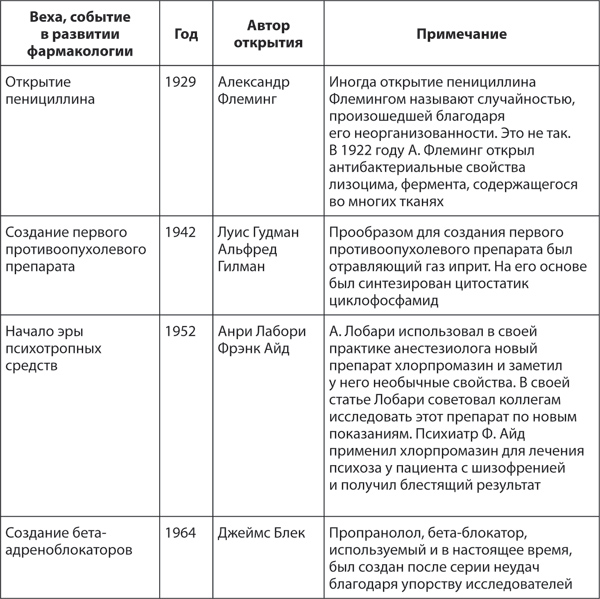
Время возникновения фармакологии как науки во многом зависит от точки зрения самого читателя. ЛС, созданные на основе растений, тканей животных, минералов, описаны в древнем Египте, Китае, Центральной Азии в 2000-х годах до нашей эры. Хорошо известен вклад в развитие лекарственной терапии Гиппократа, Цельса, Авиценны. Тем не менее существует мнение, что фармакология – наука очень молодая, существующая менее 150 лет, и она появилась благодаря возможности выделять чистые соединения и использовать научные методы исследований. Ниже приведены некоторые важнейшие вехи в развитии фармакологии и имена великих ученых, совершивших эти открытия.
Таблица 1. Развитие фармакологии с течением времени
Наименования ЛП. Лекарственные средства имеют несколько типов наименований. Как правило, это международное непатентованное наименование (МНН), торговое наименование и химическое наименование. МНН ЛС – уникальное наименование фармацевтической субстанции, рекомендованное Всемирной организацией здравоохранения (ВОЗ). Будучи уникальными именами, МНН должны различаться по звучанию и написанию и их нельзя путать с другими общеупотребительными именами (в качестве примера приведу МНН ЛП амоксициллин). Важная особенность системы МНН заключается в том, что названия фармакологически родственных веществ демонстрируют свое родство с использованием общей «основы» в наименовании. Так, например, ЛП группы пенициллина имеют в конце наименования сочетание «-циллин» (амоксициллин, ампициллин, оксациллин); блокаторы ангиотензиновых рецепторов – «-сартан» (валсартан, телмисартан).
Торговое наименование ЛС – наименование лекарственного средства, присвоенное его разработчиком (одно из торговых наименований амоксициллина – амоксил).
Химическое наименование ЛС – название, которое присваивается в соответствии с требованиями Международного союза по чистой и прикладной химии (IUPAC); химическое наименование амоксициллина [2S[2альфа5альфа,ббета(S*)]]-6-[[Амино-(4гидроксифенил) ацетил] амино]-3,3-диметил-7-ок-со-4-тиа-1-азабицикол [3.2.0] гептан-2карбоновая кислота.
Создание лекарственных средств. Источниками получения ЛС являются лекарственные растения (так получают морфин, сердечные гликозиды, атропин), ткани и органы животных (ферментные препараты панкреатин, гидролизат белков мозга церебролизин), продукты жизнедеятельности человека (гонадотропин хорионический получают из мочи беременных женщин), микроорганизмы (антибиотики), генномодифицированные микроорганизмы (продуценты инсулинов, других белковых препаратов), химический синтез низко- и высокомолекулярных соединений.
От идеи создания ЛС до его регистрации проходит около 10 лет. Вначале определяется мишень для ЛС, которую, как правило, открывают патофизиологи или молекулярные биологи. Долгое время для создания экспериментальной молекулы будущего лекарства использовали и до сих пор используют известные эндогенные соединения и на основе их структуры создаются новые лекарственные препараты. Так, например, по аналогии с молекулой гистамина были созданы ангистаминные средства – блокаторы гистаминовых рецепторов. В настоящее время, когда структура многих белков в организме известна, формулу нового лекарства рассчитывают с помощью компьютерных программ (in silico): посредством моделирования создается молекула, которая будет взаимодействовать с активными центрами белковой мишени. После завершения химического синтеза начинается доклинический этап исследований на моделях in vivo, а сейчас все чаще – на клеточных моделях in vitro, с целью выяснения механизма действия и эффективности. Важное значение имеет оценка безопасности будущего лекарства. После трагедии, связанной с применением талидомида в 1961 году ВОЗ учредила Программу по международному мониторингу за безопасностью ЛС. Талидомидовая трагедия положила начало международному фармакологическому надзору. В период с 1956 по 1961 год ЛС «Талидомид» было разрекламировано как идеальное седативное средство, в том числе для беременных. Это лекарство было разрешено в 56 странах. Однако талидомид обладал способностью вызывать врожденные уродства, то есть обладал так называемым тератогенным действием. В тот период времени родились от 8 до 12 тысяч младенцев с деформациями конечностей. Сейчас установлено, что талидомид является антагонистом эндотелиального фактора роста, стимулирующего рост сосудов. Блокада фактора роста приводила к тому, что наиболее длинные сосудистые ветви, расположенные в конечностях, не формировались, а значит, не формировались и сами конечности. Но тогда об этом никто не знал.
Согласно международным требованиям ЛС до его регистрации исследуют вначале на животных или клеточных моделях in vitro. На этом этапе оценивают различные виды токсического действия (тератогенность, эмбрио-, генотоксичность, канцерогенез и т. д.). Затем проводят клинические исследования (КИ) в 3 этапа: 1-я фаза исследования проводится на 20–100 здоровых испытуемых с целью изучения переносимости ЛС, его фармакокинетики, на этой стадии могут быть обнаружены часто возникающие нежелательные реакции. Во второй фазе КИ участвуют несколько сотен пациентов с заболеванием, для лечения которого было создано ЛС. На этом этапе оценивается, эффективно ли новое лекарство. Третья фаза КИ проводится на контингенте, насчитывающем до нескольких тысяч пациентов, с целью определения эффективности ЛС (его пользы) и его безопасности, т. е. способности вызывать нежелательные воздействия (оценка степени риска). В том случае, если соотношение польза/риск оптимально и превышает этот показатель у ранее существовавших средств, новое ЛС получает право на жизнь.
Если ЛП проходит все этапы дорегистрационных клинических исследований, почему в процессе гражданского оборота ЛП возникают новые побочные действия? Дело в том, что при клиническом дорегистрационном исследовании ЛП на нескольких тысячах пациентов невозможно выявить побочные эффекты, которые встречаются редко, однако могут быть очень опасными (часто это гепатотоксичность, нефротоксичность). В связи с этим исследование безопасности ЛП проводится на протяжении всей его жизни. С этой целью уполномоченные органы страны и производители отслеживают сообщения о нежелательных реакциях на ЛС в научной литературе, социальных сетях, а также предлагают врачам, провизорам, пациентам информировать о таких случаях, заполнив специальное извещение о побочном действии.
Вопросы
1. Кроме термина «ЛС», употребляются термины «фармацевтическая субстанция» и «лекарственный препарат». Как они соотносятся между собой?
Фармацевтическая субстанция – это тип лекарственного средства в виде одного или нескольких обладающих фармакологической активностью действующих веществ вне зависимости от природы происхождения, предназначенных для производства, изготовления лекарственных препаратов. Именно фармацевтическая субстанция определяет эффективность ЛС.
Лекарственные препараты (ЛП) – это ЛС в виде лекарственных форм – таблеток, капсул, растворов, мазей и т. д.
2. Часто в прессе можно встретить понятия «ЖНВЛП», «орфанные лекарственные препараты». Что это такое?
ЖНВЛП – перечень жизненно необходимых и важнейших лекарственных препаратов, утверждаемый Правительством Российской Федерации, обеспечивающих приоритетные потребности здравоохранения.
Орфанные лекарственные препараты – это ЛП, предназначенные исключительно для диагностики или патогенетического лечения (лечения, направленного на механизм развития заболевания, но не симптомов) редких (орфанных) заболеваний. Список орфанных заболеваний формируется Министерством здравоохранения России.
3. Какая разница между оригинальным и воспроизведенным ЛП (генериком или дженериком)?
Оригинальный лекарственный препарат – лекарственный препарат с новым действующим веществом, который зарегистрирован первым в Российской Федерации или в других государствах на основании результатов доклинических исследований лекарственных средств и клинических исследований лекарственных препаратов, подтверждающих его качество, эффективность и безопасность. Оригинальный лекарственный препарат имеет патентную защиту, максимальный срок которой может составлять 20 лет. В течение этого времени ни одна другая компания не может производить или продавать этот ЛП.
Когда оригинальное ЛС теряет эксклюзивность, появляется возможность подать заявку на регистрацию и производство этого ЛС другими производителями. Воспроизведенный ЛП (генерик) имеет эквивалентный оригинальному ЛП качественный и количественный состав действующих веществ в эквивалентной лекарственной форме. Он намного дешевле оригинального, поскольку второму производителю не нужно возмещать затраты на открытие новой молекулы, разработку, доклинические и клинические исследования этого ЛП.
Общая фармакология
Общая фармакология изучает основные закономерности взаимодействия организма и ЛС, характерные для всех лекарств, и подразделяется на два основных раздела: фармакокинетику и фармакодинамику.
Фармакокинетика изучает факторы, определяющие концентрацию лекарств в жидкостях и тканях организма во времени и включает такие процессы, как всасывание, распределение, метаболизм и выведение лекарств (сокращенно ADME), то есть фармакокинетика – это то, что организм делает с лекарством.
Фармакодинамика изучает механизмы действия ЛС, влияние лекарств на рецепторы-мишени и ткани. Если коротко, то фармакодинамика – это то, что лекарство делает с организмом.
Фармакокинетика
Концентрация ЛС в тканях организма напрямую зависит от процессов всасывания (абсорбции), распределения, метаболизма и выведения (экскреции) лекарств.
Всасывание (абсорбция) определяет механизмы движения ЛС от места введения до кровотока (некоторые виды введения составляют исключение, например, введение в спинномозговой канал).
Механизмы всасывания ЛС
1. Пассивная (простая) диффузия (трансцеллюлярный транспорт). При этом виде всасывания ЛС движется по градиенту из области высокой концентрации лекарства (просвет кишечника, место инъекции) в область с низкой концентрацией (плазма крови). Для того чтобы абсорбироваться, ЛС должно пройти липидные мембраны клетки, растворившись в них. Это возможно только для небольших липофильных, но не гидрофильных веществ (рис. 1). Пассивная диффузия не требует затрат энергии. Этот механизм абсорбции характерен для кишечника, сосудов головного мозга.
Вопрос
Какие факторы в совокупности определяют проникновение через липидные мембраны?
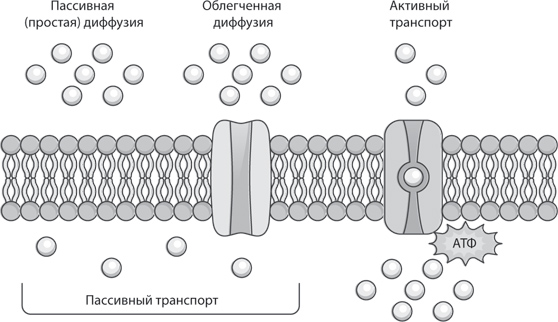
Рис. 1. Механизмы всасывания лекарственных средств. (Пояснения в тексте.)
Скорость пассивной диффузии веществ через мембраны зависит от липофильности, молекулярной массы (обратно пропорциональной квадратному корню молекулярной массы), формы молекулы вещества, температуры среды, толщины и площади мембраны, через которую проникает ЛС. Все эти факторы учитываются законом Фика, согласно которому:
dQ / dt = (С1–С2) × площадь мембраны ×
коэффициент диффузии / толщина мембраны,
где dQ/dt – скорость диффузии, (С1–С2) – градиент концентрации. Коэффициент диффузии в основном определяется степенью липофильности вещества.
2. Облегченная диффузия – это диффузия, которая поддерживается (облегчается) мембранными транспортными каналами. Эти каналы представляют собой гликопротеины, которые позволяют молекулам преодолевать мембрану (см. рис. 1).
Они почти всегда специфичны либо для определенной молекулы, либо для определенного типа молекулы (в случае ионного канала), и поэтому они тесно связаны с определенными физиологическими функциями. Например, канал GLUT4 обеспечивает вход в клетку путем облегченной диффузии гидрофильной молекулы глюкозы (из-за высокой гидрофильности глюкоза самостоятельно не может проникнуть через липидную клеточную мембрану).
Транспорт при облегченной диффузии является пассивным, насыщаемым и определяется числом переносчиков.
3. Фильтрация (парацеллюлярный транспорт). Парацеллюлярный транспорт – это перемещение ЛС через межклеточные пространства между эндотелиальными или эпителиальными клетками. Поскольку перемещение молекул ЛС происходит за счет градиента концентрации, расход энергии отсутствует. Этот вид всасывания не требует специфического переносчика. Парацеллюлярная диффузия играет незначительную роль в абсорбции ЛС из кишечника, но имеет принципиально важное значение для движения в сосудах. Исключение составляют сосуды головного мозга, где между эндотелиальными клетками имеются плотные контакты, формирующие гематоэнцефалический барьер (ГЭБ).
4. Активный транспорт – это процесс переноса веществ через клеточную мембрану с помощью специфического переносчика, сопровождающийся расходом энергии АТФ (рис. 1). В отличие от других видов транспорта, активный транспорт возможен против градиента концентрации. Этот вид транспорта, как и облегченная диффузия, насыщаем, так как число переносчиков ограничено.
Таблица 2. Сравнительная характеристика путей абсорбции ЛС
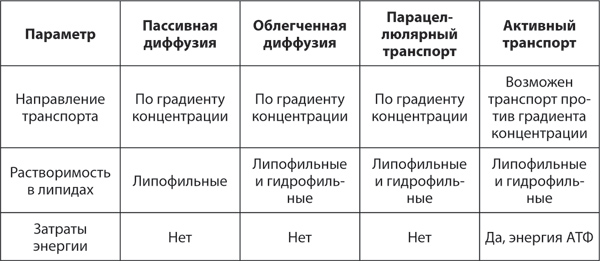
Вопрос
Активный транспорт выглядит очень эффективным путем доставки веществ в клетку. Часто ли он используется для доставки ЛС?
Увы, нет. Специфический переносчик в организме «заточен» на транспорт определенных молекул, поэтому ЛС должно быть структурно очень близко этим веществам или быть ими. В практической медицине можно привести в качестве примера противопаркинсоническое ЛС «Леводопа», являющееся аминокислотой. Всасывание леводопы из кишечника осуществляется транспортером аминокислот, предназначенным для их всасывания в процессе пищеварения.
Механизмы всасывания ЛС зависят от пути введения. Выделяют энтеральные и парентеральные пути введения.
Энтеральные пути введения. К энтеральным путям относят введение под язык, буккальное, внутрь (перорально), через зонд в желудок или двенадцатиперстную кишку, в прямую кишку (ректально). Наиболее часто используют введение ЛС внутрь (в лекарственных формах: таблетки, капсулы, растворимые гранулы, настои, микстуры и т. д.). Чтобы абсорбироваться из ЖКТ, лекарство, принимаемое внутрь, должно выдерживать воздействие низкого pH в желудке и ферментов. Пептидные препараты (например, инсулин) особенно подвержены ферментативному разрушению и практически не принимаются перорально.
Слизистая оболочка полости рта имеет тонкий эпителий и богатую васкуляризацию, что способствует всасыванию; однако контакт обычно слишком короткий, а площадь слизистой мала для существенного всасывания ЛС. Для использования этого пути введения ЛС помещают между десной и щекой (буккальное введение) или под язык (сублингвальное введение), в этом случае контакт сохраняется дольше, усиливая абсорбцию. Важное преимущество сублигвального и буккального введений – это возможность избежать первичного всасывания в систему воротной вены и последующего метаболизма в печени. Однако небольшая поверхность всасывания ограничивает применение этого способа введения.
Всасывание ЛС в некоторой степени возможно в желудке, но основным местом всасывания является кишечник. Это обусловлено тем, что площадь всасывания в кишечнике, благодаря ворсинкам слизистой, очень большая, во много раз превосходит площадь слизистой ротовой полости и желудка. Важной особенностью клеток эпителия кишечника (энтероцитов) является наличие плотных контактов, которые фактически перекрывают проход веществ между энтероцитами, предотвращая парацеллюлярный транспорт, поэтому основной механизм всасывания в кишечнике – пассивная диффузия.
Обычно в желудке происходит интенсивный контакт между лекарством, принимаемым перорально, и жидкостями ЖКТ. Хотя желудок имеет относительно большую эпителиальную поверхность, его толстый слизистый слой и короткое время транзита ограничивают всасывание лекарств. Эти свойства желудка могут влиять на рецептуру лекарств и их поведение. Поскольку большая часть абсорбции происходит в тонкой кишке, опорожнение желудка часто является стадией, ограничивающей скорость всасывания. Пища, особенно жирная, замедляет опорожнение желудка (и скорость всасывания лекарств), что объясняет, почему прием некоторых лекарств натощак ускоряет всасывание. Лекарства, влияющие на опорожнение желудка (например, атропин), также влияют на скорость всасывания других лекарств. Пища может усиливать степень всасывания плохо растворимых препаратов (например, гризеофульвина), снижать ее для препаратов, разлагающихся в желудке (например, бензилпенициллина), или иметь незначительный эффект, или не иметь никакого эффекта.
Поскольку твердые лекарственные формы (например, таблетки, капсулы) должны раствориться до того, как произойдет всасывание, скорость растворения определяет доступность лекарства для всасывания. Растворение, если оно происходит медленнее, чем всасывание, становится стадией, ограничивающей скорость. Изменение состава лекарственных форм, физико-химических свойств активного вещества (соль, кристаллическая или аморфная форма) могут изменить скорость растворения и, таким образом, общую абсорбцию.
Лекарства, вводимые ректально (per rectum), действуют быстрее, чем при пероральном введении, и имеют более высокую биодоступность (которую определяют как часть введенной дозы ЛС, которая в неизмененном виде достигла системного кровотока, и обычно выражают в процентах). Причиной является отсутствие влияния кислоты желудка и ферментов кишечника, а также попадание части ЛС в кровь, минуя систему воротной вены. Ректальное всасывание приводит к тому, что большее количество препарата достигает системного кровообращения с меньшими изменениями в пути. Помимо того, что ректальное введение более эффективно, оно также уменьшает побочные эффекты некоторых лекарств, такие как раздражение слизистой желудка, тошнота и рвота. Этот путь введения удобен для введения ЛС в педиатрии, а также при невозможности принимать ЛС внутрь. Ректальное введение противопоказано после операции на прямой кишке или кишечнике, при ректальном кровотечении или пролапсе прямой кишки.
Таблица 3. Сравнительная характеристика энтеральных путей введения
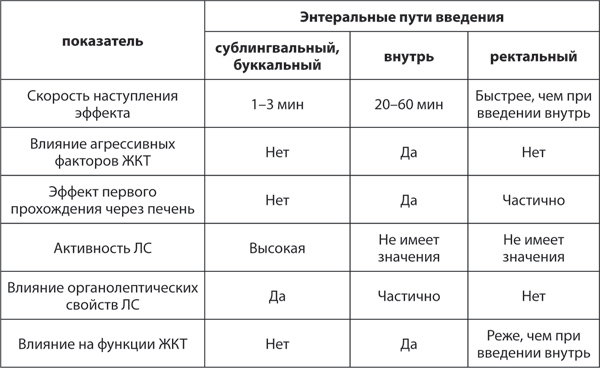
Парентеральные пути введения. Основными путями парентерального введения являются внутривенный, внутримышечный, подкожный. Реже используются интраартериальный, внутрикостный, эпидуральный, интратекальный и т. д. Лекарства, вводимые внутривенно, попадают в системный кровоток напрямую. Биодоступность ЛС при этом пути введения составляет 100 % (рис. 2).
Подкожное введение – это тип инъекции в подкожный слой или подкожную клетчатку. Подкожная клетчатка – это слой кожи, лежащий ниже дермы и эпидермиса. Лекарство, вводимое путем подкожной инъекции, всасывается медленно в течение определенного периода времени, поскольку подкожный слой не содержит большого количества кровеносных сосудов.
Внутримышечная инъекция – это тип введения, при котором ЛС вводят в крупную мышцу. Мышцы богаты кровеносными сосудами. Следовательно, всасывание препарата происходит быстрее, чем при подкожном введении.
Внутривенное введение – это инъекция ЛС непосредственно в кровяное русло. Этот тип введения должен выполняться специалистами с соблюдением условий стерильности. Это наиболее эффективный и быстрый путь введения, биодоступность при этом пути введения составляет 100 %.
Парацеллюлярный транспорт является основным путем доставки ЛС при парентеральном введении, т. е. ЛС из места введения в сосуды, а затем из крови в ткани попадают через пространства (поры) между эндотелиальными клетками сосудов. Однако в сосудистой сети есть органы и ткани, в которых эндотелиальные клетки плотно прилегают друг к другу, не образуя пор. Более того, эндотелиальные клетки соединены между собой дополнительными «замками» – так называемыми плотными контактами. В этих местах сосудистая сеть образует барьеры для ЛС: гематоэнцефалический барьер, гематоофтальмический барьер, гематоплацентарный барьер. Через барьеры путем простой диффузии могут проникать только липофильные соединения.
Парентеральное введение ЛС технически сложнее энтерального. Для этого пути введения требуются условия асептики и антисептики, а также специальные навыки и/или обученный персонал.
Таблица 4. Сравнительная характеристика парентеральных путей введения
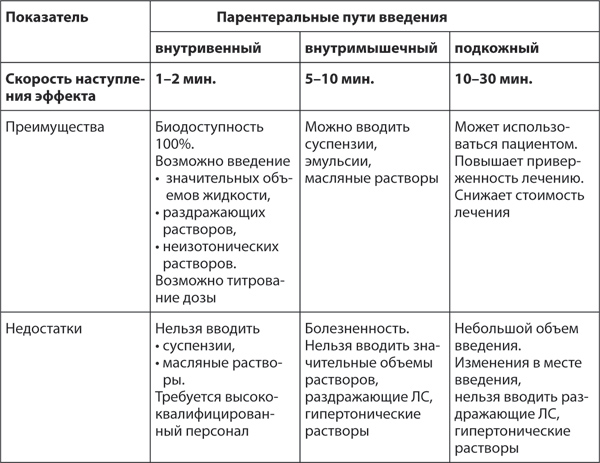
Распределение характеризует движение ЛС из сосудистого русла, распространение по органам и тканям, в том числе и в орган-мишень. Подчинено распределение тем же принципам, которые определяют всасывание лекарств (например, степень ионизации, липофильность, размер молекулы, рН окружающей среды и т. д.). В плазме крови многие ЛС неспецифически связываются с альбумином и другими белками. При этом связанные с белком ЛС не могут покинуть сосудистое русло, так как большие молекулы белков не способны преодолеть эндотелиальный барьер путем пассивной диффузии или фильтрации. Таким образом, создается своего рода депо. Очевидно, что пока лекарство неспецифически связано с белком, оно не может оказывать фармакологические действие, а также метаболизироваться. Если пациенту прописаны два и более ЛС, они могут конкурировать за места связывания на белках в плазме, вытесняя друг друга. Это может изменять фармакокинетику ЛС по сравнению с монотерапией.
Содержание ЛС в органах определяется в первую очередь степенью кровоснабжения. Лекарства будут быстрее распределяться по областям тела с обильным кровоснабжением (например, сердце, почки) по сравнению с областями, которые получают мало крови (например, кожа, жировая ткань). С другой стороны, как только липофильные лекарство достигает жировой ткани, оно может оставаться в ней в течение достаточно долгого времени, пока его концентрация в плазме не снизится и лекарство не сможет двигаться «по градиенту концентрации» обратно в кровоток.
Для анализа распределения ЛС в органах и тканях используется понятие «кажущийся объем распределения» – это показатель, который направлен на то, чтобы предсказать, насколько равномерно лекарство распределяется по организму. Кажущийся объем распределения, Vd, рассчитывают путем деления введенной дозы (мг) на концентрацию в плазме (мг/л).
Vd (л) = доза (мг) / C (мг/л)
Показатель Vd равен условному объему (компартменту), в котором ЛС должно распределиться, чтобы достичь существующей концентрации С в плазме крови. Лекарства с относительно небольшим Vd (например, 5 л) в основном остаются в плазме крови. Лекарства с Vd = 15 л распределяются по сосудистым и внеклеточным жидким компартментам. Такой показатель Vd характерен для небольших гидрофильных молекул, которые покидают сосудистое русло благодаря парацеллюлярному транспорту, но не могут попасть внутрь клеток через липидные мембраны их оболочек. Препараты с Vd>40 л обладают высокой липофильностью и распределяются по всем тканям организма (сосудистым, внеклеточным и внутриклеточным жидкостным компартментам).