
Полная версия
Панмедиа. COVID-19, люди и политика
В подтверждении этой гипотезы дегенерации приводят случаи с бактериями, а именно одноклеточными риккетсиями и хламидиями, которые способны размножаться только внутри другой клетки. Риккетсии, известные как возбудители пятнистой лихорадки Скалистых гор – инфекционное заболевание, которое переносит неприятный клещ Dermacentor andersoni, – взяли фамилию своего открывателя, американского биолога Ховарда Риккетса (1871–1910), погибшего от тифа в Мексике. В начале 1980-х годов технику культивирования риккетсий изобрел французский врач Дидье Рауль, работающий сегодня в Средиземноморском институте инфекционных болезней. В середине марта 2020-го Рауль выступил в прессе с заявлением, что нашел вакцину против коронавируса, а ученый он серьезный, и сказал он это явно не для хайпа, но заботливое французское правительство, всегда верное своим высоким принципам, вместо того, чтобы немедленно дать разрешение на испытание препарата, способного остановить развитие инфекции на ранней стадии, решило углубиться в дела бумажные, выяснить, насколько он соответствует современным нормам и протоколам.
Вторая гипотеза говорит о клеточном происхождении вирусов. В те же древние времена фрагменты ДНК и РНК могли по каким-то причинам отпочковаться от основной цепочки генома «господина», крупного клеточного организма, и зажить отдельной, но зависимой от последнего жизнью. Это могло произойти с трансмидами, молекулами ДНК, способными к межклеточной миграции, и транспозонами, блуждающими молекулами внутри одного генома. Транспозоны (transposons, mobile elements) обнаружила в 1950 году американский цитогенетик Барбара МакКлинток (1902–1992), и с тех пор они прочно вошли в корпус штудий по эволюционной генетике.
Место МакКлинток на научной карте США примерно то же, что у Николая Вавилова в СССР, но ей повезло значительно больше: несмотря на то, что ее работы по генной регуляции и «контролирующим элементам» хромосом были оценены далеко не сразу, а некоторыми коллегами воспринимались даже враждебно, ее все же никто не обвинял в продвижении заведомо ложной теории и у нее не было своего Александра Хвата, который бы пытал ее по ночам, выбивая признания[8].
Полюбив еще в молодости кукурузу не меньше, чем годы спустя Никита Хрущев, МакКлинток продолжала ею заниматься на протяжении всей своей научной карьеры, сделав ряд важнейших открытий, в том числе рекомбинации наследственной информации как следствие crossing-over’а, что изменило наши представления о геноме как статичной структуре, передающей эту информацию от одного поколения другому intactus. МакКлинток пришла к своим открытиям благодаря изучению поведенческих моделей геномов, или паттернов, из которых, как она верила, состоит вся природа без исключения. Как отмечал исследователь ее творчества Натаниэль Комфорт, «паттерн – это точка отсчета для понимания сути контролирующих элементов, открытых МакКлинток, и кроме того ее уникального взгляда на природу. Она была особенно чутка к нюансам таких паттернов, которые давали ей ключ к поведению хромосом…»[9]
Во многом открытие МакКлинток транспозонов произошло в результате тщательного изучения геномных девиаций, сломов в поведении и новых сращений тех или иных хромосом (в частности, в 1939 году с помощью рентгеновского аппарата она изучила поведение нормальной и анормальной, перестроенной 9-ой хромосомы), что в конечном счете ведет к увеличению хромосомного разнообразия. Этот же процесс, как выяснила МакКлинток, оказался ответственным за вариегантность, или пестролистность, у растений. Вирусы, однако, не дремлют и в этом мире прекрасного. Они поражают листья растений, симптомом чего, как правило, является образование узоров; например, мозаичный вирус, производящий на листе своеобразные мозайки, или цитрусовый вирус, принадлежащий семейству Bromoviridae, который заражает листья лимонных и грейпфрутовых деревьев. Поэтому, если вы разглядываете замысловатую мозайку на листе лимонного дерева, не спешите видеть в ней извечную красоту природы.
Третья гипотеза – коэволюция. Речь в ней идет о том, что вирусы произошли из комплексов белков и нуклеиновых кислот в ту же эпоху, что и первая клеточная жизнь. Не забудем также и о вироидах, которые не являются вирусами, поскольку не имеют внешнюю белковую оболочку, капсид, и состоят только из кольцевой РНК, но при этом играют огромную роль в патогенезе растений, используя клетку-хозяина для репликации. Вироиды были открыты в 1971 году швейцарским фитопатологом Теодором Динером, изучавшим патогенез картофеля, или проще говоря, существенную деформацию клубня, который был замечен агрономами на полвека раньше – пораженное растение утрачивало обычную форму и становилось веретеновидным. Динер предположил, что картошка заболевает не от какого-то неизвестного вируса, а от агента нового вида, чьи размеры значительно меньше вирусных, и это оказалось правдой. Вироид, поразивший столь важный для человечества продукт, оказался на восемь порядков меньше стандартных размеров вируса. Позже, в середине 1970-х, микробиолог Вольфрам Зенгер и его коллеги провели углубленное изучение этого картофельного вироида и пришли к выводу, что причиной деформации формы клубней является конкретный патоген – одноцепочная, ковалентно замкнутая молекула РНК, имеющая плотную палочковидную структуру (подробности ее морфогенеза я опускаю[10]). Иными словами, этот вироид прокрался в клетку картофельного клубня, запустил процесс РНК-сайленсинга в уже известной нам эукариотической клетке, когда вместо защиты последней от вирусов происходит блокировка определенных генов, невозможность их экспрессии, в результате чего клетка-хозяин заболевает.
Уже в конце 1980-х Динер предположил, что вироиды являются древнейшими реликтами, они могли появиться на Земле еще до самих вирусов и представлять доклеточный РНКовый тип жизни. Через тридцать лет Динер вернулся и дополнил свою теорию новыми наблюдениями (кстати, сегодня ученому 99 лет и он еще вполне в форме), которые многими из его коллег принимаются, хотя и не без оговорки об альтернативных источниках происхождения органики.
Подытожим – у нас есть три главных гипотезы о том, как возникли вирусы: регрессивная, предлагающая рассматривать вирусы как своего рода падших ангелов; клеточного происхождения, рассматривающая вирусы как этакий правый уклон – помним слова тов. Сталина, «правый уклон в коммунизме в условиях капитализма означает тенденцию ‹…› к отходу от революционной линии марксизма в сторону социал-демократии» – в нашем случае, революционная линия означает развитие жизни по клеточному сценарию; и гипотеза коэволюции, согласно которой вирусы пошли по самостоятельному пути развития, используя тот же материал, что и клетки. К тому же, благодаря открытию Динера, мы еще знаем о вироидах – носителей доклеточной реликтовой формы жизни.
Большинство вирусологов и биологов согласны с тем, что каждая из этих трех теорий объясняет какой-то важный аспект вирусного Dasein, как бы сказали старые немецкие авторы – Гегель или его нацистский комментатор, – но при всем том остается немало вопросов, и ни одну из этих теорий нельзя считать полной. Например, мы так и не знаем, почему микропаразитические организмы не являются вирусами? Каким образом вирусы, отпавшие от своих клеток, приобретают капсид? А если действительно имела место коэволюция, то почему вирусы не воспользовались древним естественным правом и не приобрели себе клетку, а предпочли вести зависимое существование? Очевидно, что с точки зрения оптимизации жизни и эволюционного процесса, если мы дарвинисты, постоянная жизнь при ком-то – не самый хороший вариант. А если мы, как Ньютон, верим в сверхразумного Демиурга, то тем более не понятно, зачем ему было создавать столь бессмысленных, всем досаждающих существ?
Снова возник запрещенный в строгой науке вопрос «зачем», но оставаясь в рамках метафизики, мы можем выдвигать гипотезы. Например, такую: вирусы оказались необходимыми для того, чтобы ввести все клеточные существа в режим постоянного выживания. Это нужно даже не столько ради какой-то высшей цели, которой у природы, если ей не приписывать божественного аспекта, может просто не быть, а для диверсификации самого процесса распространения жизни. Нет сомнений в том, что диверсифицированная система гораздо стабильнее и успешнее в плане адаптации к внешней среде. Вирусы в процессе своего развития выработали гиперадаптационные способности, благодаря которым они способны перестроить иммунитет – платформу, на которой строится вся коммуникация органических существ с внешней средой. Белок коронавируса, к примеру, снимает врожденную иммунную защиту своего хозяина, обезоруживая его таким образом перед средой.
Другая гипотеза состоит в том, что вирусы – это параллельный путь развития и хранения геномной информации, возможно, на тот случай, если ДНК-мир исчезнет, что отчасти коррелируется с «РНК-мировой гипотезой», впервые высказанной Карлом Вёзе, а затем развитой Лесли И. Орджелом и Уолтером Гилбертом. Поскольку РНК у вирусов берет на себя функции ДНК у живых организмов, то можно было бы предположить, опять же не выходя за рамки естественной метафизики, что вирусы играют роль backup’а. И чтобы backup был всегда в форме, они не прячутся в потаенных пещерах цивилизации, словно «великие учителя» в Шамбале, а находятся в постоянном взаимодействии с органической жизнью.
Первооткрывателем вирусов считается Антони ван Левенгук (1632–1723), голландский торговец, натуралист который их увидел в сконструированный им самим микроскоп. Микроскоп Левенгука был прорывным техническим изобретением, хотя имел ряд ограничений в силу несовершенства линз, которые тем не менее давали увеличение примерно в пятьсот раз. С его помощью Левенгук смог увидеть крошечных существ, без хвоста и очень юрких. Встреча с неизвестным дотоле миром оказалась столь внезапной, что научный истеблишмент поначалу не поверил сообщению натуралиста. В 1676 году к Левенгуку прибыла ученая делегация во главе с другим выдающимся натуралистом, англичанином Неемией Грю, автором «Анатомии растений» (1682), открывший у них органы размножения, которая подтвердила подлинность сообщения голландца.
Медицина XVII века считала, что источник всех болезней находится внутри организма, патогенный механизм мыслился исключительно как внутренний, влияние внешних факторов, а тем более невидимых глазу, не рассматривалось. Эту парадигму было не так легко сломать, и во многом это произошло благодаря очередной эпидемии чумы, пришедшей в последней трети XVIII века в Россию. Екатерина II не представляла размеры бедствия, вероятно, от нее их скрывали, и должные карантинные меры приняты не были. Чума быстро распространилась по городам, сея панику и смерть. Летом 1771 года в больницу при Николо-Угрешском монастыре, построенном в честь победы на Куликовом поле, прибыл молодой медик Даниил Самойлович (1744–1805). Он мгновенно занялся лечением зараженных, расчитывая только на свои силы. Кроме него врачей в монастырской больнице не было. Смертность росла с каждым днем, погибал почти весь медперсонал, и Самойлович начал изобретать меры защиты, которые оказались действенными. Он понял, что основное заражение происходит через дыхание и телесный контакт, поэтому все помощники могли подходить к больным только в самодельных масках в халатах, пропитанных уксусом и смазанных дегтем. Это тут же снизило количество и скорость заражений среди медперсонала. Вдобавок сам врач, который лично вскрывал бубоны на теле пациентов, носил окуренную одежду тех, кто уже умер от чумы.
Революционная идея Самойловича состояла в том, что он первый начал готовить прививки из содержимого бубонов. Ослабляя агента болезни, который по понятным причинам оставался для него невидимым, он превращал его из убийцы в спасителя. После победы в чумной войне Даниил Самойлович отправится в Европу продолжать обучение, опубликует серию работ, где изложит свои взгляды на происхождение Черной смерти, и внесет огромный вклад в развитие акушерства.
Коллега и современник Самойловича, английский врач Эдвард Дженнер (1749–1823) пошел по тому же пути, применил вакцину против натуральной оспы – одной из самых страшных болезней той эпохи. Идея была очень похожей: использовать материал болезни для борьбы с ней. На протяжении долгого времени Дженнер изучал литературу по народному врачеванию. Он заметил, что издревле, и в самых разных культурах, люди интуитивно стремились построить защиту от болезни таким способом, вводя оспенный гной в тело больного или приготавливая специальный раствор из оспенных корочек. Кто-то после этого умирал, кто-то переносил заболевание относительно спокойно и выздоравливал. Мысль понятна, люди стремились привить своим зараженным иммунитет – почти магическое действие, учитывая, что это делалось без какой-либо теории, на чистой интуиции.
Однажды и сам Дженнер решился на подобный эксперимент. Собрав материал коровьей оспы на руке одной доярки, заразившейся этой болезнью, не опасной для человека, Дженнер стал постепенно, малыми дозами его вводить здоровому восьмилетнему мальчику по имени Джим Фиппс. После нескольких недель таких сеансов Дженнер стал заражать Фиппса уже натуральной оспой, врач проделал этот трюк два десятка раз, но ребенок так и не заболел. Хотя Фиппс остается сегодня самым известным «первым» вакцинированным человеком в Европе, он таковым на самом деле не является. Несколькими годами ранее учитель из города Киля, Питер Плетт, таким же точно способом вакцинировал трех школьников, используя ту же коровью оспу. А в 1774 году, когда очередная эпидемия оспы стала накрывать Англию, фермер из Йетминстера, Бенджамин Джести, вакцинировал коровьей оспой себя и свою семью, используя иглу для пошива мешков. Несмотря на косые взгляды соседей, которые расценили поступок Джести как варварский, эксперимент оказался удачным и даже был оценен (в прямом смысле слова) правительством Уильяма Питта Старшего.
Наука пришла к открытию вирусов позже, в конце XIX века, когда микробиолог Дмитрий Ивановский (1864–1920), занимавшийся болезнями растений, в 1892 году открыл вирус табачной мозайки, поражающий все растения рода Nicotiana. Табачной мозайкой также занимался голландский ботаник Мартин Бейеринк (1851–1931), опиравшийся в этом на труды немецкого агронома Адольфа Майера, который находил причину табачной мозайки в бактериальном заражении растений, что оказалось неверным. Бейеринк опроверг это мнение, в своих исследованиях он показал, что растения заболевают от микроскопических агентов, которые, как он считал, имеют жидкообразную природу и способны редуплицироваться в организме хозяина. Вместе с Пастером или независимо от него, он назвал их «вирусами».
На самом излете XIX века два немецких микробиолога, Фридрих Лёффлер (1852–1915) и Пауль Фрош (1860–1928), сражались с крайне неприятным недугом под названием «ящур», атакующим грызунов, кур и крупных животных. Он принадлежит к семейству пикорнавирусов, имеющих как правило форму икосаэдра. Кстати, эти икосаэдры весьма опасны и для человека, они являются возбудителями полиомиелита, ринита и гепатита А, среди прочих. Тогда Лёффлер и Фрош этого еще не могли знать, но именно сражаясь с ящуром, эти ученые в 1898 году открыли субстанцию, которая, в отличие от бактерий, свободно проходила сквозь фарфоровые фильтры. Эта субстанция или агент была идентифицирована ими как единственный возбудитель болезни. Так возникла вирусология – наука о бесклеточной жизни.
COVID доступа: жизнь
Поведение COVID-19, как и остальных вирусов, очень интересно тем, что не будучи изначально в научном понимании живым, он становится таковым или мастерски мимикрирует живого в процессе взаимодействия с последним. Если средневековый философ и богослов Фома Аквинский, повторяя мысль Демокрита и Платона, считал, что мимезис заключается в подражании природе, «ars imitatur naturam», то Аристотель в «Поэтике» говорил о подражании как творческом акте, когда художник доводит само произведение природы до совершенства. Творчество коронавируса ближе к аристотелевскому определению мимезиса. Его мастерство состоит в удивительной способности выдать себя живому организму за того, кем он не является – обеспечивающим жизнь клетки элементом.
Разнообразие вирусов огромно, порядка шести миллионов, и они далеко не все похожи на нашего панмедийного врага. Одни – как он, другие имеют форму спирали, яйца или, как на рисунке ниже, могут напоминать букву фу из японской азбуки катакана[11]. Их размеры тоже варьируются: от 20 до 300 нм в диаметре. Интересно, что вирусы могут поражать не только людей и животных, но и бактерии – таких называют бактериофагами, их обнаружил в 1917 году французский микробиолог Феликс д’Эрелль (1873–1949), не писавший никаких диссертаций и едва ли вообще имевший высшее образование[12].

Известные формы вирусов. Рис. Анны Полищук
Как часто случается, открыл он их в результате других научных изысканий. После Первой мировой войны ученый с внешностью Дон Кихота занимался патогенными бактериями дизентерии, натолкнувшись на ранее неизвестного агента (инфекцию), который вызывал их смерть. Д’Эрелль начал специально заражать бактерии этим агентом и обнаружил, что он успешно увеличивает свою популяцию за счет их уничтожения. Затем д’Эреллю приходит в голову сногсшибательная мысль – как тут не согласиться с Аристотелем, что творец доводит природу до совершенства – лечить бактериальные болезни с помощью бактериофагов! Инертный ученый мир отнесся к этому скептически, однако в те времена еще не существовало антибиотиков, и предложить что-то более эффективное никто не мог. Д’Эрелль, поверив с свой метод – благо над ним не стояло государство, как сегодня над Раулем – начал его применение и получил положительные результаты, которые он изложит в книге «Бактериофаг» (1922). Самым поразительным остается описание процесса выделения, «самоидентификации», фагов-агентов из бактерий и их внеклеточного существования.
Но бактериальная драма на этом не заканчивается. Многие годы спустя биолог Сальвадор Лурия, сбежавший из муссолиниевской Италии в США, покажет, что бактерии научаются сопротивляться фагам и это умение они передают генетически. В Америке Лурия, вместе с Максом Дельбрюком и Альфредом Херши, организует неформальное научное сообщество под названием «Phage Group», куда войдет еще ряд крупных ученых, внесших огромный вклад в создание науки микробиологии. Но все это произойдет потом. А в 1934 году Сталин приглашает д’Эрелля в СССР для продолжения работы над бактериофаготерапией, чем он и займется в Тифлисе в компании со своим грузинским коллегой Гиоргием Элиавой[13], прекрасно знавшим труды француза в этой области. Бактериологи познакомились сразу после войны в Институте Пастера в Париже, куда Элиава начал ездить с научными целями, а д’Эрелль тогда в очередной раз прибыл из Мексики, где он добывал алкоголь из сока агавы. Поработав в Институте несколько лет, д’Эрелль покинет его из-за склок с администрацией. В 1921 году Элиава создает в Грузии бактериологический институт, где сам успешно занимается исследованиями фагов – до 1937-го, пока не будет расстрелян как враг народа.
В 1930-х Дельбрюк и Лурия разрабатывали количественную методологию по изучению лигических взаимодействий бактериофага и клетки, что помогло лучше понять механизм мутации. Херши со своими коллегами доказал, что генетическая информация бактериальных вирусов закодирована в их нуклеиновых кислотах, это в свою очередь дало возможность установить фундаментальную характеристику вирусов, а именно: они содержат либо РНК, либо ДНК. Далее ученые выяснили, что помимо лизиса, которые вызывают вирусы у зараженных бактерий, имеет место и так называемая вегетативная вирусная инфекция, когда фаги проникают в «хозяина» (в данном случае в бактерию) без лигических осложнений. Это явление стали рассматривать как пассивную инфекцию, и благодаря ему прояснился механизм встраивания вирусов в «хозяйскую» хромосому.
Фаги действуют как настоящие хищники: нападая на бактерию, они впрыскивают в нее свой генетический материал, запуская механизм редупликации. Но если от укуса тарантула, тоже впрыскивающего в свою жертву яд – в эпоху Ренессанса он считался причиной безумия, – пострадавшие вылечивались экстатическим танцем «тарантеллой», то у пораженной фагом бактерии такой возможности нет. В танце или без него бактерия начинает работать на производство фагов, чей геном мутирует, смешиваясь с геномом хозяина.

Захват клетки бактериофагом. Рис. Анны Полищук
Помимо РНК или ДНК, находящихся внутри агента, последний обладает еще и белковой оболочкой – капсидом (на рисунке ниже он изображен треугольником), который защищает вирус от угрозы и помогает при захвате клетки. Некоторые вирусы вдобавок покрыты липидной оболочкой, жировым слоем, который защищает их от угроз внешней среды.
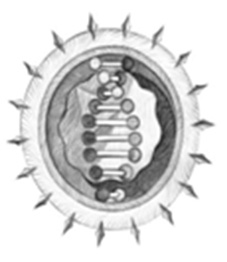
Мутированный бактериофаг. Рис. Анны Полищук
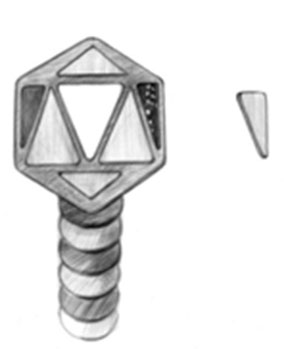
Структура агента. Рис. Анны Полищук
Агенты могут содержать до двух цепочек ДНК или одну цепочку РНК, способную удваиваться или достраи вать на себе цепочку РНК, таким образом вирусы способны размножаться в различных органеллах зараженной клетки. Органеллы – это микроструктуры, расположенные в цитоплазме клетки и выполняющие различные функции по ее жизнеобеспечению. Сами органеллы делятся на мембранные и немембранные. К первым относятся, например, удивительный «аппарат Гольджи» (Golgi apparatus), как его принято называть в биологии, открытый итальянским гистологом Камилло Гольджи. Он напоминает поезд из мембранных цистерн, работающий на станции, его задача – сортировать проходящие через станцию белки. Если чуть более подробно, то аппарат, или станция Гольджи ответственна за три вида белковой массы: плазматическую мембрану, секреты – жидкости, выделяемые клетками, в которой содержатся биологически активные вещества, и энзимы – молекулы белка, которые служат для ускорения химических процессов в клеточных организмах.

Строение клетки
К немембранным органеллам относится рибосома, играющая фундаментальную роль в синтезе белковых молекул из аминокислот по программе, которая в свою очередь определена генетическим кодом – матричной РНК. Эта мРНК в свою очередь состоит из последовательности кодонов – единиц генетического кода, или триплетов, содержащих тройку нуклеотидов. В эукариотических клетках, о них шла речь выше, рибосомы могут располагаться как на мембранах ретикулума (эндоплазматической сетки), так и быть сателитами цитоплазмы, то есть находиться в незакрепленном на ней виде.
Репликация вирусов с позитивным геномом, к которым относится и коронавирус (на сегодняшний день выявлены два его штамма, типа L и S), происходит благодаря способности геномной РНК выступать в качестве мРНК после заражения. Авторы «Вирусологии» отмечают, что «это имеет двоякие последствия. Во-первых, ферменты, ответственные за репликацию генома, синтезируются после заражения, и нет необходимости в их внесении в зараженную клетку вместе с вирионом ‹…› Во-вторых, так как все позитивные геномы относятся к монолитным и все их гены сосредоточены в одной хромосоме, первичный продукт трансляции обеих РНК (как геномной, так и мРНК) обязательно представляет собой единый белок»[14]. У вируса с негативным геномом прибавляется работа: его геномная РНК служит панелью одновременно для редупликации и транскрипции, то есть заражение должно быть внесено в клетку заранее. Работы, конечно, у «негативистов» больше, но при этом у них есть и преимущество: при промощи splicing’а (который МакКлинток исследовала на кукурузе) – процесс создания зрелого РНК, когда вырезаются интроны и сшиваются экзоны[15] – обеспечивает формирование ряда мРНК с одного и того же участка генома. В этом случае вирус берет под тотальный контроль клеточный белок.
Это – если очень кратко и схематично. Сколько-нибудь подробное изложение сложнейшей механики клетки и ее заражения вирусами не входит в нашу задачу, сказанное необходимо лишь для того, чтобы читатель смог приблизительно визуализировать эти процессы. Для детального углубления в материал нам понадобится не один месяц занятий, у вируса же эти знания отчасти врожденные, отчасти приобретаемые.
Как в Средних веках в Европе, когда в профессиональной сфере началась специализация и стали возникать цеха, у вирусов тоже есть своя специализация – по хозяевам. Иначе говоря, он опасен для одних и безопасен для других. Например, натуральной оспой (variola vera) может заболеть только человек. Это не означает, однако, что другая клада штаммов – ветвь культуры данного вируса – не могла ранее заражать кого-то другого. Штамм – принятое в науке условное обозначение культуры, или как еще говорят, субкультуры, вирусов, существующей в определенное время и имеющей определенные генетические характеристики. Во многом это научная идеализация, как «частица» в физике.





