
Полная версия
От атомов к древу: Введение в современную науку о жизни
Еще более широко известны сахара, основу которых образуют цепочки из пяти или шести атомов углерода. Такие сахара называют, соответственно, пяти- или шестиуглеродными. Познакомимся для начала с тремя их представителями:
• рибоза – пятиуглеродный сахар с четырьмя гидроксильными группами и альдегидной группой;
• глюкоза – шестиуглеродный сахар с пятью гидроксильными группами и альдегидной группой;
• фруктоза – шестиуглеродный сахар с пятью гидроксильными группами и кетогруппой.
Краткую формулу рибозы можно записать так: C5H10O5. А глюкоза и фруктоза – изомеры с общей формулой C6H12O6. Сравнив их графические формулы, легко увидеть, что глюкоза отличается от фруктозы только положением группы – CO– (в глюкозе на конце углеродной цепочки, а во фруктозе внутри нее). Этого достаточно, чтобы дать веществу совсем другие химические свойства. И действительно, фруктоза несколько иначе, чем глюкоза, участвует в нашем обмене веществ. Именно поэтому ее часто используют в качестве заменителя обычного сахара (в состав которого глюкоза как раз входит). Сладкие продукты “на фруктозе” можно сейчас найти в любом супермаркете.
Мир кислот
Следующий интересный класс веществ – карбоновые кислоты (см. рис. 1.7). Это соединения, в состав которых входит группа – CO – OH (она называется карбоксильной). Любая карбоновая кислота по общему виду формулы похожа на альдегид, но отличается от него “лишним” атомом кислорода, который и превращает альдегидную группу (–CO – H) в карбоксильную (–CO – O–H). Общая формула карбоновой кислоты: R – COOH, где R – любая углеводородная цепочка или просто атом водорода.
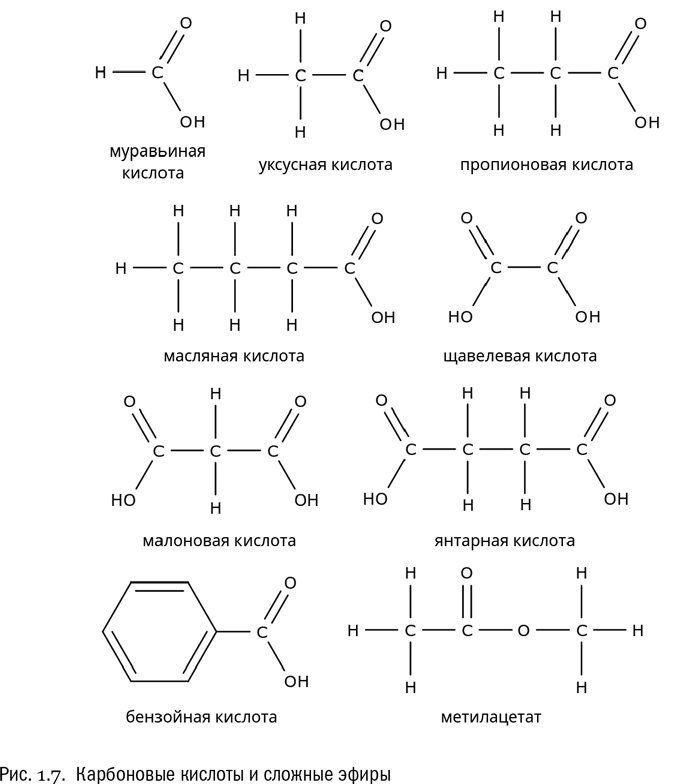
Простейшая карбоновая кислота – муравьиная (HCOOH). Следующая по сложности – уксусная (CH3COOH), затем – пропионовая (C2H5COOH), масляная (C3H7COOH) и т. д. Бывают и гораздо более экзотично выглядящие карбоновые кислоты: например, щавелевая, молекула которой представляет собой две карбоксильные группы, соединенные встык (HOOC–COOH). Она действительно есть в щавеле, а также в ревене и некоторых других растениях. Или бензойная кислота, имеющая в качестве радикала ароматическое ядро (C6H5COOH). Она тоже содержится во многих растениях, например в бруснике и клюкве, а еще служит широко распространенным консервантом (пищевая добавка E210).
Более того, молекула карбоновой кислоты вполне может включать в себя и другие группы, кроме карбоксильной. Например, в некоторых кислотах помимо карбоксильных групп есть гидроксильные (см. рис. 1.8). Такие соединения, по определению, являются одновременно кислотами и спиртами. Их называют спиртокислотами или (чаще) оксикислотами. Именно к этому классу относится важный промежуточный продукт нашего обмена веществ – молочная кислота, молекула которой включает три атома углерода, одну карбоксильную группу и одну гидроксильную (CH3–CHOH – COOH). Винная кислота, химию которой в свое время изучал великий Луи Пастер, устроена чуть сложнее: четыре атома углерода, две карбоксильные группы и две гидроксильные (HOOC–CHOH – CHOH – COOH). Она действительно есть в вине, а иногда добавляется и в еду, например в кондитерские изделия (пищевая добавка Е334). Заметим, что пугаться таких добавок не стоит: очень часто они, как в данном случае, представляют собой безобидные вещества, с тем же успехом изобилующие в самых что ни на есть натуральных продуктах. Винной кислоты, например, много в винограде и яблоках.
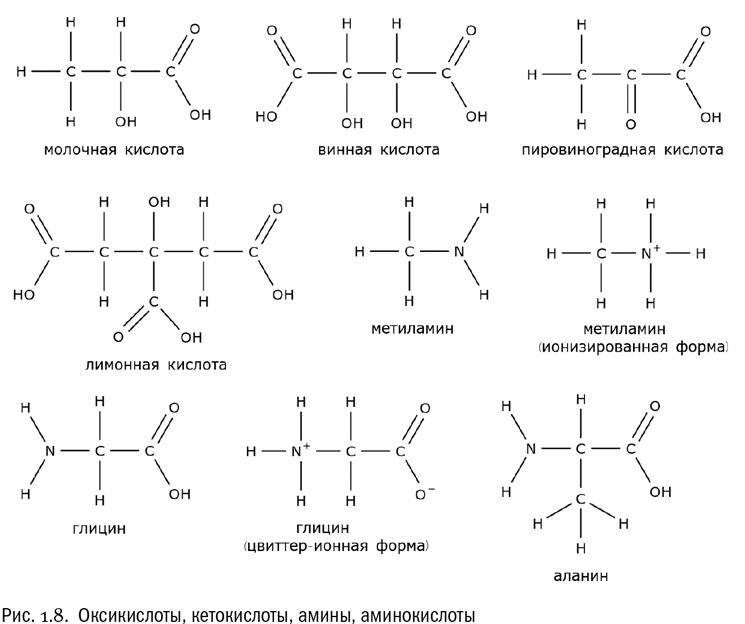
Бывают и такие кислоты, которые одновременно являются альдегидами или кетонами. Тут достаточно одного примера: пировиноградная кислота – простейшая кетокислота с формулой CH3–CO – COOH. Эта молекула тоже играет огромную роль в нашем обмене веществ (см. главу 11).
И еще несколько слов о спиртах. Карбоновая кислота и спирт могут вступить между собой в реакцию, при которой от карбоксильной группы отщепляется – OH, а от спиртовой – H. Эти отщепленные фрагменты тут же образуют воду (формула которой H – O–H или H2O). А остатки кислоты и спирта соединяются в сложный эфир – молекулу с общей формулой R1–CO – O–R2. Надо учитывать, что сложные эфиры и уже знакомые нам простые эфиры – это совершенно разные классы соединений, которые ни в коем случае нельзя путать. По-английски, например, они обозначаются разными корнями, соответственно ester (сложный эфир) и ether (простой эфир). Среди биологически активных веществ есть и те и другие, но сложных эфиров там в целом больше. Без знания того, что это такое, невозможно разобраться, например, в устройстве клеточной мембраны.
Кислоты versus основания
А теперь нам самое время задаться вопросом, что такое кислота. И заодно – что такое основание.
Начнем с кислоты. Как правило, кислотой называют молекулу, которая в водном растворе диссоциирует (это высоконаучный термин, означающий “распадается”) на катион водорода, то есть протон (H+), и некий анион. Например, уксусная кислота (CH3COOH) распадается в водном растворе на протон и ацетат-ион, имеющий формулу CH3COO–. Так же ведут себя и все остальные карбоновые кислоты. И не только карбоновые, но и любые другие. Например, соляная кислота (HСl) потому и называется кислотой, что распадается в воде на протон (H+) и ион хлора (Cl–). Правда, на самом-то деле протон не способен самостоятельно существовать в водном растворе – он всегда мгновенно захватывается водой, образуя так называемый ион гидроксония (H3O+). Концентрацию именно этих ионов реально измеряют при определении кислотности раствора.
Шведский химик Сванте Аррениус определял кислоту как соединение, диссоциирующее в водном растворе с образованием протона (H+), а основание – как соединение, диссоциирующее в водном растворе с образованием гидроксил-иона (OH–). Это определение – исторически первое и до сих пор самое известное, именно его обычно учат на уроках химии в школе. Хороший пример основания по Аррениусу – едкий натр NaOH, он же гидроксид натрия или просто натриевая щелочь. Это типичное ионное соединение. Даже в твердом состоянии натриевая щелочь состоит из ионов [Na+] и [OH–], а в воде она на эти ионы тут же распадается.
Теперь – плохая новость. В биохимии определение кислот и оснований по Аррениусу совершенно неприменимо. Вместо него мы будем пользоваться определением датского химика Йоханнеса Николауса Брёнстеда: кислота – молекула, отдающая протон, основание – молекула, принимающая протон.
Что это значит? Пусть, например, у нас взаимодействуют уксусная кислота и вода. В процессе взаимодействия от уксусной кислоты (CH3COOH) оторвется протон (H+), который перейдет к воде (H2O). В результате получатся анион CH3COO– и катион H3O+. В этой реакции уксусная кислота “работает” кислотой (она отдала протон), а вода – основанием (она присоединила протон). Это и есть определение Брёнстеда. Запись этой реакции будет такой:
CH3COOH + H2O ⇌ CH3COO– + H3O+
А если для простоты проигнорировать участие воды, то такой:
CH3COOH ⇌ CH3COO– + H+
По Брёнстеду, “кислота” или “основание” – это не постоянное свойство соединения, а только и исключительно его роль в данной химической реакции. В принципе даже уксусная кислота может оказаться в “непривычной” для себя роли основания, если смешать ее с какой-нибудь более сильной кислотой – например, серной (H2SO4). В этом случае серная кислота отдаст протон и превратится в анион HSO4–, а уксусная кислота присоединит протон и превратится в довольно редкий, однако вполне реально существующий катион CH3COOH2+:
CH3COOH + H2SO4 ⇌ HSO4– + CH3COOH2+
И, по нашему определению, уксусная кислота в этой реакции будет основанием.
К счастью, условия, с которыми приходится иметь дело в биологии, настолько однотипны, что для подавляющего большинства веществ смена ролей кислот и оснований там редкость. Так что мы можем смело считать кислотой любую молекулу, которая в условиях живой клетки обычно отдает протон, а основанием – любую молекулу, которая в условиях живой клетки обычно его присоединяет. Единственное важное исключение – вода. Она примерно с одинаковым успехом может и отдавать протон, и присоединять его. Для всех остальных веществ “роли” кислот и оснований тут более-менее постоянны.
Одно из самых распространенных в природе оснований – гидроксил-ион OH–, тот самый, который образуется при диссоциации щелочи. Он очень легко присоединяет к себе протон и превращается в воду. Но с тем же успехом в составе основания может и не быть атомов кислорода. Например, аммиак (NH3) – образцовое основание, никакого кислорода не содержащее. В растворе молекула аммиака присоединяет к себе протон и превращается в катион аммония (NH4+). Кстати, этот ион очень похож по структуре на молекулу метана (CH4). Различаются они только зарядом ядра центрального атома.
А теперь вернемся к органической химии. Соединения углерода, в которых есть группа – NH2, называются аминами. Общая формула аминов: R – NH2. Сама группа – NH2 называется аминогруппой. При желании вполне можно сказать, что амин – это аммиак, у которого вместо одного из атомов водорода углеводородная цепочка. Аминогруппа в составе амина сохраняет основные свойства (такие же, как у аммиака), поэтому амины остаются полноценными основаниями. Самый простой из всех возможных аминов – метиламин (CH3–NH2), где атом углерода всего один. Как и следует из названия, он состоит из двух групп: метильной и аминогруппы. Между прочим, это то самое вещество, с кражами которого был связан ряд приключений героев захватывающего сериала “Во все тяжкие” (Breaking Bad).
Что ж, двинемся еще на шаг вперед. Любое вещество, включающее одновременно аминогруппу (–NH2) и карбоксильную группу (–COOH), то есть являющееся одновременно амином и карбоновой кислотой, называется аминокислотой. Вот мы и добрались до насущного хлеба биохимиков. Роль аминокислот в живых организмах огромна: они служат и питательными веществами, и промежуточными продуктами обмена веществ, и – это, пожалуй, самое главное – “кирпичиками”, из которых строятся важнейшие для земной жизни молекулы, а именно белки. Как именно это происходит, мы узнаем в главе 3.
Любая аминокислота проявляет одновременно кислотные свойства (как карбоновая кислота) и основные (как амин). Когда аминокислота попадает в водный раствор, ее карбоксильная группа обычно теряет протон, зато аминогруппа в тот же самый момент протон приобретает. В результате получается цвиттер-ион – нейтральная молекула, разные части которой несут компенсирующие друг друга разноименные заряды. Карбоксильная группа, отдав протон, становится анионом, аминогруппа, присоединив протон, становится катионом, а суммарный электрический заряд молекулы аминокислоты в результате остается равным нулю.
Самая простая из всех возможных аминокислот – глицин. Формула глицина: NH2–CH2–COOH. Интересно, что в нашем организме, как и в организмах многих животных, глицин служит нейтротрансмиттером, то есть веществом, передающим сигналы в нервной системе. Причем его действие на нервные клетки – тормозящее, то есть затрудняющее возбуждение. Именно поэтому глицин часто принимают в качестве успокоительного. Так вот, по химической формуле это типичная аминокислота. В цвиттер-ионной форме она будет выглядеть так: NH3+–CH2–COO–.
Углеродный шовинизм
Сейчас мы знаем уже довольно много о химических “слагаемых” жизни. Мы знаем, что такое спирты, альдегиды, кетоны, карбоновые кислоты, простые и сложные эфиры, углеводы, амины и аминокислоты. Все это – соединения углерода. Но вот вопрос: обязательно ли любая жизнь должна быть основана на углероде?
Мнение, что жизнь может быть только углеродной, еще в 1970-х годах стали называть “углеродным шовинизмом”. Люди, употреблявшие этот термин – например, известный философ Пауль Фейерабенд, – считали “углеродный шовинизм” признаком ограниченности воображения ученых, не способных допустить существование чего-то высокоорганизованного, но при этом принципиально отличающегося от привычных нам земных животных и растений. Этот подход отлично спародировал Станислав Лем в “Звездных дневниках Ийона Тихого”. Есть там эпизод, где один ученый-негуманоид, житель огненной планеты с аммиачной атмосферой, поучает своего студента следующим образом:
“Как выглядят разумные существа иных миров? Прямо не скажу, подумай сам, научись мыслить. Прежде всего они должны иметь органы для усвоения аммиака, не правда ли? Какое устройство сделает это лучше, чем скрипла? Разве они не должны перемещаться в среде в меру упругой, в меру теплой, как наша? Должны, а? Вот видишь! А как это делать, если не хожнями? Аналогично будут формироваться и органы чувств – зрявни, клуствицы и скрябы…”
Что ж, не будем уподобляться косному мудрецу с огненной планеты. Включим воображение. В мысленных экспериментах на роль химической основы жизни не раз предлагались вместо углерода другие элементы, способные создавать цепочки атомов, – кремний (Si), бор (B) или азот (N). Однако бор и азот имеют валентность 3, а не 4, и это уже ограничивает разнообразие соединений, которые из них можно получить. При этом бора во Вселенной чрезвычайно мало, а длинные цепочки атомов азота образуются только при огромных давлениях, какие могут существовать разве что в глубинах планет-гигантов. В условиях, более-менее напоминающих земные, самым вероятным кандидатом на роль заменителя углерода остается кремний. Он имеет подходящую валентность 4, образует соединения, подобные углеводородам, и может реагировать с кислородом. Но есть несколько причин, по которым углерод при прочих равных условиях все же больше подходит на роль химической основы жизни.
Во-первых, углерод легко образует двойные связи (важнейшее для земной биохимии свойство!), а кремний из-за большего размера атома к этому неспособен.
Во-вторых, двуокись углерода (CO2) – это при нормальных условиях углекислый газ, прекрасно растворяющийся в воде. А двуокись кремния (SiO2) при тех же условиях – тугоплавкое твердое вещество с кристаллической решеткой, прошитой множеством ковалентных связей. Чистый SiO2 – это попросту кварц. Очевидно, что включить его в обмен веществ было бы гораздо труднее, чем углекислоту CO2.
В-третьих, кремний-кремниевая связь менее прочна, чем углерод-углеродная, поэтому кремневодороды по сравнению с углеводородами гораздо легче разлагаются.
В итоге надо признать: вероятность, что жизнь на других планетах окажется углеродной, достаточно высока. И тот факт, что наша собственная жизнь оказалась углеродной, определенно неслучаен. Но это вовсе не значит, что живые существа, возникшие в любой точке Галактики, будут копиями земных! Любители поспорить о возможности кремниевой жизни зачастую упускают из виду, что альтернативная биохимия, очень сильно отличающаяся от земной, в принципе может быть получена и без всякого нарушения “углеродного шовинизма”.
Давайте-ка еще раз присмотримся к химическим компонентам живых клеток. Из тех веществ, которые нам уже знакомы, в состав клеток входят, прежде всего, спирты, углеводы, сложные эфиры, карбоновые кислоты, оксикислоты и аминокислоты. Что у них общего? Ответ однозначен: все эти соединения – кислородсодержащие. Мы уже видели, что группы, за счет которых они отличаются друг от друга, почти всегда включают кислород (аминогруппа тут – единственное исключение, но и в аминокислотах кислород по определению всегда есть). Итак, земная жизнь построена из кислородсодержащей органики.
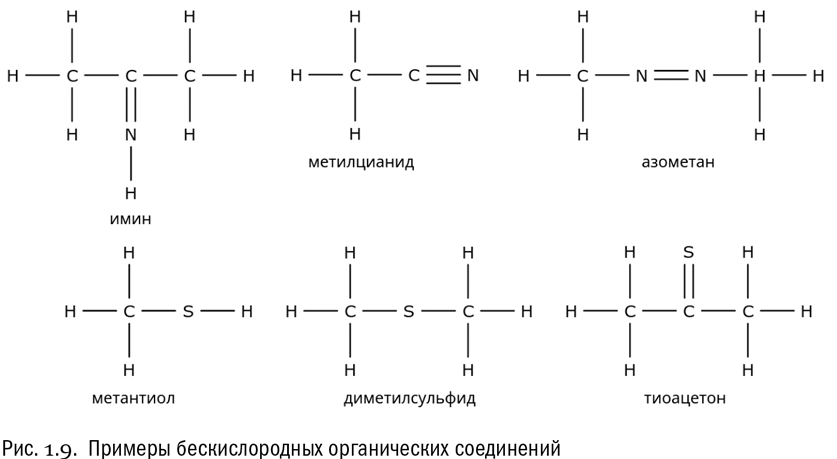
Однако ниоткуда не следует, что эта возможность – единственная. В состав органических молекул вполне могут входить и многие другие элементы помимо кислорода – например, азот и сера. С азотом мы уже знакомы, а о сере (S) сейчас достаточно сказать, что ее валентность в органических веществах чаще всего равна двум – как у кислорода. А теперь назовем навскидку несколько классов органических соединений, в которых есть азот или сера, зато никакого кислорода нет (см. рис. 1.9):
• имины – соединения с двойной связью между углеродом и азотом (C=N);
• нитрилы – соединения с тройной связью между углеродом и азотом (C≡N);
• азосоединения, включающие двойную связь между атомами азота (N=N);
• тиолы, тионы, тиоэфиры, тиоальдегиды и тиокарбоновые кислоты – аналоги, соответственно, спиртов, кетонов, простых эфиров, альдегидов и карбоновых кислот, в состав которых вместо кислорода входит сера.
Зная валентности элементов, мы можем легко представить себе набор простых представителей иминов (CH3–CNH – CH3), нитрилов (CH3–C≡N), азосоединений (CH3–N=N – CH3), тиолов (CH3–SH), тионов (CH3–CS – CH3), тиоэфиров (CH3–S – CH3), тиоальдегидов (CH3–CS – H) и тиокарбоновых кислот (CH3–CS – SH). В химическом “зоопарке” Земли это довольно редкие экспонаты – настолько, что не во всяком учебнике химии найдется упоминание о них. Но везде ли во Вселенной дело обстоит именно так? Мы этого не знаем. Если какая-нибудь планета будет по своему элементному составу обеднена кислородом, то вполне возможно, что основой жизни на этой планете послужит не кислородсодержащая органика, а азотсодержащая или серосодержащая. Такая жизнь будет вполне “углеродной” и тем не менее химически совсем иной, чем земная.
Есть, например, предположения, что молекулярная основа инопланетной жизни может иметь смешанный углеродно-азотный скелет{15}. Аналог углеводорода, построенный на таком скелете, мог бы выглядеть так: CH2=N – CH2–CH=N – CH2–CH=N–… – и т. д. А где возможны углеводороды (или хотя бы что-то на них похожее), там наверняка возможны и более сложные вещества.
Можно добавить, что в современных списках наиболее вероятных химических предшественников жизни кислородсодержащей органики на самом-то деле не так уж и много{16}. Зато там фигурируют такие интересные молекулы, как ацетилен (H – C≡C – H), сероводород (H2S), аммиак (NH3), синильная кислота (H – C≡N) и цианамид (NH2–C≡N). Глядя на эти формулы, уже нетрудно допустить, что химические “кирпичики” инопланетных живых существ, отличающиеся от привычных нам сахаров и аминокислот, но имеющие похожие функции, в принципе могли бы оказаться и бескислородными. Во всяком случае, набор возможностей здесь точно гораздо шире того, что удалось реализовать на Земле.
2. Вода
Что такое вода?
Ученые ответят: Н2O.
А Дональд Биссет:
– Алмазы на траве.
НАТАЛЬЯ ШЕРЕШЕВСКАЯ(ИЗ КНИГИ ДОНАЛЬДА БИССЕТА “ЗАБЫТЫЙ ДЕНЬ РОЖДЕНИЯ”)Вода – одно из самых распространенных веществ на планете Земля. Она покрывает две трети земной поверхности, и ее очень много в живых организмах – гораздо больше, чем любого другого вещества. Подавляющее большинство биохимических реакций, то есть превращений жизненно важных молекул друг в друга, идет в растворах, где вода является растворителем. Воды много и в космосе – например, в кометах, в недрах Урана и Нептуна или в межзвездных туманностях. В целом можно сказать, что вода – это одно из самых распространенных веществ не только на Земле, но и вообще во Вселенной. Иное дело, что далеко не на всех планетах она встречается в жидком виде (Земля – единственная планета Солнечной системы, на поверхности которой есть постоянно существующие водоемы). Так или иначе, неудивительно, что именно вода послужила средой для всем нам знакомой жизни.
Что же такое вода с точки зрения химии? Это весьма простая молекула, состоящая всего лишь из двух атомов водорода (H) и одного атома кислорода (O). Соответственно, химическая формула воды – H2O. Каждый атом водорода соединен с атомом кислорода одной ковалентной связью, в полном соответствии с валентностью кислорода, которая (как мы помним) равна двум. Формулу воды можно записать и так: H – O–H. Это эквивалентно формуле H2O, которую обычно приводят в книгах.
Многие свойства воды объясняются тем, что ее молекулы исключительно хорошо “слипаются” друг с другом. Например, на поверхности водоема они образуют пленку, по которой клопы-водомерки, отнюдь не микроскопические существа, бегают как посуху. Другие особенности воды как вещества – прекрасная теплопроводность и высокая температура кипения (на испарение литра воды надо потратить больше энергии, чем на испарение того же объема чуть ли не любой другой жидкости). Чтобы понять, почему вода именно такова, надо присмотреться к ее молекулам повнимательнее.
Водородная связь
Начнем вот с чего. В общей химии часто встречается понятие “электроотрицательность”, введенное когда-то Лайнусом Полингом. Электроотрицательность – это сила, с которой атом в составе молекулы оттягивает на себя общие с другим атомом электроны, образующие ковалентную связь. Самый электроотрицательный элемент – фтор (F), а сразу за ним на шкале электроотрицательности следует кислород (O). Иначе говоря, кислород превосходит по электроотрицательности все другие атомы, за исключением фтора, который в живой природе встречается очень редко. Запомним этот факт, он нам пригодится.
Электроотрицательность одинаковых атомов по определению равна. Если между двумя одинаковыми атомами есть ковалентная связь, то образующая ее пара электронов никуда не смещается. Грубо говоря, эти электроны располагаются между атомами точно посредине. Такая ковалентная связь называется неполярной. Само собой разумеется, что любая ковалентная связь между одинаковыми атомами будет неполярна (например, связь в молекуле водорода H – H или углерод-углеродная связь C–C).
Если же ковалентную связь образуют два разных атома, то общие электроны смещаются к тому из них, у которого электроотрицательность выше. Такая связь называется полярной (см. рис. 2.1, 2.2А). При очень большой разнице в электроотрицательности связь может даже превратиться в ионную – это случится, если один атом полностью “отберет” общую пару электронов у другого. В молекулах, из которых состоят живые существа, ионные связи встречаются относительно редко, зато ковалентные полярные – очень часто. Например, это широко распространенные в органических веществах связи C – O и H – O (см. главу 1).
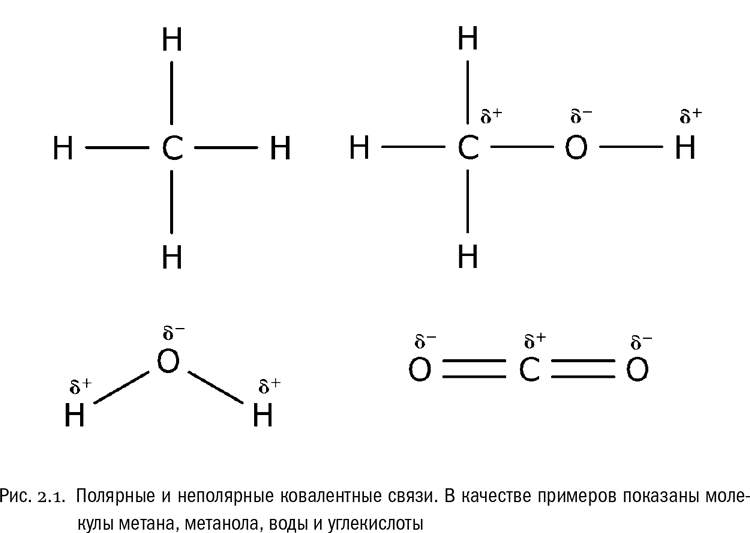
Связь между водородом и кислородом в молекуле воды – это типичная ковалентная полярная связь. Электроотрицательность кислорода намного выше, поэтому общие электроны смещены к нему. В результате на атоме кислорода образуется маленький отрицательный заряд, а на атомах водорода – маленькие положительные заряды. На графических формулах эти маленькие заряды, величина которых значительно меньше единицы, принято обозначать буквой δ (“дельта”) с добавлением соответствующего знака. Как мы теперь знаем, связи кислорода с водородом или углеродом вообще всегда полярные. Молекулы, в которых много таких связей, несут многочисленные частичные заряды, отрицательные на кислороде и положительные на водороде или углероде (см. рис. 2.1, 2.2Б).
А вот связь между углеродом и водородом (C – H) считается неполярной, хоть атомы и разные. И это тоже очень важно. Между атомами углерода и водорода разница в электроотрицательности настолько мала, что смещение электронов там незаметно. Например, молекулы углеводородов, состоящие только из атомов C и H, в силу этого полностью неполярны, никаких частичных зарядов, которые хоть на что-то влияли бы, в них нет.
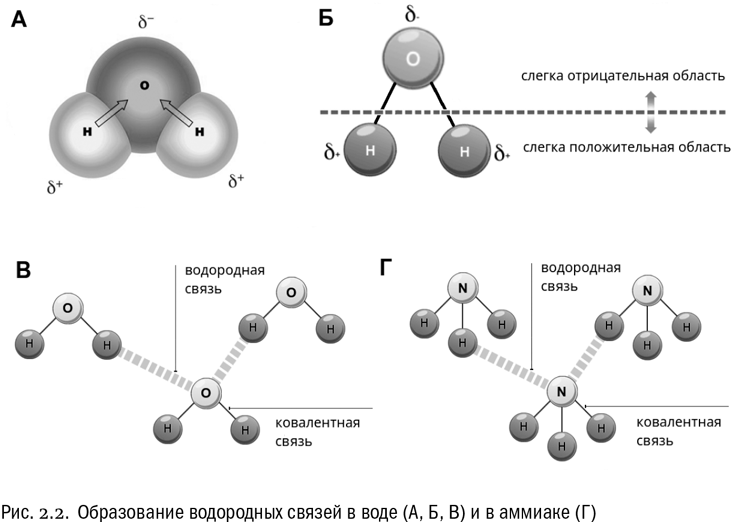
Теперь вспомним, что положительные и отрицательные электрические заряды согласно закону Кулона притягиваются друг к другу. Например, частично отрицательный атом кислорода одной молекулы воды притягивается частично положительными атомами водорода других молекул воды. В результате между водородом и кислородом возникают нековалентные связи, основанные на электростатическом притяжении, – они называются водородными (см. рис. 2.2В). Это очень слабые связи, в жидкой воде они легко образуются и так же легко рвутся при движениях молекул. Но, несмотря на то что водородные связи гораздо слабее ковалентных, они дают сильный эффект, если их много. А в воде их очень много. Например, именно из-за колоссального количества водородных связей у воды исключительно высокая теплоемкость – ее трудно нагреть и трудно остудить. Большинство особенностей воды так или иначе связано с тем, что ее молекулы очень хорошо образуют водородные связи.
“Водородная связь чем-то напоминает любовь втроем”, – писал в своем известном университетском учебнике американский биохимик Люберт Страйер{17}. Он имел в виду, что в водородной связи атом водорода связан сразу с двумя атомами кислорода: с одним ковалентно (и прочно), а с другим электростатически (и слабо). Чтобы образовать водородную связь, атом водорода обязательно должен уже состоять в ковалентной связи с другим атомом, причем значительно отличающимся от него по электроотрицательности.





