
Полная версия
Фармакотерапия гестоза
В дальнейшем гемоциркуляторные нарушения в сочетании с тканевой и клеточной гипоксией приводят к функциональным и морфологическим изменениям в органах и системах жизнеобеспечения – мозге, печени, почках, фетоплацентарной системе и др.
Вследствие неспособности органов и систем, регулирующих гомеостаз, к устранению промежуточных и конечных продуктов обмена возникают метаболические расстройства, характеризующиеся избыточным накоплением в организме недоокисленных продуктов обмена, свободных радикалов, перекисных соединений, что приводит к метаболическому ацидозу. Последний способствует прогрессированию обменных нарушений, в частности истощению компонентов АОС организма беременной.
Так создается порочный круг, усугубляющий изменения гомеостаза при гестозе (рис. 4).
Таким образом, все сказанное выше позволяет предположить, что патофизиологические механизмы гестоза обусловлены антиоксидантной недостаточностью. Первостепенное значение при этом имеют нарушения, касающиеся центральных и периферических нервных механизмов, сердечной деятельности, сосудистого и внутрисосудистого русла, процессов тканевого дыхания в организме матери, которыми определяется последовательность патологических сдвигов, приводящих к отеку, гиповолемии, диспротеинемии и дисэлектролитемии, нарушениям микроциркуляции, олигурии, гипертензии, нарушению маточно-плацентарного кровообращения, гипотрофии и риску внутриутробной гибели плода, выявленных при изучении данной патологии.
Выраженность клинических проявлений заболевания зависит как от силы и длительности действия патогенных факторов риска, так и от степени истощения компонентов АОС, роль которых сводится к защите биосубстратов организма беременной от патогенного действия этих факторов.
В пользу этого предположения говорит терапевтический эффект, достигнутый при комплексном применении триады препаратов, обладающих антиоксидантными свойствами, – унитиола, АК и токоферола.
Не вызывает сомнений необходимость продолжения исследований, направленных на всестороннее и глубокое изучение молекулярных механизмов антиоксидантной защиты при гестозе. Эти работы могут позволить пересмотреть некоторые традиционные представления о патогенезе заболевания и соответственно его фармакотерапию.
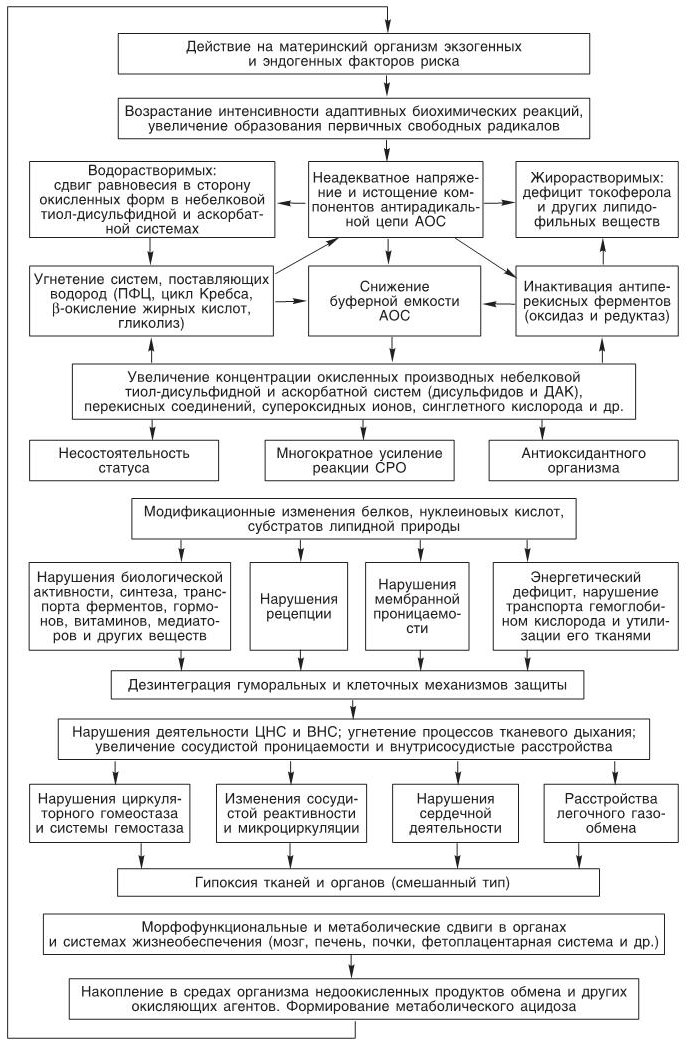
Рис. 4. Схема патогенетических механизмов развития гестоза
СПОСОБЫ ЛАБОРАТОРНОЙ ДИАГНОСТИКИ КЛИНИЧЕСКИХ ФОРМ И СТЕПЕНИ ТЯЖЕСТИ ГЕСТОЗА
• Определение соотношения концентраций восстановленных и окисленных форм тиолов и аскорбиновой кислоты SH/SS и АК/ОФ в крови – способ лабораторной диагностики клинических форм и степени тяжести гестоза [Соколовский В. В., Баскаков В. П., Абрамченко В. В. и др., 1982].
В литературе последних лет уже неоднократно высказывалось мнение о том, что редуцированные формы (SH-группы и АК) являются малоинформативными и не всегда объективными показателями истинного состояния окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах. Достоверное представление о состоянии равновесия в указанных системах возможно лишь на основании оценки соотношения концентраций восстановленных и окисленных форм тиолов и аскорбиновой кислоты SH/SS и АК/ОФ [Соколовский В. В. и др., 1974]. В связи с этим у больных, страдающих гестозом отечно-нефротического ряда, определялись не только редуцированные формы (АК и SH-групп), но и их окисленные производные (ОФ и SS-группы). Критериями, характеризующими состояние и степень выраженности нарушений в исследуемых системах, явились восстановительноокислительные коэффициенты SH/SS и АК/ОФ.
Выявленные нарушения характеризовались увеличением содержания окисленных форм аскорбиновой кислоты и белковых SS-групп, уменьшением редуцированных форм АК и белковых SH-групп, а также уменьшением восстановительноокислительных коэффициентов SH/SS и АК/ОФ. Указанные изменения коррелировались с тяжестью течения патологии. Вместе с тем необходимо отметить, что на фоне количественного увеличения окисленных форм аскорбиновой кислоты и белковых SS-групп в ряде случаев в крови больных одновременно определялось относительно высокое содержание редуцированных форм АК и SH-групп. В этих случаях нарушения в белковой тиол-дисульфидной и аскорбатной системах только лишь по количественному содержанию восстановленных форм АК и белковых SH-групп, как это предлагают Р. Л. Шуб (1961), К. В. Воронин и соавт. (1978), Д. З. Григорян (1981), без учета показателей их окисленных форм (ОФ и SS-групп), указывают на незначительные сдвиги окислительно-восстановительного равновесия в исследуемых системах. Показатели АК и SH-групп свидетельствовали о легком течении патологии. В то же время на основании клинической картины заболевания у больных было диагностировано тяжелое течение гестоза.
Таким образом, редуцированные формы АК и белковых SH-групп являются малоинформативными и не всегда объективными показателями истинного состояния окислительновосстановительного равновесия в белковой и аскорбатной системах крови. Использование их в акушерской практике в качестве критериев, характеризующих состояние и степень выраженности нарушений в тиол-дисульфидной и аскорбатной системах крови больных, а также тестов лабораторной диагностики клинических форм гестозов может привести к ошибочному заключению о состоянии равновесия в указанных окислительно-восстановительных системах и, следовательно, о тяжести клинического течения патологии.
Предлагаемые восстановительно-окислительные коэффициенты и АК/ОФ исключают возможность подобной ошибки, являются объективными и информативными показателями, характеризующими истинное состояние окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах крови больных, что позволяет рекомендовать их в качестве достоверных ранних прогностических и диагностических тестов.
• Способ лабораторной диагностики клинических форм и степени тяжести гестозов путем определения показателей стабильности липопротеиновых комплексов в сыворотке крови.
Нарушению синтеза и стабильности липопротеиновых комплексов (ЛПК) придается большое значение в патогенетических механизмах увеличения мембранной проницаемости и развитии гипоксии при различных заболеваниях. Имея в виду важность этой информации для понимания патогенеза гестоза, определялась стабильность ЛПК в сыворотке крови больных, изучалась их роль в биохимических механизмах, лежащих в основе сосудистых нарушений и развитии гипоксии при данной патологии. Для определения прочности связи липид – белок в ЛПК использован метод Л. Л. Делямуро (1968).
Результаты исследования показали, что если в поздние сроки нормально протекающей беременности имеется лишь тенденция к изменению стабильности ЛПК, то при беременности, осложненной гестозом, дестабилизация ЛПК явно выражена, при этом она тем значительнее, чем тяжелее течение заболевания. Особенно ценным является то, что изменения показателей стабильности ЛПК определялись раньше выраженных клинических симптомов патологии. Иными словами, опережали клиническую картину заболевания.
Кроме того, отмечалась нормализация показателей стабильности ЛПК при клиническом выздоровлении больных.
Учитывая значение обнаруженных нарушений в патогенетических механизмах развития патологии, пришли к выводу о целесообразности определения показателей стабильности ЛПК сыворотки крови с целью использования их в акушерской практике в качестве ранних прогностических и диагностических тестов оценки развития гестозов, контроля эффективности лечения и определения сроков госпитализации больных с данным заболеванием [Соколовский В. В., Баскаков В. П., Абрамченко В. В., Варфоломеев Д. И., Костюшов Е. В., 1982].
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ АНТИОКСИДАНТОВ В АКУШЕРСКОЙ ПРАКТИКЕ
Выраженность клинических проявлений гестоза предположительно зависит от силы и длительности действия патогенных факторов и от степени истощения компонентов биоантиоксидантной системы (небелковой и тиол-дисульфидной и аскорбатной окислительно-восстановительных систем).
Исходя из этого, с целью коррекции выявленных нарушений в тиол-дисульфидной и аскорбатной окислительно-восстановительных системах в общепринятую схему лечения гестоза были дополнительно включены лекарственные средства, обладающие антиоксидантными свойствами, – 5 % раствор унитиола и 5 % раствор натриевой соли аскорбиновой кислоты.
Комплексная интенсивная терапия проведена 93 больным гестозом: 43 (контрольная группа) получали лечение по общепринятой схеме; 50 (основная группа) проводилась терапия, при которой в общепринятую схему лечения была включена комбинация указанных препаратов. Показатели состояния тиол-дисульфидной и аскорбатной систем с вычислением коэффициентов SH/SS и АК/ОФ определялись до начала и на 6-е сутки лечения.
Первая серия исследований.43больных контрольной группы (отеки беременных, нефропатия I – III ст.) получали лечение по общепринятой схеме – диетотерапию, гипотензивные препараты, магнезиальную терапию, транквилизаторы, спазмолитики, мочегонные, антигистаминные препараты и др. Кроме того, проводилась инфузионная терапия – гемодез, реополиглюкин, комплексы аминокислот и альбуминов.
Препараты назначались по показаниям в зависимости от формы и степени тяжести патологии. Несмотря на клиническое улучшение течения заболевания, показатели величин коэффициентов SH/SS, АК/ОФ, используемых в качестве объективных критериев, характеризующих истинное состояние окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах, и устойчивости ЛПК крови по сравнению с показателями до лечения существенно не изменились, что рассматривается как свидетельство продолжающегося патологического процесса.
Вторая серия исследований. 50 больным основной группы (отеки беременных, нефропатия I – III ст.) кроме препаратов, предусмотренных общепринятой схемой лечения, вводили 5 % раствор унитиола (из расчета 1 мл на 10 кг массы тела на введение) в сочетании с 5 % раствором натриевой соли аскорбиновой кислоты (из расчета 2 мл на введение) – 3 инъекции в сутки.
Терапевтический эффект выражался в нормализации исследуемых показателей (коэффициентов SH/SS, АК/ОФ и устойчивости ЛПК крови) у больных с отеками и нефропатией I ст. и значительном их улучшении у больных с нефропатией II и III ст. по сравнению с показателями до лечения. Наряду с этим отмечалось клиническое улучшение течения заболевания.
Проводилось сравнение терапевтического эффекта у 50 больных основной группы с результатами лечения 43 больных контрольной группы. Анализ полученных данных показал, что при включении унитиола с аскорбиновой кислотой в комплекс общепринятых терапевтических средств у больных основной группы повышалась эффективность лечения и значительно снижались сроки лечения по сравнению с больными контрольной группы. В частности, стойкое клиническое улучшение состояния отмечено у 33 (76,74 %) больных контрольной группы на 8,24 ± 0,58-й день лечения, в то время как у 48 (96 %) больных основной группы стойкое улучшение наступало на 5,12 ± 0,48-й день (p < 0,001). У этих больных быстрее нормализовалось артериальное давление, уменьшались отеки, улучшались клинические и биохимические показатели крови.
Изучение особенностей течения родов у обследованных больных показало, что при применении комплексной терапии унитиола с аскорбиновой кислотой снизилось в 3 раза число преждевременных и запоздалых родов, уменьшилось в 3 раза число патологических кровопотерь и в 2,5 раза – число оперативных вмешательств. Средняя продолжительность родов (в часах) сократилась с 16,4 ± 3,8 в контрольной группе (лечение по общепринятой схеме) до 9,6 ± 2,3.
• Положительный терапевтический эффект, полученный при применении унитиола с аскорбиновой кислотой, подтверждает патогенетическую роль тиол-дисульфидной и аскорбатной окислительно-восстановительных систем в развитии гестоза беременных и позволяет рекомендовать их применение в комплексном лечении данной патологии.
• Вторым показанием к сочетанному применению унитиола с аскорбиновой кислотой является гипоксия плода. Данные объективного изучения состояния плода методом кардиотокографии показали: при однократном применении указанных средств у 36 рожениц, страдающих гестозом, состояние сердечной деятельности плода после внутримышечного (22 роженицы) и внутривенного (14 рожениц) введения унитиола с аскорбиновой кислотой в I периоде родов характеризовалось статистически достоверным увеличением внутриминутных колебаний частоты сердцебиения плода – с 4,05 ± 0,28 до 6,04 ± 0,28 уд./мин. (p < 0,001) после внутримышечного и с 4,22 ± 0,35 до 6,66 ± 0,34 уд./мин. (p < 0,001) после внутривенного введения препаратов, а также повышением миокардиального рефлекса с 16 ± 1,34 до 20,05 ± 1,12 (p < 0,05) после внутримышечного и с 13,11 ± 2,61 до 18,72 ± 1,14 (p < 0,05) после внутривенного введения препаратов, что указывает на улучшение состояния плода.
• Третьим показанием к применению комбинации унитиола с аскорбиновой кислотой является лечение слабости родовой деятельноси (СРД), которое проведено у 46 рожениц в I периоде родов. Данные клиники и наружной многоканальной гистерографии, которая проводилась на протяжении всего I периода родов, показали статистически достоверное повышение маточной активности, выражающееся в увеличении амплитуды с 8,76 ± 0,44 до 11,39 ± 0,61 мм (p < 0,001) после внутримышечного (32 роженицы) и с 9,53 ± 0,9 до 14,37 ± 1,15 мм (p < 0,05) после внутривенного введения (14 рожениц) препаратов и возрастанием частоты сокращений матки за 10 мин. с 3,13 ± 0,34 до 4,22 ± 0,31 (p < 0,05) после внутримышечного и с 3,18 ± 0,16 до 4,37 ± 0,35 (p < 0,001) после внутривенного введения.
Это дает основание считать, что применение унитиола и аскорбиновой кислоты в родах способствует улучшению обменных процессов в миометрии, следствием чего является повышение маточной активности.
Полученные данные свидетельствуют о необходимости применения смеси указанных антиоксидантов в акушерской практике в комплексной терапии гестоза с целью интра- и антенатальной защиты плода, а также в качестве средств, усиливающих родовую деятельность.
КОНЦЕПЦИЯ ГЕНЕЗА ГИПОКАЛЬЦИЕМИИ ПРИ ГЕСТОЗЕ
Общеизвестно, что поддержание кальциевого гомеостаза является одним из важнейших условий нормального функционирования жизненно важных органов и систем.
С этой точки зрения трудно переоценить значение гипокальциемии в возникновении целого каскада нефизиологических реакций в системе мать – плацента – плод во время беременности, осложненной гестозом. Вместе с тем вопрос о молекулярных механизмах, лежащих в основе дефицита кальция при рассматриваемой патологии, до сих пор остается открытым.
Так, в исследовании Roelofsen et al. (1988) изучен метаболизм Ca и Mg в моче и крови при нормальной беременности и при беременности, осложненной гипертензией, или при задержке роста плода. У всех обследуемых уровень Ca в течение беременности снижался. При этом содержание ионизированного Ca не менялось. Концентрация Mg в крови снижалась в начале беременности и оставалась на одном уровне в III триместре. Отмечено, что концентрация Mg в крови повышена при задержке роста плода. Экскреция Ca и Mg с мочой возрастает при беременности и не зависит от осложнений. Таким образом, метаболизм Ca и Mg слабо меняется при патологии беременности.
В противоположность этим данным в работе Taufield et al. (1987) была поставлена задача: может ли гипокальциурия являться прогностическим критерием развития токсикоза. С этой целью авторы выделение Ca с мочой определяли у 40 беременных с гипертензиейиу10женщин с неосложненным течением беременности. Содержание ионизированного Ca и P в сыворотке крови в обеих группах было одинаковым, экскреция Ca с мочой у здоровых беременных составляла 313 ± 140, при транзиторной гипертензии – 248 ± 138, при гипертонической болезни – 233 ± 41, при токсикозе – 42 ± 29, при сочетанной его форме – 78 ± 49 мг/сут. Фракционная экскреция Ca с мочой была ниже при гестозе, чем в других группах.
Экскреция Na с мочой оказалась одинаковой. Снижение экскреции Ca с мочой может служить четким лабораторным критерием гестоза. Лечение Mg и Ca приводит к увеличению выделения Ca с мочой. Гипокальциурия служит для дифференцирования гестоза от других заболеваний беременных, сопровождающихся гипертензией. Остается неясным, может ли гипокальциурия являться прогностическим критерием развития гестоза.
В этой связи значительный интерес представляют экспериментальные данные о зависимости кальциевого обмена от состояния окислительно-восстановительного гомеостаза и прежде всего тиол-дисульфидной и аскорбатной систем организма [Мусил Я., 1985; Bruyn et al., 1977; Gambardella, Richardson, 1977].
Отсутствие в литературе сведений о роли тиол-дисульфидной и аскорбатной окислительно-восстановительных систем в молекулярных механизмах генеза гипокальциемии при гестозе послужило основанием для настоящей работы.
С этой целью комплексному клиническому обследованию с использованием современных клинико-физиологических и биохимических методов подверглись 228 женщин в возрасте от 18 до 40 лет, которых распределили следующим образом.
В 1-ю группу вошли женщины с физиологически протекающей беременностью при сроке 38 – 40 нед., в том числе и в начале нормальных родов (всего 38 человек). Указанная группа была взята в качестве контроля (табл. 1).
Таблица 1
Биохимические показатели плазмы крови больных гестозом
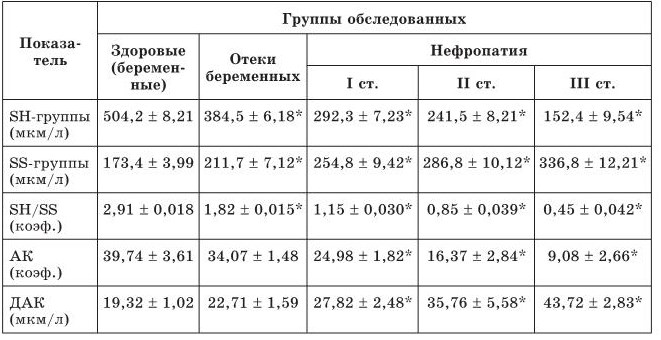
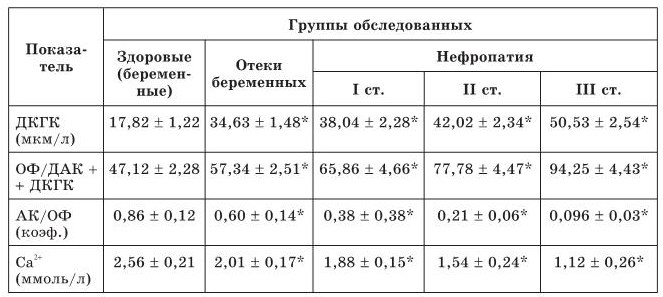
* Показатель статистически достоверно отличается от своего значения в контрольной группе (p < 0,05).
Последующие четыре группы (190) составили женщины с беременностью 32 – 40 нед., осложненной гестозом беременных, распределенные на основании клинических признаков заболевания по формам и степени тяжести согласно принятой классификации: 2-я группа – отеки беременных (80), 3-я – нефропатия I ст. (66), 4-я – нефропатия II ст. (26), 5-я – нефропатия III ст. (18).
У всех обследуемых определялось содержание оксалатов в моче, проводилось биохимическое исследование крови с целью изучения состояния тиол-дисульфидной системы, аскорбатной окислительно-восстановительной системы и кальциевого гомеостаза.
В работе использованы методы прямого и обратного амперометрического титрования сульфгидрильных (SH) и дисульфидных (SS) групп, раздельного определения редуцированной формы аскорбиновой кислоты (АК) и ее окисленных форм – дегидроаскорбиновой (ДАК) и дикетогулоновой (ДКГК) кислот [Соколовский В. В. и др., 1974, 1977]. Концентрация кальция в плазме крови определялась методом плазменной фотометрии. О наличии оксалатов судили на основании данных микроскопического осадка мочи. Получены также данные содержания стероидных гормонов в сыворотке крови в контрольной группе с использованием радиоиммунологического метода с применением стандартных наборов KIT фирмы «CEA – IRE – SORIN». Результаты исследований были подвергнуты математической обработке методами вариационной статистики [Беленький М. Л., 1963] (табл. 2).
Таблица 2
Выраженность оксалатурии в моче больных гестозом
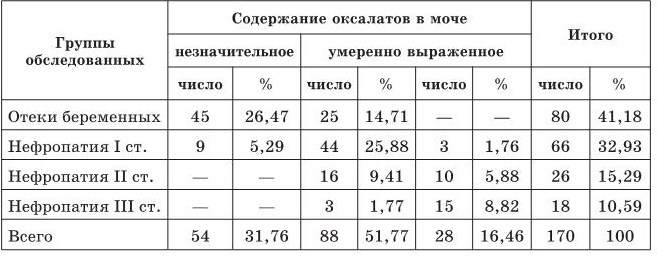
Анализ полученных данных показал (см. табл. 1 и 2), что развитие гестоза сопровождается глубокими нарушениями состояния окислительно-восстановительного равновесия в тиолдисульфидной и аскорбатной системах плазмы крови больных по сравнению с контролем. Эти нарушения характеризуются уменьшением содержания редуцированных форм (SH-групп и АК) указанных систем и увеличением концентрации их окисленных производных (SS-групп и ДАК + ДКГК), что наиболее наглядно проявляется в уменьшении величин коэффициентов SH/SS и АК/ОФ. Наряду с этим обнаружен дефицит кальция в плазме крови и увеличение оксалатов в моче больных. Причем в ходе проведенных исследований установлена прямая зависимость тяжести клинического течения патологии и степени выраженности указанных нарушений. Особо необходимо акцентировать внимание на то, что интенсивность сдвигов окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах, в свою очередь, коррелировала с выраженностью гипокальциемии и оксалатурии в плазме крови больных (рис. 5).
Необходимо отметить, что в контрольной группе не удалось выявить статистически достоверных изменений со стороны содержания стероидных гормонов и концентрации ионов кальция при сравнении показателей при 38 – 40 нед. беременности и во время начала родов. Так, эстриол соответственно составлял 264,7 ± 35,7 и 205,1 ± 28,3 мкг/мл, эстрадиол 26,93 ± 3,16 и 18,16 ± 2,8 мкг/мл, содержание прогестерона незначительно уменьшалось с 179,83 ± 18,25 до 102,63 ± 7,53 мкг/мл (p < 0,05), концентрация ионов кальция оставалась стабильной – 2,46 ± 0,08 и 2,26 ± 0,04 ммоль/л.
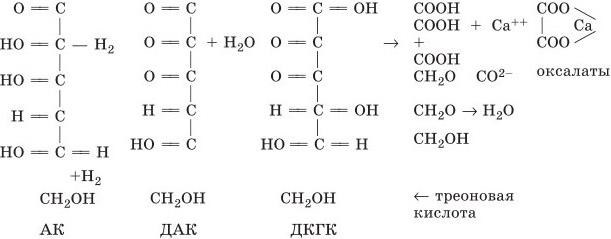
Рис. 5. Механизм образования оксалатов в плазме крови больных гестазом
В свете этих данных возможные причины гипокальциемии при гестозе беременных могут состоять в следующем.
Во-первых, окисление редуцированной формы АК приводит к накоплению ее окисленных производных – ДАК и ДКГК кислот. Последняя (ДКГК), как известно, являясь необратимо окисленной формой АК, в свою очередь, расщепляется на щавелевую и треоновую кислоты. Появление высоких концентраций щавелевой кислоты в различных средах организма при усилении процессов окисления АК обнаружили ряд исследователей [Мусил Я., 1985; Wapnick et al., 1968; и др.]. Исходя из этого, представляется, что биологический эффект ДКГК обусловлен появлением в организме больных одного из продуктов ее расщепления – щавелевой кислоты в значительном количестве, которая, взаимодействуя с ионами кальция плазмы крови, образует оксалаты, частично выводящиеся с мочой, вследствие чего происходит потеря кальция организмом. В пользу этого заключения свидетельствуют данные нашей работы. В частности, в результате проведенных исследований была обнаружена корреляционная зависимость между увеличением содержания ДКГК в плазме крови больных, с одной стороны, и уменьшением уровня кальция в плазме крови и увеличением концентрации оксалатов в моче больных – с другой. Правомерность высказанного предположения подтверждается результатами исследований ряда авторов, выявивших увеличение концентрации оксалатов в моче при введении в организм АК в больших количествах на фоне повышенной оксидазной активности [Мусил Я., 1985; и др.].
Во-вторых, известно, что появление оксалатов в организме может быть непосредственно связано с нарушениями процессов их оксалирования (распада). В то же время механизмы нарушения оксалирования обусловлены снижением активности ряда тиоловых ферментов: оксалатдекарбоксилазы (4.1.1.2), оксалат-оксидазы (1.2.3.4), оксалат-КоА-лигазы (6.2.1.8), оксалат-КоА-трансферазы (2.8.3.2)1. Активность тиоферментов, как известно, определяется состоянием тиол-дисульфидной системы организма, сдвиг которой в сторону окисления приводит к их инактивации. Поэтому есть все основания полагать, что нарушениями окислительно-восстановительного равновесия в тиол-дисульфидной и аскорбатной системах, обнаруженными при гестозе, может быть обусловлено снижение активности тиоловых ферментов, принимающих участие в процессах оксалирования. В этих условиях возможность образования и присутствия оксалатов в организме больных становится еще более вероятной.
Естественно, предлагаемая концепция не исчерпывает всей сложности возможного механизма гипокальциемии при гестозе. Тем не менее развивающиеся при данной патологии нарушения окислительно-восстановительного равновесия играют важную роль в генезе гипокальциемических состояний.
Таким образом, при гестозе закономерно возникают нарушения окислительно-восстановительного гомеостаза с уменьшением редуцированных и увеличением окисленных форм компонентов тиол-дисульфидной и аскорбатной систем. Эти нарушения в количественном выражении прямо пропорциональны степени выраженности клинических проявлений гестоза; одним из наиболее вероятных механизмов гипокальциемии является увеличение щавелевой кислоты как следствие описанного сдвига окислительно-восстановительного гомеостаза на фоне резкого снижения активности тиоловых ферментов и угнетения естественного механизма оксалирования.
РОЛЬ ФИКСИРОВАННЫХ В ПЛАЦЕНТЕ ИММУННЫХ КОМПЛЕКСОВ В ПАТОГЕНЕЗЕ ГЕСТОЗА
Гестоз является одним из наиболее тяжелых видов акушерской патологии и встречается у 12 – 20 % беременных. Несмотря на многочисленные исследования патогенетических механизмов развития заболевания и появление новых методов лечения гестоза, он продолжает занимать ведущее место среди причин материнской и перинатальной заболеваемости и смертности. Гестоз является причиной материнской смертности в 9,6 – 20 % случаев, а перинатальная смертность в 3 – 4 раза превышает этот показатель у женщин без гестоза [Айламазян Э. К., 1993; Репина М. А., 1988; Савельева Г. М. 1996]. При гестозе хроническая гипоксия плода и асфиксия новорожденных отмечается в 17 – 58,3 % случаев, гипотрофия плода и новорожденного – в 14,6 – 20,8 %. В неонатальном периоде у детей от матерей с гестозом часто наблюдаются такие осложнения, как нарушение мозгового кровообращения, постгипоксическая энцефалопатия, синдром дыхательных расстройств, нарушение процесса адаптации к внеутробной жизни [Озерец Н. А. и др., 1996]. Высокая частота гестоза и характер его осложнений для матери и плода диктуют необходимость дальнейшего изучения патогенеза этого заболевания в поисках новых методов профилактики и лечения.


