
Полная версия
Код иммунитета. Как циркадные ритмы, питание и хронический стресс влияют на иммунное старение
В 1918 году появилась микробная теория инфекций, которая утверждала, что микроорганизмы, иначе говоря микробы, вызывают заболевания. Это был самый современный взгляд на причины множества заболеваний. Для устранения патогенов применялись различные методы лечения, такие как антитоксические сыворотки, кровопускание и новые вакцины (первую вакцину от оспы разработали в 1798 году), но работали они неважно, за исключением нескольких вакцин против сравнительно мало мутирующих вирусов. [35] Самым эффективным терапевтическим средством того времени было переливание плазмы крови. Введение крови или плазмы от переболевших пациентов больным, находящимся в тяжелом состоянии, снизило уровень смертности на 50 %. [36] Выжившие после перенесенных инфекционных заболеваний вырабатывали антитела к вирусу и иммунитет, который надежно защищал их от определенного штамма, по крайне мере на некоторое время. В этом заключалась идея вакцинирования.
Во время вспышки испанского гриппа заболевших было настолько много, что медицинские учреждения были вынуждены оказывать минимальную помощь пациентам и надеяться, что они сами справятся с инфекцией. В Бостоне и Массачусетсе многие медработники и пациенты не погибли только из-за пребывания в госпиталях под открытым небом, которые организовывали в школах, общественных приемных, на кораблях и в частных усадьбах. [37] Полевые госпитали устраивали в местах «с максимальным доступом солнечного света и свежего воздуха днем и ночью». [38] В Восточном Бостоне из 5100 моряков, находившихся на борту кораблей, испанским гриппом заразились 1200 человек. [39] В самых плохо проветриваемых отсеках кораблей у больных развивалась тяжелая форма пневмонии. Из 154 медицинских работников заразились только шестеро медсестер и двое санитарок, причем в пяти случаях они подхватили вирус не на рабочем месте.
Свежий воздух, солнце и тщательная личная гигиена помогли значительно сократить количество смертельных исходов. Эта практика, получившая название аэротерапия (лечение свежим воздухом), была впервые предложена английским врачом Джоном Коукли Леттсомом (1744–1815), который лечил больных туберкулезом детей при помощи морского воздуха и солнечного света. [40] Действительно, витамин D, ультрафиолетовое излучение и кислород обладают противовирусными и антибактериальными свойствами, за счет чего, безусловно, поддерживают иммунную систему. [41] Рахит – детское заболевание, развивающееся на фоне дефицита витамина D, связывают с развитием респираторных инфекций, а низкий уровень витамина D повышает риск заражения гриппом. [42] Лабораторные исследования показали, что ультрафиолетовое излучение дезактивирует вирус гриппа и другие патогены, [43] а также уничтожает бактерии. Кроме того, под действием солнечного света лучше заживали гнойные боевые ранения, и больные быстрее выздоравливали. [44] Также было доказано, что у больных, перенесших сердечный приступ, было больше шансов выжить, если они лежали в солнечных палатах. [45] Если быть кратким, то солнечный свет полезен для сердца и иммунной системы.
После Первой мировой войны исследованиями противовирусных свойств свежего воздуха продолжил заниматься физиолог сэр Леонард Хилл. В 1919 году в медицинском журнале British Medical Journal он писал, что дыхание холодным воздухом и сон под открытым небом – это лучшие средства борьбы с вирусом гриппа, а солнечный свет помогает добиться положительных результатов при лечении туберкулеза. [46] Свежий воздух оказывает стерилизующее воздействие даже на самые мельчайшие патогенные частицы. [47] Неизвестно, сколько именно свежего воздуха нужно запускать в помещение, чтобы предотвратить развитие инфекционных заболеваний, но определенно проветривать следует чаще, чем это принято в современных больницах, школах и офисах. [48]
Пандемии XXI века и извлеченные из них уроки
Пандемии постоянно вспыхивали на протяжении всей истории человечества, и они будут возвращаться снова. В 2020 году мир столкнулся с новым коронавирусом SARS-CoV2, который стал причиной эпидемии COVID-19. Прежде люди никогда не сталкивались с этой разновидностью коронавируса, а потому мы не располагали проверенной информацией о его вирулентности, способности вызывать летальный исход и потенциальных долгосрочных последствиях заболевания. Однако нам известно, что SARS-CoV2 в первую очередь убивает пожилых и людей с нарушенным обменом веществ. Если посмотреть на статистику по населению в целом, то количество заболеваний SARS-CoV2 со смертельным исходом составляет почти 3 % (в Соединенных Штатах Америки этот показатель составляет 2,86 %). [50] Вероятно эти цифры завышены и не отражают реальной частоты смертельных исходов (многие люди с SARS-CoV2 не обращались за помощью к врачам и выжили после инфекции). Тем не менее, по данным Всемирной организации здравоохранения, на 29 сентября 2020 года с инфекцией SARS-CoV2 было диагностировано более 33 млн человек по всему миру, один миллион из которых не смогли пережить заболевание.
Первая опасная вспышка коронавируса, известная как тяжелый острый респираторный синдром (SARS), произошла в 2003 году. Тогда заразились 8000 человек, из которых погибли 774 (что составило около 10 % случаев со смертельным исходом). Предположительно, вирус начал распространяться в Китае от летучих мышей и через пальмовых циветт – вид кошкообразных зверьков – перешел к человеку. Еще одна коронавирусная эпидемия, получившая название Ближневосточный респираторный синдром (MERS), началась по вине верблюдов в 2012 году в Саудовской Аравии. Всего к 2020 году вирусом заразились 2500 человек, из которых погибли 866 пациентов (что составило около 35 % случаев со смертельным исходом). Затем пришла лихорадка Эбола, которая с 1976 года испытывала на прочность население Африки к югу от Сахары. Сообщалось, что за 2013 год Эболой заразились 2387 человек, среди которых 1590 не смогли справиться с заболеванием (что составило около 66,6 % случаев со смертельным исходом). Конечно, эти цифры не так поражают, как смертоносные эпидемии чумы и пандемии прошлых веков. Однако текущая ситуация с SARS-CoV2 напоминает нам, что очередное серьезное заболевание, вероятно, притаилось буквально за углом. И в сложившихся обстоятельствах мы, как отдельные личности и члены общества, не можем просто почивать на лаврах. Невозможно отрицать тот факт, что сегодня разные регионы планеты теснее связаны друг с другом, чем в прошлом, и люди могут перемещаться по миру гораздо быстрее. А значит, беда может разразиться в течение одного дня.
В отличие от «испанки», коронавирусная инфекция COVID-19 заражала в основном старых и больных, и оказалась не настолько заразна. Бесспорно, любая потерянная жизнь – это повод для скорби, но количество погибших несоизмеримо с эпидемией испанского гриппа 1918 года. Тогда люди умирали через несколько дней или даже часов после инфицирования. Конечно, в то время рекомендации по гигиене намного уступали современным, но подумайте, сколько людей из ваших знакомых подхватили коронавирусную инфекцию и погибли за считанные дни? Большинство смертельных случаев от COVID-19 зафиксировано спустя две или три недели, а не через два или три дня.
Согласно последним исследованиям, жертвами вируса SARS-CoV2 чаще всего становятся пожилые, люди с ослабленным иммунитетом и такими сопутствующими патологиями, как диабет, гипертония, онкология, сердечно-сосудистые заболевания, заболевания печени и ожирение. [51] В основном к факторам риска относятся признаки нездорового образа жизни, которые поддаются коррекции. Любая смерть – это трагедия, но еще и важное напоминание, что наша первоочередная защита от вирусов – это метаболическое здоровье и крепкая иммунная система. Мы не можем предугадать появление нового вируса в другой части планеты, как и не можем взять под контроль его распространение по всему миру. Единственное, что нам действительно под силу контролировать, это состояние здоровья и иммунитет. Жизнь в современном обществе создает иллюзию защищенности, и мы привыкли ждать неизбежно счастливой развязки. К сожалению, природой управляют другие законы, и если мы хотим выжить во время пандемий, то мы должны как можно лучше заботиться о здоровье всего организма.
Пандемии прошлого преподали нам множество важных уроков. Вирусы склонны меняться и мутировать, поэтому медицинский подход к ним должен быть адаптивным. Однако вспышки заболеваний практически всегда проходят по одному и тому же сценарию, особенно в отношении человеческой природы и общественной реакции.
● Пандемии характеризуются несколькими волнами. Все эпидемии чумы и вспышки инфекционных заболеваний случались более одного раза. Очевидно, таковы правила жизни бок о бок с постоянно развивающимися вирусами. Каждые несколько столетий человечество сталкивалось с тремя наиболее беспощадными вспышками чумы. Страшно подумать, но до сих пор в мире каждый год насчитывается как минимум 12 случаев заболевания бубонной чумой. [52] Испанский грипп на протяжении двух лет то появлялся, то затухал, а Антонианова чума свирепствовала 15 лет, пока наконец не иссякла. И несмотря на это, люди продолжали жить и справляться с этой напастью. Мы не можем предугадать, сколько волн той или иной пандемии прокатится по нашему обществу и как долго это будет продолжаться. Поэтому крайне важно проявлять инициативу и принимать дополнительные защитные меры.
● Вакцины может и не быть. У нас нет вакцины от «испанки» и коронавирусных инфекций по типу тяжелого острого респираторного синдрома (SARS). Существующие вакцины от бубонной чумы и даже от гриппа не всегда срабатывают против новых, ежегодно появляющихся штаммов. Вакцины против РНК-содержащих вирусов тоже не могут похвастаться высокими показателями, потому что эти вирусы постоянно меняются. Конечно, мы не утверждаем, что вакцины не работают, хотя вопрос о степени их реальной эффективности пока остается открытым. И все же вакцина – это не панацея. И что самое важное, вакцины могут не оказать нужного эффекта на тех, кому они нужнее всего, то есть на пожилых и страдающих от ожирения людей. [53, 54, 55]
Можно сказать, человечеству пока что сопутствовала удача. В конце концов, мы смогли сохранить жизнь нашего вида и на протяжении тысячелетий успешно справлялись с нападками инфекций, чумы и вирусов. Впрочем, этим мы обязаны не столько везению, сколько нашей способности адаптироваться и выживать. Человеческое тело представляет собой самоадаптирующееся устройство, которое развивалось в неблагоприятных внешних условиях на протяжении нескольких тысяч лет. Оно позволило нам построить современную цивилизацию, но, к сожалению, созданная им защита может сделать нас уязвимыми перед неожиданными пандемиями будущего. Можно не сомневаться, что впереди нас ждет множество пандемий, и последние потрясения напомнили о важности активно следить за состоянием своего здоровья и иммунной системы. И для этого нужно обратиться к основам, а именно уделить внимание питанию, физическим упражнениям, сну, снятию стресса и прогулкам на открытом воздухе.
Глава вторая:
Основополагающие элементы иммунной системы и старение иммунитета
Иммунная система – это набор важнейших компонентов и процессов живых организмов, которые участвуют в выполнении различных функций. Она надежно защищает нас от угроз внешнего мира и инфекционных агентов. Крепкий иммунитет уверенно отталкивает инородные микроорганизмы и поддерживает тело в состоянии гомеостаза.
Абсолютно все живые организмы, в том числе простейшие и бактерии, наделены примитивной иммунной системой, которая называется системой рестрикции-модификации. [56] Базовые функции иммунитета растений и эукариот включают в себя производство противомикробных пептидов дефензинов, поглощение крупных частиц путем фагоцитоза и каскад комплемента, который усиливает эффективность антител. Люди и челюстноротые обладают более совершенными защитными механизмами, например, способностью со временем более эффективно распознавать определенные патогены и лучше к ним адаптироваться (адаптивный иммунитет). [57]
Иммунная система – это удивительно сложное явление. Она подразделяется на множество более мелких категорий и поддерживает связь со всеми системами тела, например, с сердечно-сосудистой, эндокринной и нервной системой. [58] Коротко говоря, иммунитет отвечает за распознавание патогенов и противодействие им, но на самом деле сфера его ответственности намного шире.
В этой главе мы рассмотрим основополагающие элементы иммунной системы и выясним, как они работают. Также мы обсудим компоненты иммунной системы, их иммунный ответ и защитные механизмы. Кроме того, мы узнаем, как стресс и процесс старения – неотъемлемые составляющие регуляции иммунного ответа организма – влияют на иммунитет.
Классификация иммунной системы
Слово «иммунитет» восходит к латинскому «immunis», что означает «невосприимчивый». То есть обладающий способностью противостоять инфекциям, патогенам, вредным микроорганизмам и вырабатывать иммунитет к болезням. Для оптимальной работы иммунной системе нужно уметь находить и устранять как можно больше патогенов, при этом отличать их от здоровых компонентов тела. В противном случае организм может атаковать сам себя, то есть спровоцировать аутоиммунную реакцию, что наносит такой же сильный вред организму, как и сама инфекция.
Иммунная система состоит из множества категорий и подсистем, которые включаются в работу на разных этапах развития инфекции или заболевания. Она работает по типу многослойной защиты, где такие физические барьеры, как кожа и слизистые оболочки, обеспечивают первый слой защиты. Они препятствуют попаданию в организм самых крупных и наименее сложно устроенных вредных микроорганизмов. Однако большинство бактерий и вирусов обладают настолько мелкими размерами, что протискиваются даже в самые крошечные лазейки. В этот момент иммунная система берет ситуацию под контроль и немедленно отвечает на вторжение.
Существуют две основные категории иммунной системы, которые управляют нашими защитными механизмами:
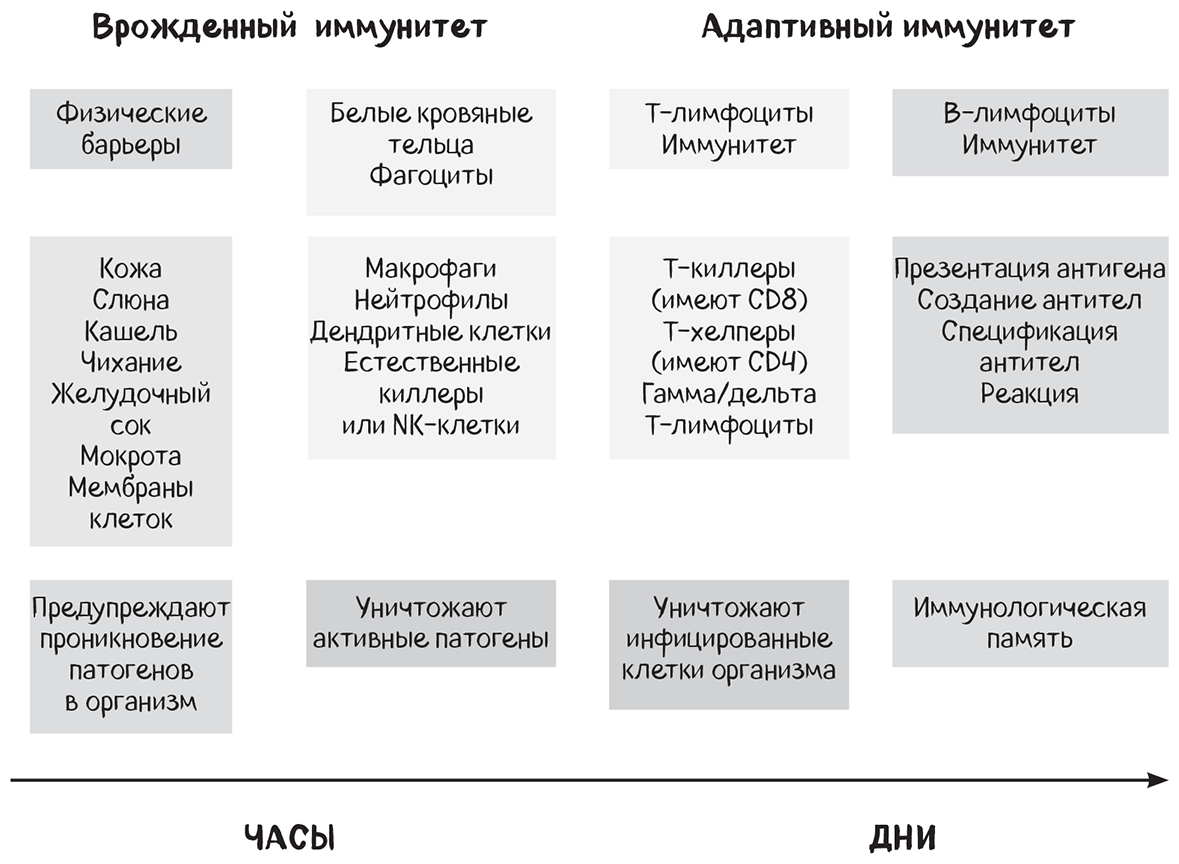
● Врожденный (естественный) иммунитет, который включает в себя большинство защитных сил организма. [59] С ним человек рождается и по умолчанию получает способность распознавать инородные вещества и реагировать на них неспецифическим, обобщенным способом. Врожденный иммунитет проявляет активность, когда микробы или патогены вторгаются в организм, и образраспознающие рецепторы (ОРР) распознают эти микробные компоненты. [60] То же происходит в момент получения травмы, нарушения физической целостности и стресса. [61] Все живые организмы используют рецепторы ОРР.
• К поверхностным защитным барьерам, которые препятствуют попаданию патогенов в организм, относятся кожа и слизистые оболочки животных, экзоскелет насекомых и внешняя оболочка листьев. Также существуют химические барьеры, такие как антимикробные пептиды, которые выделяет кожа, [62] антибактериальные ферменты слюны, слез, [63] грудного молока и желудочного сока. [64] Когда частицы попадают внутрь через функциональные отверстия тела, например, ноздри или рот, такие механические реакции, как чихание, кашель и мочеиспускание, помогают быстро избавиться от нависшей угрозы. [65]
• Образраспознающие рецепторы в основном представлены клетками врожденного иммунитета, например, дендритными клетками, макрофагами, моноцитами, нейтрофилами и эпителиальными клетками. [66] Они распознают патоген-ассоциированные молекулярные паттерны (ПАМП) и дефект-ассоциированные молекулярные паттерны (ДАМП). Внеклеточные ПАМП частично подтверждаются толл-подобными рецепторами. [67] Толл-подобные рецепторы запускают секрецию цитокинов, которые включают последующие защитные механизмы тела.
– Процесс уничтожения патогенов антителами реализуется за счет каскада или системы комплемента, в которой принимают участие более 30 различных белков. Эта система представляет наибольшее гуморальное звено врожденного иммунитета. [68] Система комплемента активирует фагоцитоз, воспаление и атаку клеточных мембран вредных бактерий.
– Антитела или иммуноглобулины (Ig) – это крупные белки Y-образной формы, которые производятся плазматическими клетками для обезвреживания патогенов. Они распознают специфические молекулярные характеристики у определенных патогенов-антигенов и помечают их как подлежащие уничтожению. У млекопитающих существует пять видов антител (IgA, IgD, IgE, IgG и IgM). [69]
• Врожденная иммунная система опосредована белыми кровяными тельцами (лейкоцитами), к которым относятся фагоциты (макрофаги, нейтрофилы, дендритные клетки), врожденные лимфоидные клетки, тучные клетки, эозинофилы, базофилы и естественные киллеры. Они либо физически атакуют и уничтожают патогены, либо поглощают их. [70] Второй процесс называется фагоцитозом и представляет собой древнейшую форму иммунной защиты организма. [71] Фагоциты мигрируют по организму в поисках инородных частиц и откликаются на зов цитокинов. [72]
– Дендритные клетки – это фагоциты, которые живут на коже, в носу, легких и кишечнике. Они поддерживают связь между тканями тела и иммунной системой, предоставляя (презентуя) антигены Т-лимфоцитам. [73]
– Естественные киллеры (NK-клетки) – это лимфоциты, которые не атакуют инородные частицы напрямую. Вместо этого они устраняют дисфункциональные защитные клетки организма, например, опухолевые клетки, стареющие или инфицированные клетки путем секреции цитотоксических молекул. [74] Естественные киллеры распознают инфицированные клетки по признаку «потеря своего», которым обладают клетки с низким уровнем мембранного маркера MHC I (главный комплекс гистосовместимости I). Нормальные здоровые клетки поддерживают оптимальный уровень MHC-антигенов, и NK-клетки их не трогают. [75]
• Воспаление – это мгновенный ответ врожденного иммунитета на появление инфекции. [76] В результате этой реакции появляются отек, жар, потоотделение, боль, а также усиливается прилив крови к поврежденной области. Повышение температуры обусловливают простагландины, которые представляют собой группу липидов-эйкозаноидов, обладающих гормоноподобным воздействием. [77] Также воспалительный процесс могут запускать цитокины, например, интерлейкины, которые поддерживают общение между белыми кровяными тельцами и интерферонами, которые управляют клеточными функциями в период вирусной инфекции. [78] Цитокины призывают иммунные клетки, чтобы те уничтожили патогены и инициировали процесс заживления. [79]
● Адаптивную иммунную систему человек приобретает в результате взаимодействия с различными патогенами на протяжении жизни. Каждая перенесенная инфекция записывается в иммунологической памяти, которая хранит воспоминания обо всех инфекционных агентах и наделяет их личными антигенами. [80] Это более специфическая реакция, которая запускается при распознавании чужеродных антигенов во время так называемой презентации антигена. Адаптивный иммунитет можно приобрести естественным путем через знакомство с вредными микроорганизмами, либо искусственным через вакцинацию. Впервые адаптивная иммунная система начала функционировать у позвоночных, так как у беспозвоночных видов она отсутствует. [81] Отметим, что адаптивный иммунитет способен помогать бороться даже с теми инфекциями, с которыми вы не сталкивались ранее. Например, ранее перенесенная простуда, вызванная обычными штаммами коронавируса, дает некоторую защиту от SARS-CoV2 в связи со сходством структур этих вирусов. [82, 83] Необходимо отметить, что иммунитет Т-клеток сохраняется десятилетиями, тогда как защита антител длится всего несколько месяцев. Для адаптивного иммунитета крайне важно наличие правильно функционирующих Т-лимфоцитов. К сожалению, по причине возраста, плохого питания и хронических заболеваний их функции деградируют.
• Адаптивная иммунная система состоит из лимфоцитов, таких как Т-клетки (Т-киллеры, Т-хелперы) и В-клетки (продуцирующие антитела), которые происходят от гемопоэтических стволовых клеток в костном мозге. Т-клетки связаны с клеточно-опосредованным иммунным ответом, в то время как В-клетки вовлечены в гуморальный иммунный ответ. Как только вредная инородная частица попадает в клетку, а значит, умудряется беспрепятственно обойти барьер антител, организм подключает Т-клетки для уничтожения патогена.
– Т-киллеры уничтожают инфицированные, поврежденные и неработоспособные клетки, [84] которые они узнают по антигенам, прикрепленным к молекулам MCH I. Этому процессу способствуют корецепторы CD8, расположенные на Т-лимфоцитах. Когда между ними устанавливается контакт, Т-клетки выпускают цитотоксины, которые проникают через мембрану клетки-мишени и инициируют апоптоз (программируемую клеточную смерть), [85] чтобы остановить репликацию вируса.
– Т-хелперы (или T-лимфоциты, имеющие CD4) влияют на врожденный и адаптивный иммунитет, помогая принимать решение, какой из иммунных ответов наилучшим образом подойдет к определенному патогену. [86] Они не обладают цитотоксическими или прямыми патогенными свойствами. Однако после активации Т-хелперы выбрасывают цитокины, которые усиливают бактерицидное воздействие макрофагов и повышают активность Т-киллеров. [87] Т-хелперы и регуляторные Т-лимфоциты распознают антигены на молекулах MCH II через экспрессию рецепторов на Т-лимфоцитах.
– Гамма/дельта Т-лимфоциты обладают теми же свойствами, что и Т-киллеры, Т-хелперы и NK-клетки. [88] На них расположены нетипичные рецепторы Т-лимфоцитов, состоящие из одной γ (гамма) цепи и одной δ (дельта) цепи в отличие от обычной αβ (альфа/бета). Наибольшую концентрацию гамма/дельта Т-лимфоцитов можно заметить в слизистой оболочке кишечника, которые участвуют в адаптивной и врожденной иммунной реакции. [89] Гамма/дельта Т-лимфоциты распознают интактные антигены, связанные с MCH-рецепторами.
• На поверхности В-лимфоцитов расположены антигенспецифические рецепторы В-клеток, которые распознают патогены полностью, без потребности в обработке антигенов. Они связываются с чужеродными антигенами и превращают их в антигенные пептиды посредством протеолиза. [90] Эти пептиды появляются на молекулах MCH II, расположенных на поверхности В-лимфоцитов, и привлекают Т-хелперов. Т-хелперы продуцируют лимфокины, которые активируют В-клетки. [91] В результате В-клетки начинают делиться, и их потомки секретируют миллионы антител, которые попадают в кровеносную и лимфатическую систему, где они распознают патогены, экспрессирующие определенный антиген. Затем они связываются с этими патогенами и помечают их на уничтожение. Каждая родственная линия В-лимфоцитов экспрессирует определенное антитело, таким образом весь комплекс антигенных рецепторов представляет совокупность антител, которые способно произвести наше тело. [92]
Патогены разработали множество механизмов, чтобы с их помощью успешно проникать в организм и инфицировать его, не попадаясь бдительным иммунным клеткам. [93] Бактерии прорывают внешние барьеры, выделяя пищеварительные ферменты через секреторную систему 2 типа. [94] При помощи секреторной системы 3 типа они пронизывают клетку-мишень шприцеподобным каналом, по которому направляют инфицированные белки и отключают защитные системы клетки. [95] Некоторые патогены, такие как сальмонеллы, которые вызывают пищевые отравления, и Plasmodium falciparum, которые несут ответственность за развитие малярии, прячутся в клетке-хозяине, чтобы ничем себя не выдать. Палочка Коха (Mycobacterium tuberculosis) закрывается в защитную капсулу. [96] Другие бактерии, например, синегнойная палочка (Pseudomonas aeruginosa) и Burkholderia cenocepacia у больных муковисцидозом, создают биопленку, которая защищает их от иммунных клеток. [97] Некоторые патогены на поверхности производят белки и соединения, которые лишают антитела эффективности. [98]
В-лимфоциты и Т-лимфоциты обладают долгосрочной памятью, в которой хранятся «записи» о всех патогенах, с которыми они сталкивались. Поэтому они сумеют эффективно противостоять им при следующей встрече. Здесь мы подходим к функции иммунологической памяти адаптивного иммунитета, которая формируется на протяжении жизни человека. Она может иметь вид пассивной краткосрочной или активной длительной памяти.
Эпизодические недомогания оказывают положительное воздействие на организм в течение длительного периода времени. Повышенная температура и не слишком агрессивные инфекции, перенесенные в раннем детстве, защищают во взрослой жизни.
Согласно результатам исследования 2019 года, переболевшие гриппом маленькие дети в будущем вырабатывают сильный иммунитет к мутировавшим штаммам того же вируса. [99] Когда мы получаем опыт взаимодействия с инфекциями, тело учится эффективно уничтожать похожие патогены. Однако бывают случаи, когда происходит совершенно противоположное. Например, корь может стирать приобретенную память иммунной системы, что делает человека беззащитным перед заболеванием. [100] Поэтому серьезные заболевания не приносят пользы, так как они истощают иммунные ресурсы организма, а недомогания, которые мы испытываем время от времени, наоборот, помогают человеку приспосабливаться.





