Полная версия
2. Guggisberg D, Hadj-Rabia S, Viney C, et al. Skin markers of occult spinal dysraphism in children: a review of 54 cases. Arch Dermatol 2004;140 (9): 1109.
3. Wright DR, Frieden IJ, Orlow SJ, et al. The misnomer «macrocephaly-cutis marmorata telangiectatica congenita syndrome»: report of 12 new cases and support for revising the name to macrocephalycapillary malformations. Arch Dermatol 2009; 145 (3):287.
4. Gonzalez ME, Burk CJ, Barbouth DS, et al. Macrocephaly-capillary malformation: a report of three cases and review of the literature. Pediatr Dermatol 2009;26 (3):342
5. Cordoro KM, Speetzen LS, Koerper MA, et al. Physiologic changes in vascular birthmarks during early infancy: mechanisms and clinical implications. J Am Acad Dermatol 2009;60 (4):669—75.
6. Swerlick RA, Cooper PH. Pyogenic granuloma (lobular capillary hemangioma) within port-wine stains. J Am Acad Dermatol 1983;8 (5):627—30.
7. Rajan N, Natarajan S. Impetiginized eczema arising within a port-wine stain of the arm. J Eur Acad Dermatol Venereol 2006;20 (8):1009—10.
8. Mulliken JB, Glowacki J. Classification of pediatric vascular lesions. Plast Reconstr Surg 1982;70 (1): 121.
9. Pascual-Castroviejo I, Pascual-Pascual S, Velazquez-Fragua R, et al. Sturge-Weber syndrome: study of 55 patients. Can J Neurol Sci 2008;35 (3): 301—7.
10. Comi AM. Sturge-Weber syndrome and epilepsy: an argument for aggressive seizure management in these patients. Expert Rev Neurother 2007;7 (8): 951e6.
11. Hennedige AA, Quaba AA, Al-Nakib K. Sturge-Weber syndrome and dermatomal facial port-wine stains: incidence, association with glaucoma, and pulsed tunable dye laser treatment effectiveness. Plast Reconstr Surg 2008;121 (4):1173—80.
12. Nelson JS, Geronemus RG. Redarkening of portwine stains 10 years after laser treatment. N Engl J Med 2007;356 (26):2745—6
13. Hershkovitz D, Bercovich D, Sprecher E, et al. RASA1 mutations may cause hereditary capillary malformations without arteriovenous malformations. Br J Dermatol 2008;158 (5):1035—40.
14. Boon LM, Mulliken JB, Vikkula M. RASA1: variable phenotype with capillary and arteriovenous malformations. Curr Opin Genet Dev 2005;15 (3): 265—9.
15. Revencu N, Boon LM, Mulliken JB, et al. Parkes Weber syndrome, vein of Galen aneurysmal malformation, and other fast-flow vascular anomalies are caused by RASA1 mutations. Hum Mutat 2008; 29 (7):959—65.
16. Kienast AK, Hoeger PH. Cutis marmorata telangiectatica congenita: a prospective study of 27 cases and review of the literature with proposal of diagnostic criteria. Clin Exp Dermatol 2009;34 (3): 319—23.
17. Fujita M, Darmstadt GL, Dinulos JG. Cutis marmorata telangiectatica congenita with hemangiomatous histopathologic features. J Am Acad Dermatol 2003;48 (6):950—4.
18. Ulrich S, Fischler M, Walder B, et al. Klippel-Trenaunay syndrome with small vessel pulmonary arterial hypertension. Thorax 2005;60 (11):971—3.
19. Minkis K, Geronemus RG, Hale EK. Port wine stain progression: a potential consequence of delayed and inadequate treatment? Lasers Surg Med 2009; 41 (6):423—6.
20. Lam SM, Williams EF. Practical considerations in the treatment of capillary vascular malformations, or port wine stains. Facial Plast Surg 2004;20 (1):71—6.
21. Owens WW, Lang PG. Herpes simplex infection and colonization with Pseudomonas aeruginosa complicating pulsed-dye laser treatment. Arch Dermatol 2004;140 (6):760—1.
22. Strauss RM, Sheehan-Dare R. Local molluscum contagiosum infection as a side-effect of pulsed-dye laser treatment. Br J Dermatol 2004;150 (5):1047—9.
23. Jasim ZF, Handley JM. Treatment of pulsed dye laser-resistant port wine stain birthmarks. J Am Acad Dermatol 2007;57 (4):677—82.
24. Yang MU, Yaroslavsky AN, Farinelli WA, et al. Longpulsed neodymium: yttrium-aluminum-garnet laser treatment for port-wine stains. J Am Acad Dermatol 2005;52 (3 Pt 1):480—90.
25. Kono T, Frederick Groff W, Chan HH, et al. Longpulsed neodymium: yttrium-aluminum-garnet laser treatment for hypertrophic port-wine stains on the lips. J Cosmet Laser Ther 2009;11 (1):11—3.
26. Borges da Costa J, Boixeda P, Moreno C, et al. Treatment of resistant port-wine stains with a pulsed dual wavelength 595 and 1064 nm laser: a histochemical evaluation of the vessel wall destruction and selectivity. Photomed Laser Surg 2009;27 (4):599—605.
27. Izikson L, Nelson JS, Anderson RR. Treatment of hypertrophic and resistant port wine stains with a 755 nm laser: a case series of 20 patients. Lasers Surg Med 2009;41 (6):427—32.
28. Reynolds N, Exley J, Hills S, et al. The role of the Lumina intense pulsed light system in the treatment of port wine stainsda case controlled study. Br J Plast Surg 2005;58 (7):968—80.
29. Ozdemir M, Engin B. Mevlitoglu I. Treatment of facial port-wine stains with intense pulsed light: a prospective study. J Cosmet Dermatol 2008;7 (2):127—31.
30. Faurschou A, Togsverd-Bo K, Zachariae C, et al. Pulsed dye laser vs. intense pulsed light for portwine stains: a randomized side-by-side trial with blinded response evaluation. Br J Dermatol 2009; 160 (2):359—64.
31. Yuan K, Li Q, Yu W, et al. Comparison of photodynamic therapy and pulsed dye laser in patients with port wine stain birthmarks: a retrospective analysis. Photodiagnosis Photodyn Ther 2008;5 (1): 50e7.
Лимфатическая мальформация
ЭТИОЛОГИЯ
Причины возникновения и развития лимфатических мальформаций (ЛМ) до сих пор полностью не изучены, остается очень много вопросов в тактике ведения данных пациентов и выборе методов лечения.
Эмбриональное развитие лимфатических сосудов начинается с перестройки венозных эндотелиальных клеток в лимфатические эндотелиальные клетки под влиянием факторов транскрипции (PROX1, SOX18 и COUPTF2). Затем эти клетки мигрируют и размножаются в окружающей мезенхиме, образуя первичные лимфатические мешочки, которые, расширяясь, образуют первичную древовидную лимфатическую сосудистую сеть, это происходит под действием сигнального пути VEGF-C/VEGFR-3 и ангиопоэтина-1. Считается, что нарушение регуляции данных процессов может привести к патологическому изменению лимфангиогенеза и образованию лимфатической мальформации. Проведенные исследования демонстрируют, что соматически активирующиеся мутации фермента PIK3CA могут нарушить и активировать клеточный сигнальный путь PI3K/AKT/mTOR, который участвует в ангиогенезе и лимфангиогенезе, а также в росте клеток и их метаболизме. Данные изменения могут приводить к развитию лимфатических мальформаций, но точный механизм четко не определен.
Соматические мутации PIK3CA были выявлены у пациентов с различными «сосудистыми» синдромами, связанными с гипертрофией тканей.
Поверхностные лимфатические мальфомации встречаются чаще, чем висцеральные, однако, четкие эпидемиологические данные отсутствуют. Частота лимфатических мальформаций в области лица и шеи составляет 1,2%—2,8%.
КЛАССИФИКАЦИЯ
Согласно классификации Международного общества по изучению сосудистых аномалий ISSVA лимфатическая мальформация относится к сосудистым мальформациям с медленным течением жидкости.
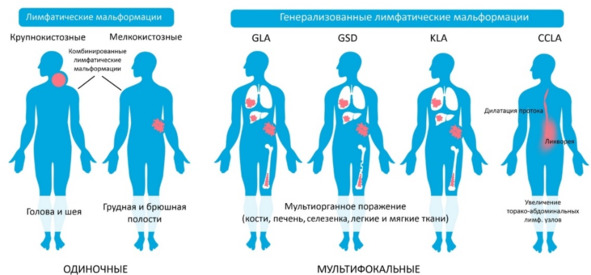
Виды лимфатических мальформаций.
Лимфатические мальформации могут быть изолированными, комбинированными (например, капиллярно-лимфатические или капиллярно-лимфатико-венозные мальформации) или ассоциированными с синдромами (например, Клиппеля-Треноне или CLOVES).
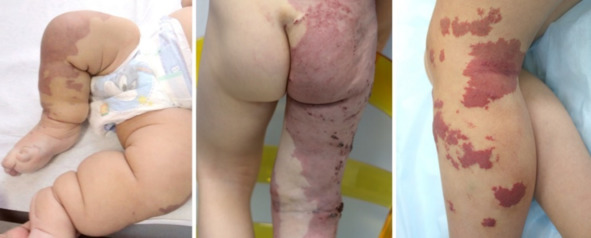
Пациенты с комбинированной формой сосудистых мальформаций.
ДИАГНОСТИКА
На ранних этапах беременности еще внутриутробно возможно диагностировать лимфатическую мальформацию. Ультразвуковое исследование плода и МРТ являются высокоинформативными методами визуализации с целью пренатальной диагностики и анатомической оценки данной патологии. Большинство лимфатических мальформаций среднего и крупного размера можно диагностировать в первом триместре беременности, и почти все они могут быть диагностированы при ультразвуковом исследовании во втором триместре.
Лимфатические мальформации в области шеи следует отличать от повышенной прозрачности затылка (затылочная прозрачность) при скрининговом УЗ исследовании, которая представляет собой частую задержку лимфатической резорбции при синдроме Дауна (трисомии 21) и некоторых заболеваниях сердца.
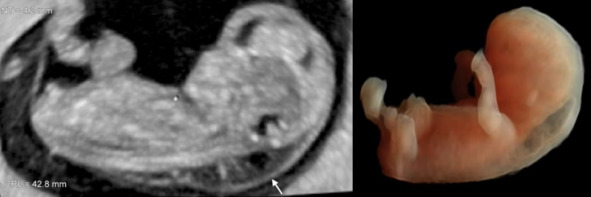
Скрининговое УЗИ плода с повышенной прозрачностью затылочной области, дифференцируется между возможным синдромом Дауна и лимфатической мальформацией. В-режим и 3D УЗИ
Данный признак не указывает на дальнейшее развитие лимфатической мальформации. Пренатальная МРТ диагностика направлена на определение характера поражения (локализация, макро- или микрокисты7, смешанный тип лимфатической мальформации). Но, несмотря на очень хорошую визуализацию при МРТ плода, особенно в режиме Т2, точная оценка наличия и распространения микрокистозной лимфатической мальформации, особенно в области ЛОР органов или на конечностях, затруднена.
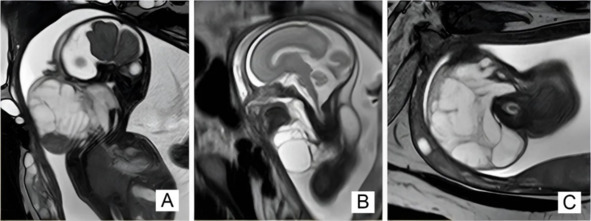
МРТ диагностика плода с лимфатической мальформацией. А. в области шеи, B. в поднижнечелюстной области, С. в области шеи при сагиттальном сканировании. Изображения из статьи https://doi.org/10.2147/IJWH.S430858
Поверхностные или объемные лимфатические мальформации чаще всего видны уже сразу после рождения. Однако они могут проявляться и позже, часто в течение первых 2 лет жизни, иногда они манифестируют после вирусной инфекции или кровоизлияния в результате травмы.
Макрокистозные лимфатические мальформации проявляются в виде подкожных, круглых или дольчатых, безболезненных образований, обычно от нескольких сантиметров в диаметре, с нормальным цветом кожи над ними и мягкой, поддающейся вдавливанию консистенцией тканей.
Микрокистозные лимфатические мальформации могут проявляться в виде аналогичных подкожных образований, немного более плотных, и тогда их можно отличить от макрокистозных лимфатических мальформаций при пальпации. Микрокисты также могут быть поверхностными, эпидермальными и слизистыми, в виде полупрозрачных или геморрагических пузырьков, рассеянных или сгруппированных в бляшки, называемых лимфангиоэктазиями. Они могут отсутствовать при рождении и проявляться постепенно, как в детском возрасте, так и во взрослом периоде.
Во всех случаях лимфатические мальформации требуют клинического обследования, УЗИ и МРТ диагностики. В зависимости от локализации и особенно при расположении в области верхних дыхательных путей, а также при определенных шейно-лицевых формах, необходимо обязательное расширенное обследование.
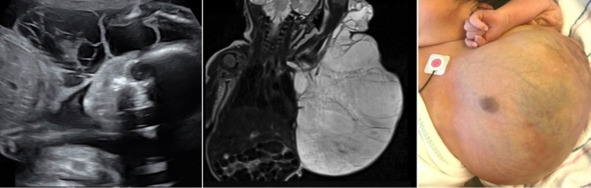
Пренатальное УЗИ (слева); антенатальное МРТ (в центре); внешний вид пациента с лимфатической мальформацией (справа). Клинический случай из статьи https://doi.org/10.1016/j.crwh.2021.e00319
Лимфатические мальформации могут осложняться воспалительными и инфекционными эпизодами, внутрикистозными кровоизлияниями, которые могут быть опасны для жизни в случае сдавливания дыхательных путей при шейно-лицевой локализации. Нередко лимфатические мальформации становятся причиной боли, геморрагических выделений, возникновения серьезных деформаций, а также функциональных нарушений (например, при локализации в области орбиты, вплоть до нарушения зрения).
Ультразвуковое исследование является методом визуализации для первоначальной оценки лимфатических мальформаций, особенно в случаях небольших поверхностных поражений.

Диагностика лимфатической мальформации. Внешний вид пациента (слева), термография (в центре), 3D МРТ (справа).
МРТ является основным методом для определения анатомического расположения лимфатической мальформации. Обследование обязательно должно проводится с использованием режимов Т2 в двух пространственных плоскостях, а также режима T1 для выявления геморрагических изменений и визуализации инфильтрации в жировых структурах. Также рекомендуется проводить МРТ в STIR8 режиме, что позволяет более информативно оценить объем патологических изменений.
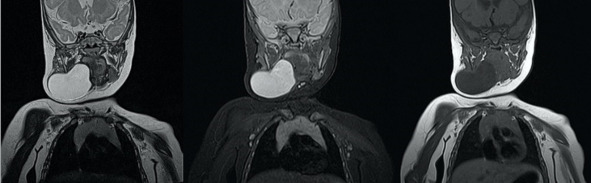
МРТ пациента с лимфатической мальформацией в поднижнечелюстной области. Слева на изображении режим Т2, в центре STIR, справа Т1
Артериография, венография, лимфография и изотопная лимфосцинтиграфия не являются дополнением к стандартному МРТ и не имеют ключевого значения в диагностике. Компьютерная томография выполняется для уточнения возможной инвазии и деформации костных структур, вызванных микрокистами.
Биопсия редко бывает необходима при постановке диагноза лимфатическая мальформация.
С целью иммуногистохимической диагностики лимфатической мальформации оцениваются маркеры: подопланин, CD34, LYVE-1 и VEGFR-3.
Также возможен поиск мутаций гена PIK3CA, особенно если мальформация связана со сложным сосудистым синдромом.
Дифференциальная диагностика
Дифференциальная диагностика в основном заключается в исключении врожденных кист (кисты щитовидно-язычных протоков, кисты вилочковой железы, брахиогенные кисты, бронхогенные кисты и дупликации пищеварительного тракта); пороков развития поверхностных вен; глубоких младенческих гемангиом; а также других пороков развития или опухолей (главным образом тератом). Микрокистозные формы лимфатической мальформации можно спутать с ангиокератомами, пиогенными гранулемами (ботриомикомами), контагиозным моллюском или кондиломами, если они находятся в области гениталий или в перианальной области.
Развитие лимфатической мальформации
Довольно часто лимфатические мальформации характеризуется бессимптомными периодами, иногда продолжающимися несколько лет, иногда перемежающиеся эпизодами болезненных воспалительных вспышек, суперинфекций или внутрикистозных кровоизлияний различной частоты. Не у всех пациентов наблюдаются осложнения или обострения, а у некоторых наблюдается стабильная форма лимфатической мальформации в течение очень длительных периодов жизни.
При возникновении воспалительного процесса лимфатические мальформации довольно резко увеличиваются в размере и становятся болезненными. Обычно воспалительные изменения длятся от нескольких суток до 1 месяца, в среднем около 10 дней и причиной являются, как правило, вирусные заболевания. Увеличение и болезненность может также возникнуть при травматизации лимфатических мальформаций с последующим подкравливанием в лимфатическую полость.
Считается, что половое созревание является пусковым фактором прогрессирования лимфатических мальформаций, но четких корреляций с половым созреванием в проведенных исследованиях нет.
Достоверно установлено, что спонтанная регрессия лимфатических мальформаций не происходит у пациентов с микрокистозными формами. При макрокистозных и смешанных формах лимфатических мальформаций спонтанная регрессия возникала в течение 3 месяцев после первоначального появления, и это могло быть связано с изменениями характера лимфотока. Спонтанной регрессии наиболее часто подвержены дорсальные лимфатические мальформации. Четкой статистики по данному вопросу нет, ввиду оценки малых групп пациентов с лимфатическими мальформациями за непродолжительный временной промежуток.
Лимфатическая мальформация кожи
Микрокистозные лимфатические мальформации могут проявляться в виде полупрозрачных или геморрагических пузырьков малых размеров (до 1—2мм), рассеянных или сгруппированных в бляшки на поверхности кожи, называемых лимфангиоэктазиями. Они могут быть покрыты бородавчатым гиперкератозом и осложняться выделением лимфы, а также осложняться хроническим кровотечением. Со временем лимфатическая мальформация кожи прогрессирует, увеличивается количество пузырьков, происходит утолщение тканей, характеризующееся усилением выделения лимфы (пропотеванию в области мальформации) и кровоточивости из лимфатических пузырьков. В некоторых случаях возможно присоединение бактериальных инфекций, особенно если лимфангиоэктазии находятся на слизистой полости рта и половых органах.
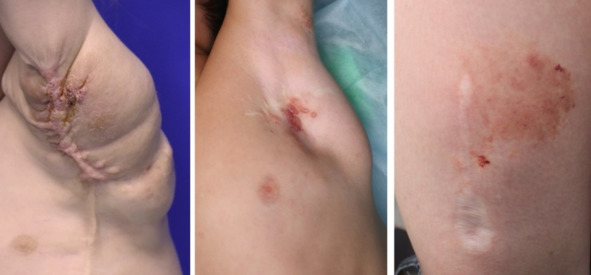
Пациенты после хирургического лечения лимфатической мальформации, в послеоперационном периоде отмечается развитие лимфатической мальформации кожи в области рубцов.
ЛЕЧЕНИЕ ЛИМФАТИЧЕСКИХ МАЛЬФОРМАЦИЙ
Некоторые лимфатические мальформации практически не проявляют себя и являются случайной диагностической находкой, в этом случае наиболее подходящим методом «терапии» является отсутствие лечения с последующим наблюдением.
Целью лечения лимфатических мальформаций является подчас не избавление от сосудистого порока полностью, а поддержание функциональности, контроль сопутствующих симптомов, сохранение эстетической целостности и качества жизни, а также предотвращение развития осложнений.
Интервенционная радиология (склеротерапия). Склеротерапия является основным методом лечения для большинства лимфатических мальформаций. Операция обычно проводится под общей анестезией, хотя в некоторых случаях, в зависимости от выбора склерозирующего вещества, возможно проведение склеротерапии и под местной анестезией.
Склерозирование лимфатических мальформаций более эффективно при макрокистозных формах порока. Проведение склеротерапии требует обязательной ультразвуковой навигации. Это позволяет не только точно пунктировать патологические полости и исключить травматизацию близлежащих артерий и вен, но и четко контролировать процесс аспирации содержимого полостей, что обеспечивает контролируемое введения препарата в патологическое пространство.
Препараты, применяемые в качестве склерозирующего вещества, оказывают повреждающее действие на эндотелий сосудов с последующим развитием асептического воспаления, что приводит к фиброзу и облитерации лимфатических сосудов. Препараты вводятся после аспирации кистозного содержимого в объеме от 30% до 50% от общего объёма аспирированного содержимого лимфатической мальформации. Вызванная введением препарата воспалительная реакция со стороны тканей может быть болезненной и даже опасной (для глаз и дыхательных путей). Эффективность проведенного лечения оценивается по меньшей мере через 1—1,5 месяца, как правило, склерозирование требует несколько сеансов.
Для склерозирования используются несколько препаратов: тетрадецилсульфат натрия (фибро-вейн), ОК-432 (пицибанил), полидоканол или лауромакрогол 400 (3% Этоксисклерол®), абсолютный этанол (99% этаноловый спирт), доксициклин и блеомицин. Каждый склерозант имеет свои преимущества и недостатки, и их применение также связано с опытом клинического центра и специалистов.
Например, абсолютный этанол является сильнодействующим средством, вызывающим жизнеугрожающие состояния. Блеомицин, при несоблюдении дозы введения, также имеет серьезные побочные эффекты. Однако, вызывая слабую воспалительную реакцию, он эффективен при склерозировании лимфатических мальформаций, расположенных в сложных анатомических областях.
На базе нашего медицинского центра разработан и запатентован метод склерозирование лимфатических мальформаций с использованием препарата Гемоблок (Патент №2804229 и Патент 2797741). Данный препарат обладает хорошими «склерозирующими свойствами» и полным отсутствием токсичности. Благодаря данной методике, мы смогли минимизировать риски осложнений при проведении склерозирования лимфатических мальформаций.
Побочные эффекты от склерозирующих средств включают: отек, боль, изъязвления кожи и поражение близлежащих нервов. Риск серьезных осложнений (повреждение нервов, некроз кожи, сердечно-легочные нарушения) составляет порядка 0—3% в зависимости от выбора препарата.
Склеротерапия является методом выбора в лечении лимфатических мальформаций, лечение носит этапный характер, с интервалом не менее 3—6 месяцев.
Хирургия. В большинстве случаев полное хирургическое удаление лимфатической мальформации затруднено или даже невозможно из-за инфильтрирующих поражений, которые трудно идентифицировать и иссечь во время операции. Поэтому хирургическое вмешательство, как правило, является частичным или приостанавливающим развитие при обширных процессах методом лечения, и редко является методом выбора. Возможно применение хирургического лечения при ограниченных макрокистозных лимфатических мальформациях.
Электрокоагуляция, лазерное лечение, радиочастотная терапия эффективны для поверхностного удаления лимфатических мальформаций, остановки кровотечения и уменьшения покраснения кожи. Данное лечение всегда требует повторных манипуляций и носит только временный характер. Микрокистозные лимфатические мальформации в области языка являются классическим показанием для данного лечения. При кожных лимфангиоэктазиях лечение CO2-лазером безопасно и дает хороший временный эффект. Побочные эффекты обычно незначительны, встречаются нечасто и заключаются в развитии депигментации кожи в области воздействия и развития плоских рубцов небольших размеров.
Физиотерапия. Применение компрессии и лимфодренажа при лифматических мальформациях малоэффективно. Например, ручной лимфодренаж не особо эффективен при лимфатической мальформации, но хорошая переносимость его пациентами и хорошее самочувствие после него может улучшить качество жизни пациента.
Медикаментозное лечение. Сиролимус (или рапамицин) ингибирует лимфангиогенез, вмешиваясь в сигнальный путь PI3K/AKT/mTOR. Данная терапия успешно используется в сложных случаях уже 10 лет. Многие исследования подтвердили его эффективность. Медикаментозное лечение частично уменьшает объем лимфатической мальформации. Продолжительность лечения часто бывает длительной (более 6 месяцев), и нет никаких критериев принятия решения о его прекращении, кроме побочных эффектов, которые требуют отмены данной терапии. Всем пациентам, получающим терапию, необходим регулярный клинический и биологический мониторинг (примерно через 1 месяц после начала лечения, затем каждые 2—3 месяца). Для коррекции дозировки следует измерять концентрацию сиролимуса в крови (необходимая концентрация 4—12 нг/мл), данный мониторинг позволяет поддерживать эффективность терапии и избегать развития осложнений.
Силденафил (Виагра) является мощным и селективным ингибитором фосфодиэстеразы 5-го типа. Несколько небольших исследований показали эффективность данной терапии, но без дальнейшего подтверждения и развития клинических рекомендаций. Поэтому силденафил не показан в варианте широкого применения, за исключением специфических ситуаций.
Бевацизумаб – это моноклональное антитело, активное против VEGF-A, оказывающее влияние на лимфангиогенез. Бевацизумаб был предметом нескольких клинических случаев системного применения и в качестве склерозирующего средства. В настоящее время нет достаточных доказательств его эффективности в лечении лимфатических мальформаций.
Алпелизиб – это таргетная терапия, которая непосредственно ингибирует PIK3. Соматические активирующие мутации гена PIK3CA были идентифицированы в лимфатических мальформациях, особенно при синдромах с гипертрофией мягких тканей (таких как CLOVES синдром, синдром Клиппеля-Треноне). Пилотное исследование сообщило о многообещающих результатах, и эта терапия проходит клиническую оценку (профиль эффективности и безопасности) при синдромных формах лимфатических мальформаций.
Терапевтическое лечение лимфатических мальформаций должно проводиться исключительно специалистами из медицинских центров, специализирующихся на данной патологии.
Синдромные лимфатические мальформации. В случае, когда лимфатические мальформации являются частью сложного синдрома (Синдром Протея, CVOVES синдром, синдром Клиппеля-Треноне), лечение всегда является комплексным и сочетает хирургическое вмешательство, склеротерапию и антикоагулянтную терапию при венозных аномалиях, осложненных тромбозом. Назначение препарата сиролимус является таргетной терапией при данных состояниях.

