
Полная версия
Роль кислотно-пептического фактора в развитии кислотозависимых заболеваний организма
На освобождение эндогенного гистамина могут указывать и следующие симптомы:
1) ощущение покалывания в верхней половине груди;
2) зуд, который вначале ограничен областью лица и шеи, а с увеличением концентрации гистамина распространяется на грудь и живот, затем – на всё тело;
3) крапивница;
4) расширение сосудов;
5) падение артериального давления;
6) головная боль;
7) замедление дыхания;
8) нарушение со стороны желудочно-кишечного тракта.
Механизмы, инактивирующие биологическую активность гистамина:
1) окислительное дезаминирование с образованием имидазолуксусной кислоты и рибозида имидазолуксусной кислоты;
2) метилирование азота имидазольного кольца гистамина с образованием метилимидазолуксусной кислоты;
3) ацетилирование аминогруппы с образованием ацетилгистамина.
В основном инактивация гистамина в организме осуществляется посредством окислительного дезаминирования с помощью фермента гистаминазы (диаминоксидазы). Гистаминаза была названа также диаминоксидазой, так как она инактивирует и другие диамины (путресцин, кадаверин). Способность диаминоксидазы кишечной стенки разрушать гистамин, кадаверин и путресцин имеет большое практическое значение в защите организма от отравления этими веществами, которые образуются в кишечнике в результате жизнедеятельности бактерий. Кора надпочечников, печень, слизистая оболочка кишечника имеют наибольшую концентрацию гистаминазы, которая активна только в присутствии кислорода.
Повышенный уровень свободного гистамина в организме зависит от двух основных факторов: от поступления гистамина в организм человека (как эндогенного, так и экзогенного) и пониженной выработки гистаминазы. Инактивирующее действие на гистамин, кроме гистаминазы, оказывает ещё и группа противогистаминных препаратов. Уменьшение процесса кислотообразования после введения противогистаминных препаратов объясняется не только прямым действием их на секрецию, но и их действием на нервную систему (уменьшается возбудимость всей системы, в частности, блуждающего нерва).
Следовательно, гистамин не может проявлять полностью своего действия в следующих случаях:
1) при инактивирующем действии гистаминазы;
2) при инактивирующем действии противогистаминных препаратов;
3) при блокирующем влиянии ряда веществ на метаболизм тех клеток, которые подвергаются действию гистамина.
К последней группе следует отнести все наркотические и анестезирующие вещества, применение которых прекращает желудочную секрецию, вызванную введением гистамина. Установлено, что у собак во время углубления наркоза прекращается образование соляной кислоты в желудке.
Париетальная клетка содержит рецепторы для трех соединений, вызывающих активацию секреции кислоты. Это М3 – мускариновые рецепторы для ацетилхолина. Н2 рецепторы для гистамина и ССК-В рецепторы для гастрина, представляющий собой подтип В рецепторов для холецистокинина.
Гормоны и другие биологические активные вещества, которые не проникают внутрь клетки, оказывают свое действие на клетку, связываясь с рецепторами клеточной поверхности, что в свою очередь обеспечивает продукцию вторичных мессенджеров. Эти небольшие молекулы, распространяясь в клетке путем диффузии, передают сигнал от рецептора к внутриклеточным белкам, что приводит к активации клеточной функции, т.е. сокращение или секреция. В настоящее время к числу вторичных мессенджеров относят около десятка соединений.
Заключение.
Регуляция секреции соляной кислоты желудком осуществляется с участием как центральной, так и периферической нервной системы. Периферическая регуляция обеспечивается с использованием нейрональных, эндокринных и паракринных путей. Ацетилхолин, секретируемый нервными терминалами, взаимодействует с М3-рецепторами париетальных клеток и М1-рецепторами ECL-клеток. Эти клетки, расположенные под эпителием желудка поблизости от париетальных клеток, секретируют гистамин, взаимодействующий с Н2 рецепторами париетальных клеток. Ацетилхолин стимулирует также G-клетки, секретирующие гастрин, который в свою очередь активирует париетальные и ECL-клетки.
Ацетилхолин, освобождаемый из нервных терминалей, связывается также с D-клетками антрального отдела слизистой оболочки желудка. Это приводит к ингибированию секреции D-клетками соматостатина, который в свою очередь является ингибитором секреции гастрина G-клетками, что усиливает секрецию соляной кислоты. Обратная связь между внутриклеточным значением рН и активацией париетальных клеток поддерживается за счет подавления освобождения гастрина при снижении рН ниже 3,0. Эти сложные взаимоотношения между различными гормонами и паракринными агентами обеспечивают тонкую регуляцию секреции соляной кислоты.
В конечном итоге активация секреции кислоты париетальной клеткой вызывается взаимодействием с ней трех биологически активных соединений: ацетилхолина, гастрина и гистамина.
2. Фазы желудочной секреции
Существуют 4 фазы желудочной секреции:
– базальная;
– цефалическая (мозговая, нейро-рефлекторная);
– желудочная (нейро-гуморальная);
– кишечная.
Установлено, что во время приёма пищи желудочная секреция осуществляется в трёх фазах: психической, химической и кишечной.
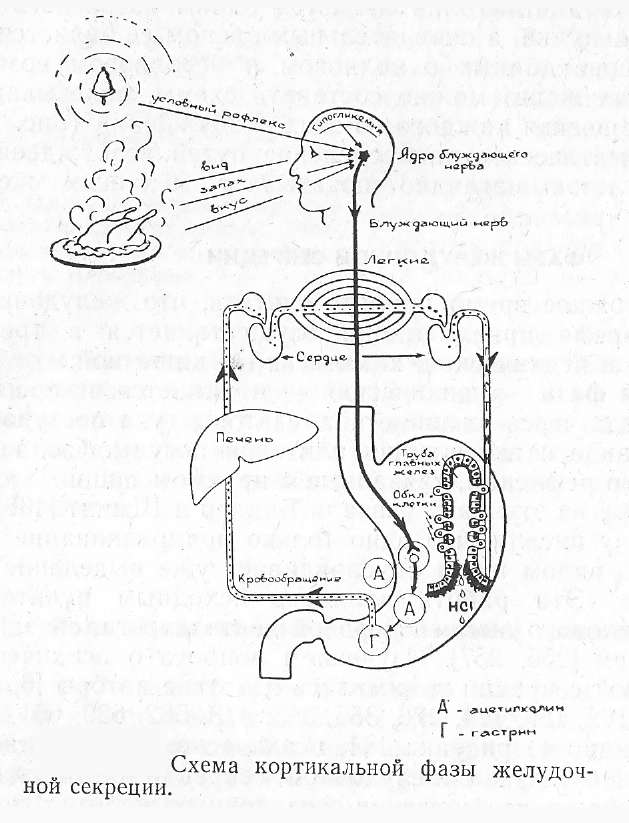
Первая фаза желудочной секреции – психическая. Она берёт начало в коре головного мозга, когда от внешних раздражителей через анализаторы туда поступает информация о представлении, виде и вкусе пищи. Сюда можно отнести и условные рефлексы, связанные с приёмом пищи. На рисунке показана психическая, или кортикальная, фаза желудочной секреции.
Она осуществляется по виду волнового возбуждения желудочных желез. Такой вид возбуждения, как показано на рисунке, состоит из двух компонентов: нервного (внешний раздражитель – анализатор – гастринвырабатывающие клетки) и гуморального (гастрин-обкладочные клетки).

Вторая фаза желудочной секреции – рефлекторно-химическая (или гуморальная, или гастрическая). Вторая фаза желудочной секреции обусловлена действием пищи на чувствительные окончания центростремительных нервов желудка, поэтому И.П. Павлов предложил эту фазу назвать нервно-химической.
На этапах изучения и становления вопроса о фазах желудочной секреции было установлено, что вторая фаза желудочной секреции осуществляется при действии нервной системы и гормона привратника. В связи с чем предлагалось вторую фазу назвать антральной, т.к. для этой фазы характерно выделение антрального гормона. Ряд авторов полагали, что механизм второй фазы желудочной секреции определяется действием не только гастрина, но и пищей и продуктами её распада, которые, всасываясь, попадают в круг кровообращения. Тем самым могут непосредственно возбуждать секреторную деятельность желудочных желез. Однако не было четкого указания на то, происходит ли всасывание элементов продуктов распада пищи из желудка или же из кишечника. Следует полагать, что если всасывание происходит из кишечника, то это уже относится к третьей фазе желудочной секреции. Впоследствии ряд авторов четко разделили вторую фазу на пилорическую (с образованием гастрина) и кишечную. В связи с тем, что нет четких и достоверных данных, что питательные вещества из потребленной пищи всасываются именно из желудка, ряд авторов предлагает называть вторую фазу гастрической. Принимается во внимание также место, откуда возникает информация, поступающая к обкладочным клеткам во время этой фазы.
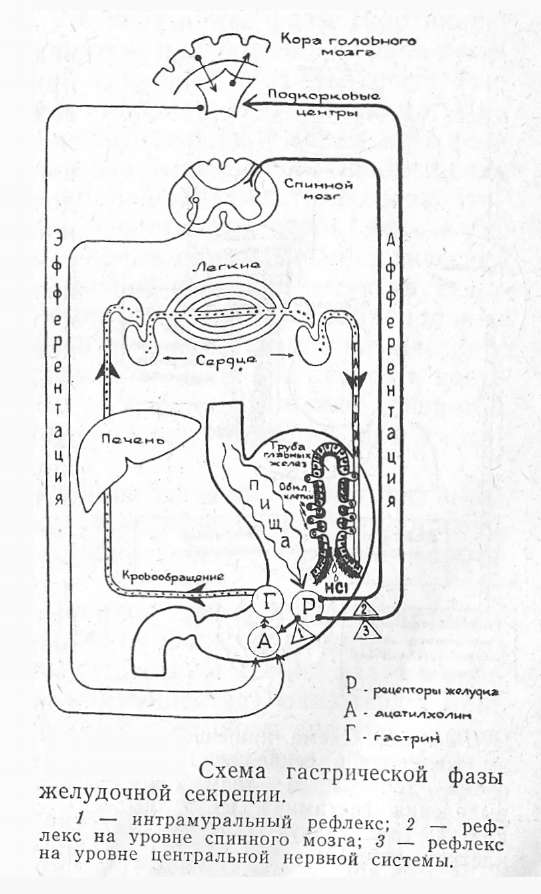
Изложенные позиции свидетельствуют о том, что вторая фаза осуществляется при помощи двух составляющих: нервного (рефлекса от рецепторов желудка к
гастринвырабатывающим клеткам) и гуморального
(гастрин-обкладочные клетки). Схема гастрической фазы желудочной секреции показана на рис.
Третья фаза желудочной секреции – кишечная фаза. Кишечная фаза желудочной секреции также была установлена в лаборатории И.П.Павлова, сотрудники которой на основании ряда опытов пришли к заключению, что введение некоторых раздражителей: либиховского экстракта, пептона, воды и др. в тонкий кишечник возбуждает секреторную деятельность желудка. Однако они также наблюдали и противоположный эффект. Ряд веществ (15%-ный раствор поваренной соли, желудочный сок, соляная кислота), введенные в тонкий кишечник, подавляют секреторную деятельность желудка. Ряд авторов также установили, что введение раздражителей в тонкий кишечник в большинстве случаев вызывает повышение секреторной деятельности желудка, а в некоторых случаях этот раздражитель не только не влияет стимулирующе на деятельность желудка, но даже подавляет её.
Установлено, что секреция желудка в кишечной фазе происходит благодяря всасыванию химических веществ пищи. Допускается, что кишечная фаза желудочной секреции может осуществляться благодаря образованию специального «кишечного» гастрина.
Вышеизложенное свидетельствует о неволновой природе возбуждения обкладочных клеток во время кишечной фазы. Это подтверждается также рядом исследований, свидетельствующих о том, что раздражение рецепторов тонкой кишки не вызывает секреции желудочных желез.
Желудочную секрецию во время кишечной фазы, учитывая вышеизложенное, можно представить такой, как это показано на рисунке.
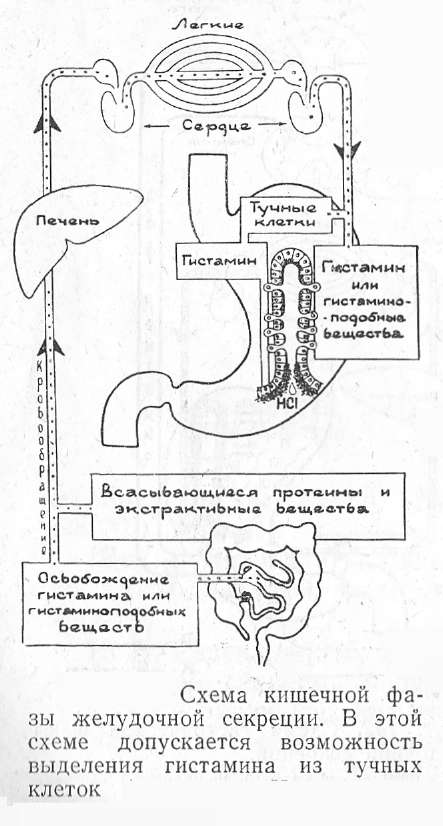
Допускается возможность того, что возбуждение обкладочных клеток в третьей фазе желудочной секреции может осуществляться посредством тучных клеток, которые, подвергаясь влиянию экстрактивных или других веществ, освобождают гистамин. Можно также предположить, что тучные клетки являются звеньями, при помощи которых гипоталамус, гипофиз и адреналовая система оказывают влияние на кишечную фазу желудочной секреции.
Отдавая дань истории развитяи этого вопроса, целесообразно привести таблицу Рота и Бокуса, в которой показан механизм желудочной секреции в каждой фазе отдельно таб.
Если сранивать эту таблицу со схемами отдельных фаз желудочной секреции (рис. 37-40), то мы можем заметить различие в интерпретации механизмов кортикальной фазы.
Исходя из данных таблицы, во время кортикальной фазы блуждающий нерв вызывает местное освобождение ацетилхолина, но дальше нет пояснений, на какие именно элементы атетилхолин действует во время образования соляной кислоты. Ряд авторов приводят данные литературы, указывающие на то, что действие ацетилхолина не распространяется прямо на обкладочные клетки и что раздражение блуждающего нерва во всех случаях вызывает образование гастрина, который и является возбудителем обкладочных клеток.
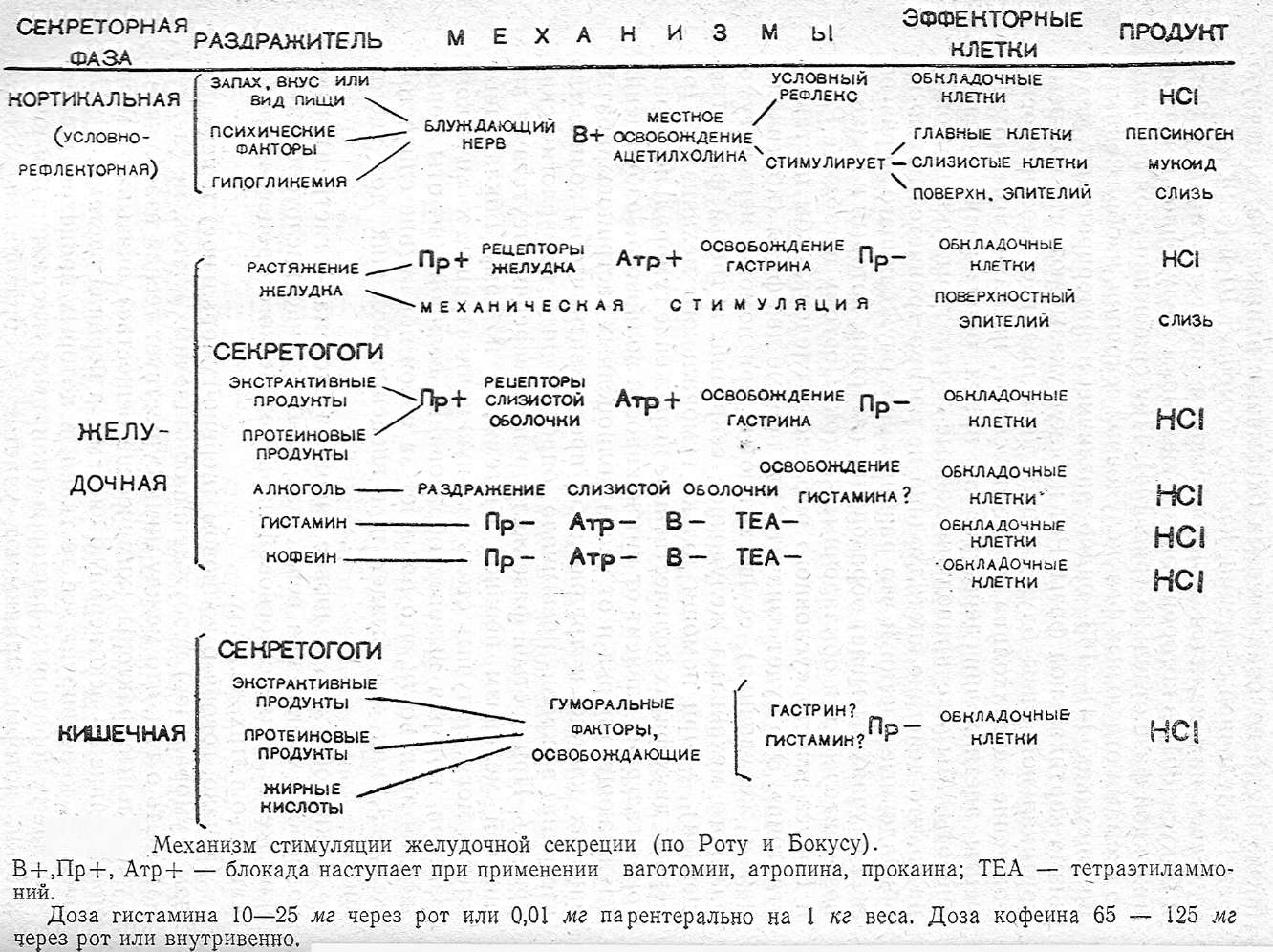
Таблица.
Е.Ю. Линар предлагает в таблице Рота и Бокуса вместо «условного рефлекса» поставить «гастрин». Это бы означало, что первые две фазы (кортикальная и желудочная) осуществляются при помощи нервно-гуморального механизма желудочной секреции, а третья фаза (кишечная) – при помощи только гуморального механизма. При первых двух фазах количественное выражение гуморального фактора (гастрин) зависит как от интенсивности волнового возбуждения блуждающего нерва, так и от полноценных гастринвырабатывающих клеток. При таком рассуждении трудно себе представить, чтобы количество гастрина в крови превышало определенный физиологичекий уровень.
В третьей фазе желудочной секреции защитный механизм нервной системы отсутствует, и обкладочные клетки могут получить столь сильную концентрацию химического фактора, которая вызовет образование соляной кислоты повышенной активности, что может повлечь за собой поражение слизистой желудка, как при введении больших доз гистамина.
Между волновым (нервно-гуморальным) и неволновым (гуморальным) возбуждением обкладочных клеток существует тесная взаимосвязь.
Гуморальные факторы оказывают мощное влияние на всю нервную систему, а она, в свою очередь, иннервирует все ткани, в которых происходит образование гуморальных факторов (к примеру, гистамина), и все те клетки, которые принимают участие в образовании соляной кислоты. Необходимо ещё отметить, что волновое (нервная система – гастрин) и неволновое (гуморальное) возбуждение кислотообразующих желез является основой парабиотического процесса, протекающего в этих железах.
3. Роль кислотно-пептического фактора в патогенезе развития язвенной болезни желудка и 12-типерстной кишки
Проблема кислотозависимых заболеваний органов пищеварения остается на сегодняшний день одной из серьезных проблем не только в гастроэнтерологии, но и для клинической медицины в целом.
Объективные предпосылки:
Язвенная болезнь, гастроэзофагальная рефлюксная болезнь, хронический гастрит, гастродуоденит относятся к патологии человека, имеющей традиционно широкое распротсранение, и имеют тенденцию к росту;
Гастроэзофагальная рефлюксная болезнь является в настоящее время одним из наиболее распространенных гастроэнтерологических заболеваний.
Было показано, что изжогу (основной клинический симптом ГЭРБ) испытывают ежедневно 7% всего населения, хотя бы 1 раз в неделю – 14%, хотя бы 1 раз в месяц – 40%. За последние 20 лет относительная частота обнаружения язв желудка и двернадцатиперстной кишки при эндоскопических исследованиях уменьшалась соответственно с 15,9% до 4,6% и с 39,1% до 9,3%, а частота выявления эрозивной формы ГЭРБ, напротив, возраслас 3,1% до 16% (Assimakopoulos S. et all., 2007).
3. На современном этапе происходит расширение спектра кислотозависимых заболеваний органов пищеварения и переосмысление роли кислотно-пептического фактора в патогенезе развития указанной группы заболеваний. Одним из очевидных достижений последних лет является формирование научно обоснованной точки зрения, согласно которой хронический панкреатит также относится к числу заболеваний, отчётливо зависящих от уровня кислотной продукции желудка;
4. Вызывает озабоченность стойко высокий уровень деструктивных и неопластических осложнений кислотно-зависимых заболеваний органов пищеварения;
5. Проблема кислотозависимых заболеваний органов пищеварения включает не только клиническую, но и социально-экономическую составляющую, связанную с необходимостью колоссальных затрат государственного бюджета, обусловленных лечением больных в стационарах и в условиях амбулаторно-поликлинических учреждений;
6. Дебют кислотозависимых заболеваний в основном приходится на лиц молодого и среднего, наиболее трудоспособного и социально-активного, возраста.
Следовательно, совершенствование научных и методических подходов к дальнейшему изучению патогенеза кислотно-зависимых заболеваний органов пищеварения и разработка адекватной тактики их лечения является важной медико-социальной проблемой.
Неоспоримым является факт, что кислотно-зависимые заболевания органов пищеварения характеризуются общностью патогенетических механизмов их развития. Дополняя известный тезис, что «без кислоты нет язвы», с современной точки зрения с уверенностью можно утверждать, что без участия кислотно-пептического фактора нет хронического гастрита, гастродуоденита, гастроэзофагальной рефлюксной болезни, хронического панкреатита и других дисфункций желудочно-кишечного тракта.
Язвенная болезнь – хроническое заболевание, основным морфологическим проявлением которого служит рецидивирующая язва желудка или двенадцатиперстной кишки, как правило, возникающая на фоне гастрита, вызванного инфекцией Helicobacter pylori.
Язвенная болезнь относится к наиболее распространенным заболеваниям пищеварительной системы, в странах Европы ею страдают от 5 до 20% населения.
В развитии этого заболевания весомую роль играют наследственность, а также социально-экономические и демографические факторы.
Эпидемиологические исследования свидетельствуют о том, что язвенная болезнь выявляется преимущественно у городских жителей развитых стран, имеющий низкий социальный статус. Заболевание преобладает у мужчин, причём язва двенадцатиперстной кишки чаще развивается в более молодом возрасте (после 30 лет), а язва желудка – чаще после 40 лет.
Основные этиологические факторы
Несмотря на более чем 170-летний период интенсивного изучения язвенной болезни, до сих пор нет полной ясности о природе заболевания. В связи с тем, что язвы слизистой желудка и двенадцатиперстной кишки сочетаются с изменением самой слизистой (гастрит, гастродуоденит) и с изменением нервной системы и других органов, данное заболевание принято называть «язвенная болезнь». Этим самым акцентируется, что язвенный дефект является лишь частным проявлением общего заболевания.
Дискуссии продолжаются до сих пор о том, одно или два заболевания представляет язва двенадцатиперстной кишки и язва желудка.
Сторонники дуалистической теории считают язвенную болезнь желудка и язву двенадцатиперстной кишки различными заболеваниями с различным патогенезом и клинической картиной.
Аргументы в пользу дуалистической теории:
Язвенной болезнью двенадцатиперстной кишки чаще болеют, в основном, молодые люди с высокой кислотообразующей функцией желудка;
– язва двенадцатиперстной кишки не обладает способностью малигнизироваться;
– язва двенадцатиперстной кишки характеризуется сезонностью обострений, повышенной эвакуаторной деятельностью желудка, поздними голодными и ночными болями, реже возникает рвота, чаще наблюдаются осложнения в виде кровотечения и пенетрации, слизистая тела желудка чаще всего остаётся интактной;
– язвой желудка чаще болеют люди старшего возраста с нормальной или сниженной кислотностью желудочного сока;
– язва желудка чаще обладает способностью малигнизироваться;
– при язве желудка эвакуаторная деятельность желудка снижена, реже наблюдается сезонность обострений, а в клинической картине преобладают диспепсические явления.
Аргументы в пользу унитарной теории:
– имеются одинаковые морфологические изменения в слизистой;
– возможность получения язвенного дефекта в желудке и двенадцатиперстной кишке едиными экспериментальными методами, а также сходством в клинической картине заболевания, её течения и положительного терапевтического эффекта от применения одинаковых лекарственных средств;
– язвы могут проявиться одновременно в желудке и двенадцатиперстной кишке, могут мигрировать при очередных рецидивах по малой кривизне из желудка в 12-перстную кишку и обратно.
Вместе с тем, большинство авторов (Богер Н.М., 1986 и др.) считают, что, учитывая тот факт, что между язвенной болезнью желудка и двенадцатиперстной кишки имеется много общего, и это – единое заболевание с различными формами течения в виде язв желудка, двенадцатиперстной кишки или их сочетания.
Между тем дискуссионным также остаётся вопрос о симптоматических язвах слизистой желудка и двенадцатиперстной кишки, возникающих при различных заболеваниях, стрессовых ситуациях и после приёма некоторых лекарств.
Также нет единого мнения, какие язвы считать симптоматическими, а какие отнести к язвенной болезни. К примеру, И.Т.Абасов, О.С.Радбиль язвы, возникающие при легочной недостаточности, относят к симптоматическим, а Гроссман считает эту патологию важным этиологическим фактором язвенной болезни.
Несомненно одно, что при решении данного вопроса следует исходить из единого генеза как симптоматических, так и язв, появляющихся при язвенной болезни. И те, и другие возникают при усилении агрессивных факторов желудочного сока или снижении защитных свойств слизистой.
Исходя из многолетних наблюдений, проведенных во многих регионах мира, можно прийти к выводу, что язвенная болезнь является полиэтиологичным заболеванием.
Ф.И.Комаров и О.С.Радбиль разделяют все этиологические факторы язвенной болезни на три группы: нервные, алиментарные и генетические.
Наряду с этим можно добавить, что в последние годы придаётся большое значение инфекции H. pylori. Инфекция H. pylori признана наиболее частой причиной развития язвенной болезни. Расшифрованы некоторые, обусловленные присутствием бактерии, молекулярные механизмы, ослабляющие репаративную регенерацию желудочного эпителия, в результате чего инфекция H. pylori приводит к замедлению заживления язв желудка и двенадцатиперстной кишки. Оказалось, что H. pylori тесно связан с фактором агрессии при язвенной болезни. H. pylori, возможно, непосредственно, а, возможно, и опосредованно через цитокины моноцитов и лимфоцитов воспалительного инфильтрата приводят к дисгармонии во взаимоотношениях G-клеток, продуцирующих гастрин, и D-клеток, продуцирующих соматостатин и играющих важную роль в регуляции функционирования париетальных клеток. Гипергастринемия вызывает усиленное образование париетальных клеток и повышение продукции соляной кислоты.
Ранее, при проведении первых эпидемиологических исследований, было показано, что инфекция ответственна за возникновение более чем 90% дуоденальных язв и 70-80% язв желудка. После уточнённые результаты широкомасштабных исследований в разных странах мира показали, что на долю язвенной болезни, ассоциированной с инфекцией H. pylori, приходится 56% дуоденальных и 38% язв желудка.
В этих же исследованиях показано, что второй по частоте причиной развития пептических язв, преимущественно с локализацией в желудке, является приём НПВП. Показаны также редкие причины образования гастродуоденальных язв, которые перечислены в таблицах.(Цитировано по Ивашкину В.Т. 2002г.)
Снижение частоты рецидивов язвенной болезни после эрадикации инфекции H.pylori служит главным подтверждением роли инфекции в патогенезе заболевания. У пациентов с язвенной болезнью желудка и двенадцатиперстной кишки после эффективной антигеликобактерной терапии обострения заболевания в течение последующих лет наблюдаются не более чем в 5% случаев в год, в то время как в отсутствие такого лечения, к примеру, при язве двенадцатиперстной кишки, в течение года рецидивы возникают в 50-80 % случаев (Ивашкин В.Т., 2003).
Причины развития язв двенадцатиперстной кишки (Modlin I.,
Sachs G. Acid related diseases//Biol. and Treatment. – 1998)
Основная – Инфекция H. pylori
Редкие H. pylori – отрицательные дуоденальные язвы
1. Синдром Золлингера-Эллисона (гастринома) 10. Гиперкальциемия
2. НПВП
3. Хронические обструктивные заболевания лёгких 11. Инфекция Gastrospirillium
4. Циррозы печени hominis
5. Почечная недостаточность 12. Пенетрация рака поджелудоч-
6. Болезнь Крона ной железы
7. Целиакия 13. Системный мастоцитоз
8. Лимфома 14. Амилоидоз IV тип
9. Заболевания ЦНС (травмы) с поражением задней 15. Пахидермопериостоз
черепной ямки – язвы Кушинга 16. Полицитемия rubra vera
17. ВИЧ-инфекция
Таблица. Причины развития язв желудка (Modlin I.,
Sachs G. Acid related diseases//Biol. and Treatment. – 1998)
Основная
1. Инфекция H. pylori
2. Прием НПВП
Редкие
H. pylori – отрицательные язвы желудка при отсутствии приема НПВП
1. Аденокарцинома 7. Сахарный диабет
2. Карциноид 8. Болезнь Крона
3. Пенетрация опухолей соседних органов 9. Лимфома
4. Саркома 10. Сифилис
5. Лейомиома 11. Туберкулез
6. Инородные тела 12. ВИЧ-инфекция
Патогенез
В связи с отсутствием до настоящего времени единой теории этиологии и патогенеза язвенной болезни, можно говорить о полиэтиологичности и полипатогенетичности данного заболевания. Также можно полагать, что язвенная болезнь тела желудка и язвенная болезнь пилородуоденального отдела отличаются друг от друга по этиологическим и патогенетическим факторам.
Имеются патогенетические особенности при ювенильной и старческой язве, язве у женщин и у мужчин и язвенной болезни, возникающей при различных заболеваниях.
Ранее были предложены различные концепции теорий патогенеза язвенной болезни:
1) язвы желудка и двенадцатиперстной кишки образуются только на фоне гастрита и дуоденита, являющиеся предшественниками данного заболевания. Предложена Крювелье и детально разработана Конечным;
2) механическая теория Г.Ашофа, которая до сих пор имеет своих сторонников;
3) кортико-висцеральная теория Быкова-Курцина также имеет своих сторонников и в настоящее время;
4) сосудистая теория Р.Вирхова, согласно которой язва образуется вследствие тромбообразования сосудов слизистой. Неоднократно подвергалась критике за механичность и локализм. Она не объясняет общих механизмов возникновения язвенной болезни, но в интерпретации местных механизмов имеет важное значение и в настоящее время;
5) пептическая теория разработана в 1882 г. Квинке. Согласно этой теории, язва образуется под влиянием усиленной переваривающей способности желудочного сока в результате повышения кислотно- и пепсинообразующей функции желудка. Предложено называть такие язвы пептическими. Однако этой теорией нельзя объяснить все случаи возникновения язвы, так как последняя может иметь место и при сниженной кислотности, а по некоторым данным – и при ахлоргидрии.









