
Полная версия
Гастродуоденальные язвенные кровотечения. Врачу-хирургу
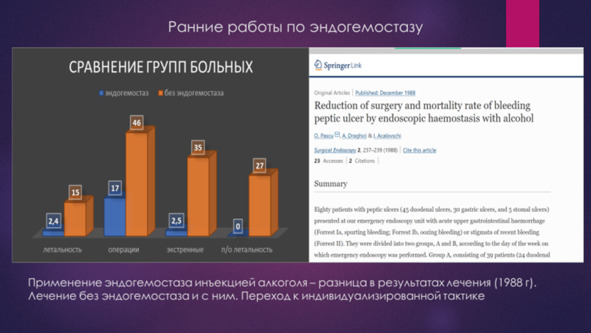
Современный эндогемостаз в комплексе с противоязвенной терапией активно начал противопоставляться хирургическим методам лечения (Seewald S. et al., 2001; Jensen D.M. et al., 2002; Monkemuller K.E., Eloubeidi M.A., 2002; Church N.I. et al., 2003; Bini E.J., Cohen J., 2003; Sung JJ. et al., 2003; Kahi C.J. et al., 2005).
У больных с тяжелой сопутствующей патологией и тяжелой степенью кровопотери неоперативнный гемостаз является единственным шансом на спасение (Еров С. А. и соавт., 2006).
Уже в «Руководстве по неотложной хирургии органов брюшной полости» под редакцией академика В.С.Савельева 2004 г., описывалась тактика относительно категории больных высокого операционного риска: «… мы обязаны обратить внимание еще на одну группу больных, которым неотложная операция любого объема является неприемлемой. Это больные преклонного возраста с предельной степенью операционно-анестезиологического риска, как правило, обусловленного декомпенсацией сопутствующих заболеваний на фоне перенесенной кровопотери. Такие больные, даже при указаниях на высокий риск рецидива кровотечения (а иногда и при продолжающемся кровотечении) вынужденно ведутся консервативно с активными динамическими ЭГДС. Консервативная терапия включает в себя: интенсивную коррекцию кровопотери и вызванных ею синдромных нарушений, введение гемостатических и антифибринолитических средств, ингибиторов протоновой помпы под контролем внутрижелудочного рН, антигеликобактерную терапию. Контрольные эндоскопические исследования проводятся на 1, 2,4 сутки и вплоть до исчезновения риска рецидива кровотечения».
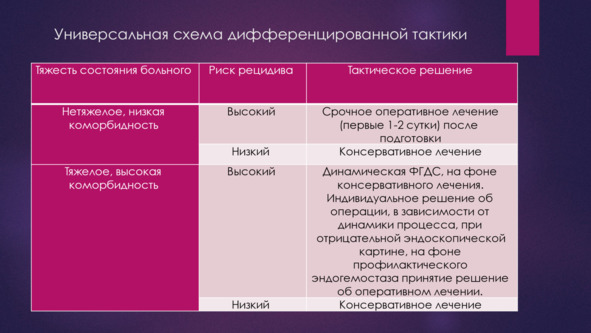
По мнению Вербицкого В. Г., Багненко С. Ф., Курыгина А. А. 2004 г. центральная проблема тактики при ГДЯК дифференцированный подход с учетом риска рецидива и риска операции. Она основана на клинико-эндоскопическом подходе к оценке стабильности гемостаза и степени тяжести пациента.
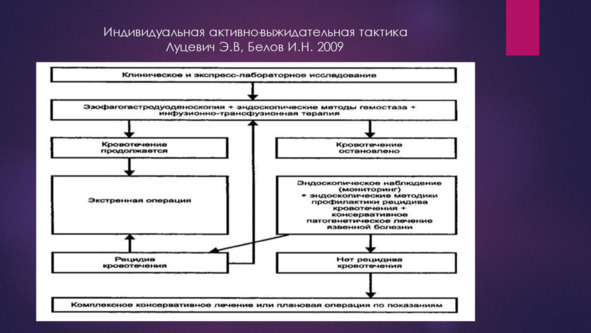

Активная и активно-выжидательная тактика лечения больных пожилого и старческого возраста с язвенными гастродуоденальными кровотечениями приводит к высокой послеоперационной летальности и поэтому не приемлема для данной категории больных (Кубышкин В. А., и соавт., 2013 г; Шугаев А. И. и соавт., 2009). Можно следующим образом охарактеризовать больных с максимальной степенью операционно-анестезиологического риска и наибольшей вероятностью летального исхода после экстренной операции. Это прежде всего пациенты старше 60 лет, имеющие сопутствующую патологию, поступившие в тяжелом состоянии, с нестабильной гемодинамикой, с указанием на перенесенные ранее сердечно-сосудистые коллапсы и тяжелой кровопотерей.


Риск операции увеличивается, если больной ранее был оперирован на желудке или локализация язвы предполагает большой объем операции (язвы задней стенки ДПК). Важно, что эти признаки усугубляют риск операции как при продолжающемся, так и при остановившемся кровотечении. Следовательно, их необходимо учитывать как для выбора объема операции (при продолжающемся кровотечении), так и для решения вопроса о длительности и качестве предоперационной подготовки при угрозе рецидива кровотечения. (Потахин С. Н., Шапкин Ю. Г. 2014).
Таким образом, высокий риск операции, имеющийся у пожилых коморбидных больных, является на ряду с риском рецидива ГДЯК важным фактором летальности, который должен учитываться при выборе тактики лечения. У этой категории больных важно избегать операции, предпочтительным является неоперативный гемостаз, а в случае выполнения операции предпочтительными являются щадящие не радикальные, а условно-радикальные, паллиативные операции. Выработка тактики лечения с учетом риска рецидива ГДЯК и операционного риска легло в основу создания дифференцированной тактики.
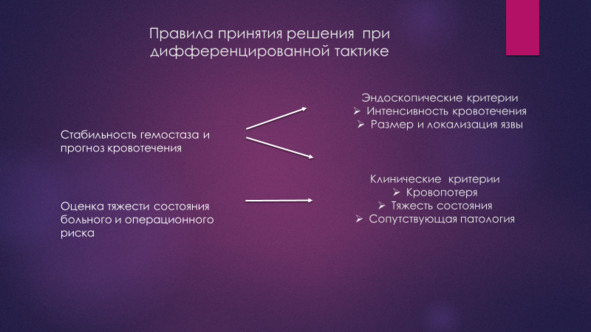

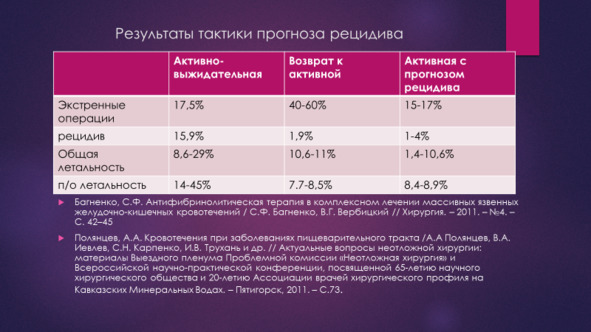


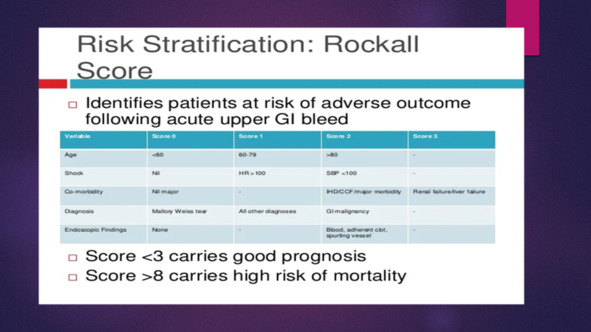
Дифференцированная тактика
Данный тактический подход подробно описан в монографиях Гостищева В. К., Евсеева М. А. Гастродуоденальные кровотечения язвенной этиологии. Руководство для врачей. М.:Гэотар, 2008., Вербицкого В. Г., Багненко С. Ф., Курыгина А. А. Желудочно-кишечные кровотечения язвенной этиологии: патогенез, диагностика, лечение. 2004.
Все больные с остановившимся ГДЯК при этом условно делятся на 4 группы в зависимости от риска операции и риска рецидива. Неоперативный гемостаз в следствии несовершенства его методов не позволял избежать операции у больных высокого операционного риска. Так по данным Гостищева В. К. и Евсеева М. А. (2003) комплексное применение эндоскопического воздействия и медикаментозного подавления желудочной секреции позволило остановить продолжающееся кровотечение (Forrest I) у 96% пациентов, однако окончательная остановка ГДЯК при применении консервативных мероприятий гемостаз удалось добиться лишь у 78,5% пациентов. Таким образом, применение средств консервативного гемостаза, включающих механическую компрессию аррозированного сосуда, формирование коагуляционного струпа или клеевой композиции на поверхности язвы, ингибирование кислотно-пептического фактора, имеет своей основной задачей предотвращение ранних рецидивов кровотечения. То есть гемостаз носит не окончательный, а временный характер. В случае уже сформированных очагов ишемического некроза в периульцерозной зоне и при угрозе позднего рецидива кровотечения консервативный гемостаз является временным. имеет своей целью лишь пролонгирование безрецидивного периода для подготовки больного к неотложной операции.


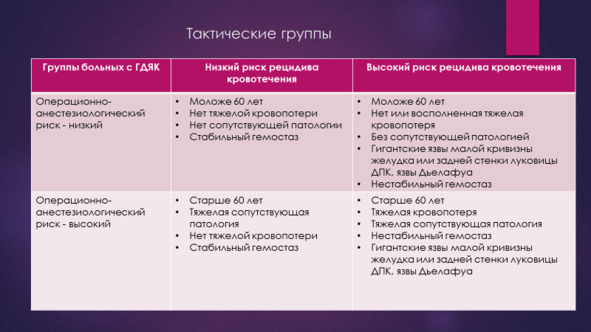
Выделение тактических групп позволяет выделить среди них так называемую «проблемную» группу, группу высокого риска рецидива и высокого операционного риска, дающую до 90% летальных исходов. Именно решение вопросов точного выделения данной группы больных с ГДЯК и эффективного их лечения, в условиях, когда неоперативный гемостаз не позволяет избежать рецидива кровотечения, что делает операцию неизбежной.
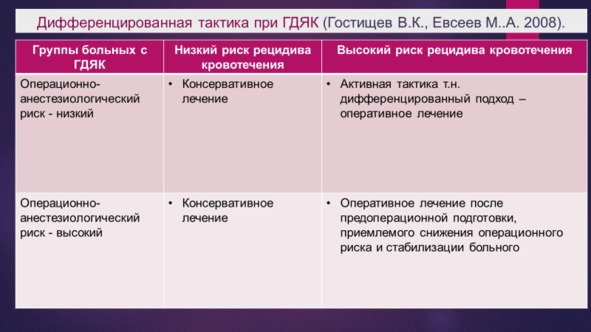
Дифференцированная тактика диктует ряд подходов, которые в этих условиях позволяют эффективно снизить послеоперационную летальность именно в «проблемной группе». Каким образом?
Гостищев В.К, Евсеев М. А. максимально делают подход к оценке риска как операции, так и рецидива, так и готовности больного к операции объективным. Для этого используется шкала APACHE 3. Комбинированный гемостаз в «проблемной» группе используется для пролонгации без рецидивного периода для предоперационной подготовки больного.



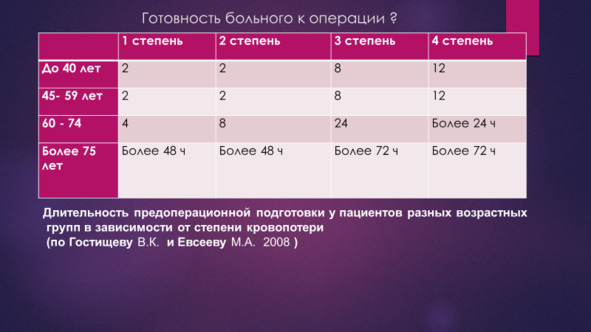
Гостищев В. К., Евсеев М. А. 2008 г. предлагают четкие критерии готовности больного к оперативному лечению, где соответственно возрасту предлагается строго определённое количество баллов шкалы APACHE 3. Эти ученные так же смогли установить временные сроки необходимые для подготовки больных к операции.

Оценка локального гемостаза при гастродуоденальном язвенном кровотечении проводится по классификации J.A. Forrest:
Ia – продолжающееся артериальное кровотечение
lb – продолжающееся венозное или капиллярное кровотечение
IIa – кровотечение остановилось, четко видимый тромбированный сосуд в крае или дне язвы
lIb – кровотечение остановилось, имеется плотно фиксированный сгусток в дне язвы
IIc – кровотечение остановилось, гематин в дне язвы
III – отсутствуют признаки состоявшегося кровотечения, наложения фибрина в дне язвы.
В зависимости от эндоскопической картины диагностическая эзофагогастродуоденоскопия трансформируется в лечебную.
При продолжающемся кровотечении (Forrest Ia, Ib) показано применение комбинированного эндоскопического гемостаза при сочетании следующих методов:
1. инфильтрация 0,01% раствора адреналина;
2. аргоно-плазменная коагуляция;
3. эндоклиппирование.
При остановившемся кровотечении (Forrest IIa, IIb) с целью профилактики рецидива кровотечения применяют методы превентивного эндогемостаза: инфильтрация 0,01% раствора адреналина, аргоно-плазменная коагуляция, орошение нитратом серебра, эндоклиппирование (в моноварианте или в комбинации).
При эндоскопической картине Forrest IIc проведение превентивного эндогемостаза не показано.
На основании клинико-эндоскопической оценки определяется степень риска рецидива кровотечения. Критериями высокого риска рецидива кровотечения являются:
а) кровопотеря тяжелой и крайне тяжелой степени на момент госпитализации;
б) эндоскопическая картина Forrest la, lb, IIa;
в) размеры язвенного дефекта в желудке более 2,5 см, в двенадцатиперстной кишке – более 1,5 см.
После применения эндоскопических методов остановки кровотечения или превентивного эндогемостаза проводится динамический эндоскопический контроль. Повторные ЭГДС выполняются вне зависимости от наличия или отсутствия клинических признаков рецидива кровотечения. При высоком риске рецидива кровотечения повторные ЭГДС (и – при необходимости – эндогемостаз) выполняются каждые 2 часа. При низком риске рецидива кровотечения повторная ЭГДС выполняется через 6 часов.
После проведения ЭГДС в просвет желудка устанавливается назо-гастральный зонд.
Показанием к проведению экстренного оперативного вмешательства является продолжающееся кровотечение (в том числе и рецидивное) при неэффективности эндоскопических методов гемостаза (для кровотечений из варикозно расширенных вен пищевода и желудка – при неэффективности гемостаза на фоне установленного зонда Блэкмора). Интенсивная терапия по подготовке к экстренному хирургическому вмешательству проводится на операционном столе, являясь элементом анестезиологического пособия.
Однократный рецидив кровотечения в стационаре не является прямым показанием к экстренной операции. Обоснованным в такой ситуации будет повторное выполнение эзофагогастродуоденоскопии с проведением эндоскопического гемостаза на фоне активной противоязвенной, гемостатической терапии.
Срочная операция выполняется в течение 24—48 часов после первичного эндоскопического гемостаза больным с язвенным гастродуоденальным кровотечением при наличии объективных признаков сохраняющегося на фоне консервативного лечения и эндогемостаза высокого риска рецидива кровотечения. Она проводится на фоне компенсации постгеморрагических расстройств после предоперационной подготовки. Объем оперативного вмешательства при гастродуоденальных язвах, осложненных кровотечением – дистальная резекция 2/3 – ¾ желудка с удалением или экстерризацией кровоточащей язвы.
Объем оперативного вмешательства при продолжающемся язвенном кровотечении у пациентов крайне высокого операционного риска – гастро- (дуодено-) томия с прошиванием кровоточащих сосудов на протяжении.

Переход к консервативной тактике

Дальнейшее совершенствование неоперативного гемостаза, который стал применятся как окончательный, а не временный, пролонгирующий без рецидивный период, заключающееся в широком применении ингибиторов протонной помпы, сандостатина, гемостатиков, эрадикационной терапии, повышении эффективности методов эндоскопического гемостаза, привело к изменениям в тактике лечения.
Изменился подход лечения больных в группах высокого риска рецидива, прежде всего в «проблемной» группе. Стала оцениваться возможность отказа от операции, стало развиваться мнение, что сама по себе операция – угроза неблагоприятного исхода.
По данным В. К. Гостищева и М. А. Евсеева (2005), снижение хирургической активности в экстренных ситуациях ниже 10% приводит к снижению общей летальности до уровня 1—2%. Операции при язвенных гастродуоденальных кровотечениях приносят плохие результаты. (Шаповальянц С. Г., Михалев А. И., Бабкова И. В. 2017) При возникновении рецидива кровотечения частота неблагоприятных исходов лечения резко возрастает, общая летальность достигает 15%, а послеоперационная летальность 40% и более (Асташов В. П., Клейн В. Е. 2005, Багненко С. Ф., Синеченко Г. И., Вербицкий В. Г., Курыгин А. А. 2007, Гостищев В.К, Евсеев М. А. 2003, Гостищев В. К., Евсеев 2005, Затевахин И. И., Щеголев А. А., Титков Б. Е. 2005, Луцевич Э. В., Белов И. Н. 2008). Особенно это касается пациентов с повышенным операционно-анестезиологическим риском
Высокую эффективность использования эндогемостаза в комплексном лечении более чем у 93% больных с кровотечениями язвенной этиологии. В более чем 90% случаев эндоскопическая остановка кровотечения позволила добиться окончательного гемостаза в язвенном кратере с последующей выпиской пациентов на амбулаторный этап долечивания.
В группе операционного риска немедикаментозный гемостаз используется не в качестве способа временной остановки кровотечения, для пролонгации без рецидивного периода, а в качестве способа окончательной остановки кровотечения.

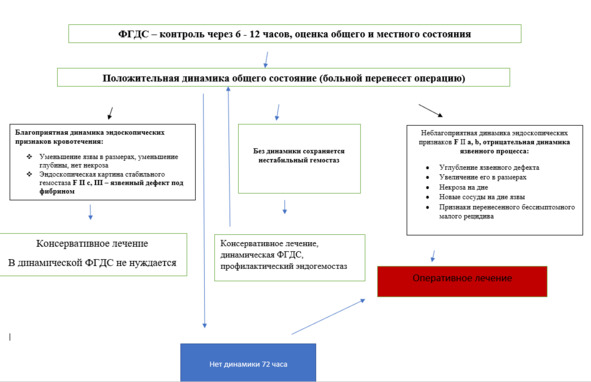

При этом при сохраняющихся эндоскопических признаках нестабильного гемостаза на фоне лечения, показан контроль источника кровотечения – назогастральный зонд, динамическая ФГДС, профилактический гемостаз. При положительной клинико-эндоскопической динамике данные мероприятия при этом тактическом подходе осуществляется до стабилизации гемостаза. Отрицательная динамике клинико-эндоскопической картины при динамической ФГДС является показанием к срочному оперативному лечению.



Консервативный гемостаз И NOM-СТРАТЕГИЯ
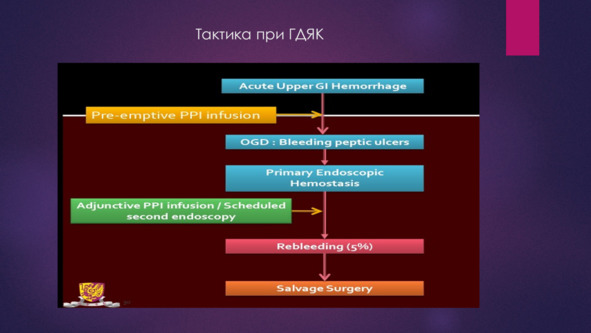
Современный подход к лечению ГДЯК это консервативный подход с применением комбинированного эндоскопического и медикаментозного гемостаза и эндоскопический гемостаз на фоне динамического эндоскопического наблюдения.
Оценка факторов летальности при ГДЯК и расширение эффективности неоперативного гемостаза привела к эволюции тактических подходов и снижению летальности при лечении данной патологии. Хирурги стали избегать операции «отчаяния» на высоте кровотечения, рецидивов, как операций, выполняемых у неподготовленных декомпенсированных больных в крайне неблагоприятных условиях так как они в большинстве случаев приводили к гибели пациентов. Анализ летальности позволил выявить тот факт, что львиная доля, до 60 – 90% смертности при ГДЯК, приходится на послеоперационную летальность. Снижение уровня летальности при ГДЯК было сопряжено со снижением оперативной активности, переходом к современным высокоэффективным методам неоперативного: эндоскопического, медикаментозного и эндоваскулярного гемостаза.
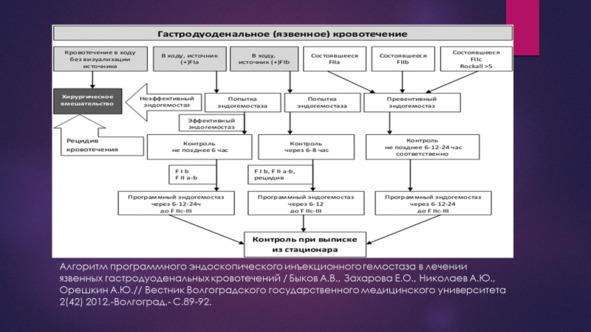

При этом рецидивы язвенного кровотечения стали принципиально расцениваться как ошибки и погрешности в применении методов неоперативного гемостаза. Так А. А. Щеголевым (2024 г) в выступлении на конференции приводит 264 случая неоперативного гемостаза всего лишь с 1 случаем рецидива кровотечения.
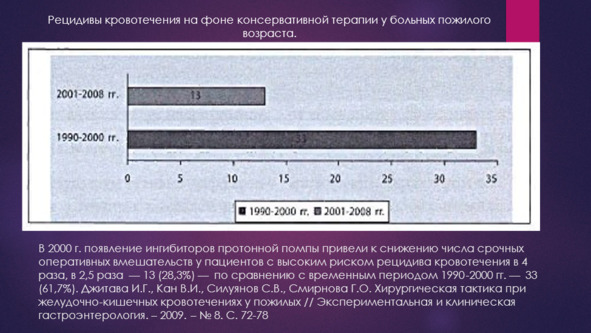
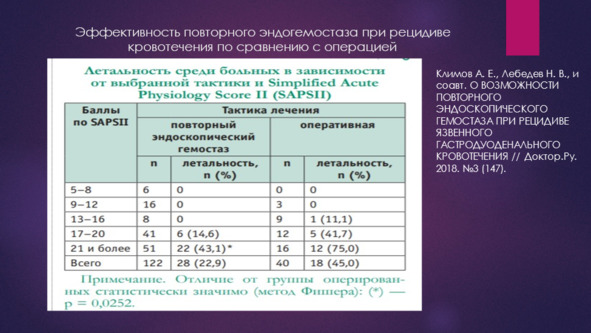
Принципы активного применения неоперативного гемостаза легли в основу NOM стратегии, лежащую в основе современного подхода к лечению ГДЯК.
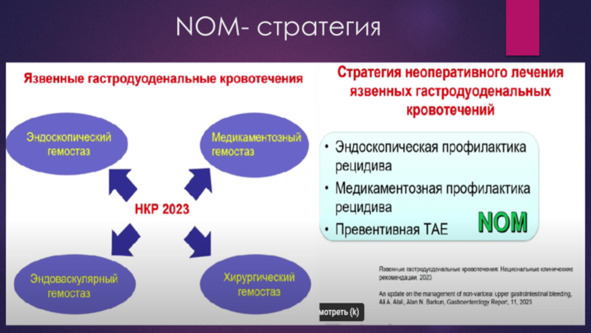


Оперативное лечение при NOM – cстратегии, вынужденная мера при неэффективности прочих методов гемостаза, применяющаяся крайне редко. В рамках данного подхода западные гадлайны по лечению ГДЯК пишутся гастроэнтерлогами, а не хирургами, о применении оперативного лечения в них практически не упоминается.



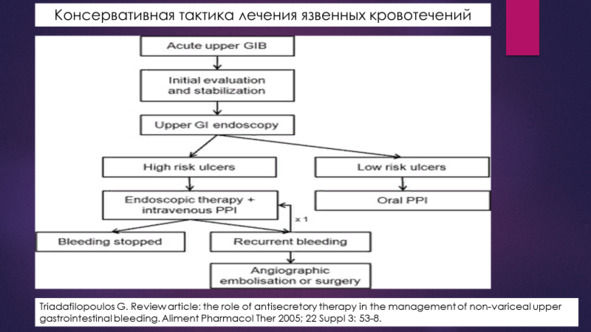
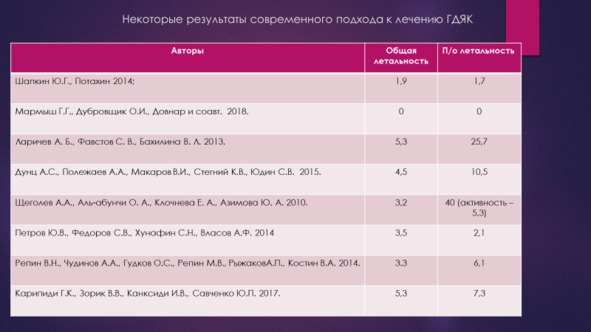
Морфологические изменения при язвенном кровотечении
Таблица 2. Стигматы язвенного кровотечения
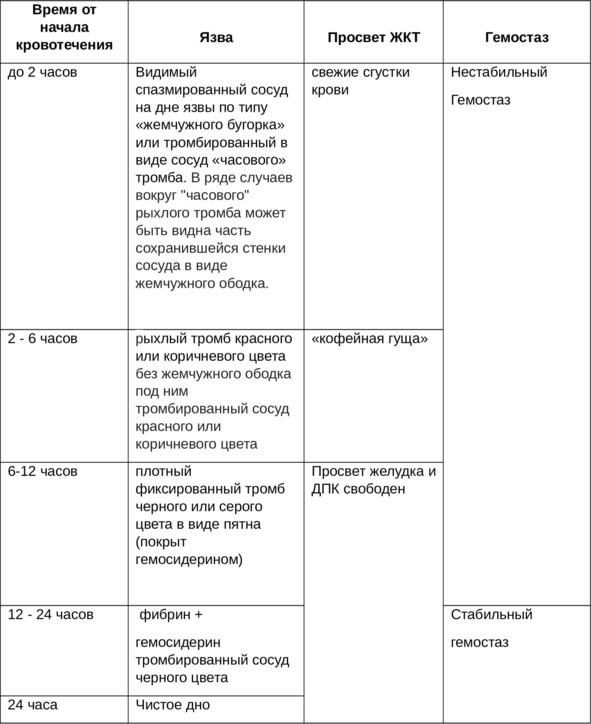
При патологии длительность фаз стигматов удлиняется.
Классические представления о причинах возникновения язвенной болезни сводятся к нарушению равновесия между защитными и агрессивными факторами. Схематически это отражено на так называемых «весах Shey» (1959),
Факторы агрессии
– Желудочный сок
– Ферменты желудочного сока
– Н. Руlori – цитотоксины. Ощелачивание антрального отдела и гипергастринемия.
Факторы защиты:
Желудочная слизь
Центральную роль при этом играет снижение выработки факторов защиты, где пусковым механизмом является гипоксия, ишемия – при кровопотере, сердечной недостаточности, сепсисе. А. Л. Костюченко и соавт. (2000), Н. А. Майстренко и соавт. (1998) указывают, что результатом стессорных воздействий является возникновение стойкого спазма сосудов чревной зон. Б. Р. Гельфанд и соавт. (2004) полагают, что наиболее выраженные нарушения микроциркуляции у больных в критических состояниях возникают именно в проксимальных отделах пищеварительной трубки вследствие наибольшего содержания в их артериях a—адренорецепторов. А. Л. Костюченко и соавт. (2000), в условиях ишемии слизистой оболочки естественная нейтрализация соляной кислоты становится недостаточной, и даже при обычном уровне кислотной продукции развивается ацидоз слизистой оболочки, которая легко подвергается переваривающему действию пепсина.
Не менее важную роль играет и повышенный выбор кортизола при стрессе, а также применение НПВС.
При этом происходит повреждение стенки желудка или ДПК с некрозом и аррозией стенки подлежащего артериального сосуда. При отторжении некроза из язвы возникает разгерметизация аррозированного сосуда или сосудистой системы (сосудов) и наблюдается язвенное кровотечение. Язвенное кровотечение всегда носит артериальный характер. Не редко излившаяся кровь нейтрализует желудочный сок – проходят боли в животе и изжога.
Остановка кровотечения
Ангиоспазм
– Жемчужный бугорок на дне язвы (спазм аррозированного сосуда). Аррозированный сосуд (вена или артерия) на дне язвы рефлекторно спазмируется (артериальные сосуды желудка или ДПК – артерии мышечного типа богатые адренорецепторами, гастродуоденальная область, где особенно их много, реагирует сосудистой реакцией). При кровопотере более 15% ОЦК – уровень катехоламинов в крови растет (достигая показателей в 300 раз превышающих норму).
– Вторичный спазм сосудов происходит за счет выброса из тромбоцитов сосудосуживающих веществ (например, тромбоксана А2 и серотонина), к которому приводит активация тромбоцитов.
– У пожилых людей из-за отстутсвия контракции атеросклеротически измененных сосудов снижена, что ведет повышенному риску кровотечения.
– В каллезной язве стенки аррозированного сосуда изменены, уплотнены, малоэластичны, окружены рубцовой тканью и поэтому не спадаются
На ФГДС аррозированный спазмированный сосуд выступает над дном язвы (желтого цвета) в виде бугорка (жемчужный бугорок). При эндоскопии эта фаза называется фаза «видимого сосуда». Исчезновение видимых сосудов при ФГДС происходит без рецидива кровотечения (98%) в течение 72 часов. Lin HJ, Perng CL, Lee FY, et al Clinical courses and predictors for rebleeding in patients with peptic ulcers and non-bleeding visible vessels: a prospective study. Gut 1994; 35:1389—1393. Белый цвет выступающего сосуда обусловлен его спазмом, спазмированный сосуд характеризуется наибольшей частотой рецидива. Особенно если он расположен на периферии язвы и выступает. Амано, Ю., Н. Морияма, Х. Суэцугу, Н. Ишимура, Т. Имаока, Ю. Комазава, Х. Фудзиширо, С. Исихара, К. Адачи и Ю. Киношита. «Какие типы не кровоточащих видимых сосудов при язвенной болезни желудка следует лечить с помощью эндоскопического гемостаза?». Журнал гастроэнтерологии и гепатологии 19, №1 (2004): 13—17.
В англоязычной литературе существует понятие NBVV (не кровоточащий видимый сосуд). NBVV представляет собой нестабильную и преходящую фазу заживления язвы после начального кровотечения.
Таблица 3. NBVV (не кровоточащий видимый сосуд).
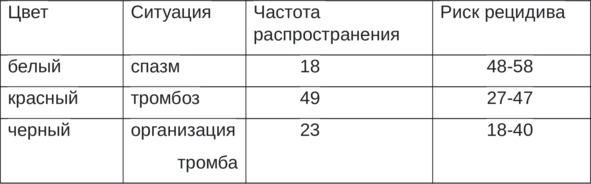
Периферическое расположение сосуда – рецидив 56%, центральное – 20%.
Риск рецидива – видимый не кровоточащий сосуд -40-50%, плотный фиксированный кровяной сгусток – 20—35%.
– В так называемой «опасной зоне» – малая кривизна желудка (при данной локализации язва часто проецируется в зоне внедрения в стенку желудка крупных первичных ветвей передней и задней нисходящих ветвей левой желудочной артерии, ветви чревного ствола отходящей от аорты) или задняя стенка ДПК (гастродуоденальная артерия – ветвь общей печеночной) аррозия особенно опасна. Это сосуды относительно большого диаметра с высоким давлением. Малая кривизна является «пищевой дорожкой», и поэтому легко травмируется, железы ее слизистой оболочки выделяют наиболее активный желудочный сок, стенка в большей степени богата рецепторными приборами и наиболее реактивна, но складки ригидные (негибкие) и при сокращении мышечного слоя не в состоянии закрыть дефект. С этими явлениями связано плохое заживление острой язвы этой локализации и наиболее частое развитие кровотечений. Именно поэтому такая локализация язв желудка, а также их сочетание с язвами желудка другого расположения, может рассматриваться как один из факторов риска развития желудочно-кишечных кровотечений

