
Полная версия
Местные анестетики
Виды нарушения функциональной активности натриевых каналов:
• предотвращение инактивации Nа+-каналов – биологические токсины (типа бутрахотоксина, аконита, вератридина, яда скорпионов) – взаимодействуют с рецепторами, расположенными в ионных каналах и пролонгируют ток ионов натрия; считается, что эти соединения повышают активность Nа+-каналов;
• блокада Nа+-каналов – биологические токсины (токсины морских животных, тетродоксин, сакситоксин) – связываются с рецепторами ближе к наружной поверхности мембраны и нарушают вход ионов натрия в клетки.
Средства для местной анестезии действуют в области натриевых каналов в различных клетках организма. Эффект МА наиболее выражен в области нервных окончаний, нервных волокон и кардиомиоцитов.
Местноанестезирующие средства нарушают развитие фазы деполяризации мембраны клеток в результате взаимодействия со специфическими рецепторами в потенциал-чувствительных натриевых каналах, расположенных на внутренней стороне мембраны. В результате развивается время- и потенциал-зависимая блокада канала. Это приводит:
• к блокаде стимулирующего влияния ионов натрия на проводимость;
• к снижению скорости и степени деполяризации мембраны;
• к нарушению образования и распространения потенциала действия;
• к уменьшению возбудимости окончаний нервных волокон;
• к стабилизации потенциала действия мембраны;
• к блокаде проводимости в периферических нервах;
• к снижению ответа центральной нервной системы на стимуляцию нерва.
Эти рецепторы в норме взаимодействуют с ионами кальция.
Выявлено, что МА способны взаимодействовать с рецептором как в виде неионизированной [МА], так и ионизированной [МАН+] формы. Как показано на рисунке 1, место связывания для неионизированных молекул на специфическом рецепторе расположено ближе к наружной поверхности мембраны, а для ионизированных форм – к внутренней. Чтобы осуществилось присоединение местного анестетика к месту связывания, расположенном ближе к внутреннему краю мембраны, молекула ЛС должна проникнуть внутрь клетки. Соединение поступает в клетку только в том случае, если оно находится во внеклеточной среде в неионизированном виде. В цитоплазме клеток происходит диссоциация молекулы МА с образованием катиона, который и взаимодействует с рецептором. При присоединении МА к рецептору происходят структурные изменения липопротеинов мембраны, что вызывает уменьшение диаметра и снижение проницаемости натриевого канала. Считается, что большее значение в реализации анестезирующего эффекта имеет взаимодействие с рецепторами именно ионизированной формы МА.
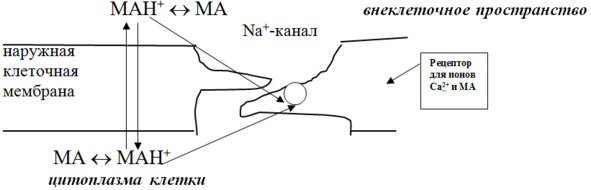
Рис. 1. Схема механизма действия местноанестезирующих средств
Последовательность процессов, приводящих к блокаде проведения импульса по нервному волокну под влиянием местноанестезирующего средства, представлена на схеме 1. Такая последовательность развития событий связана с увеличением количества рецепторов, заблокированных МА, то есть чем выше концентрация препарата, тем выраженность анестезирующего эффекта больше.
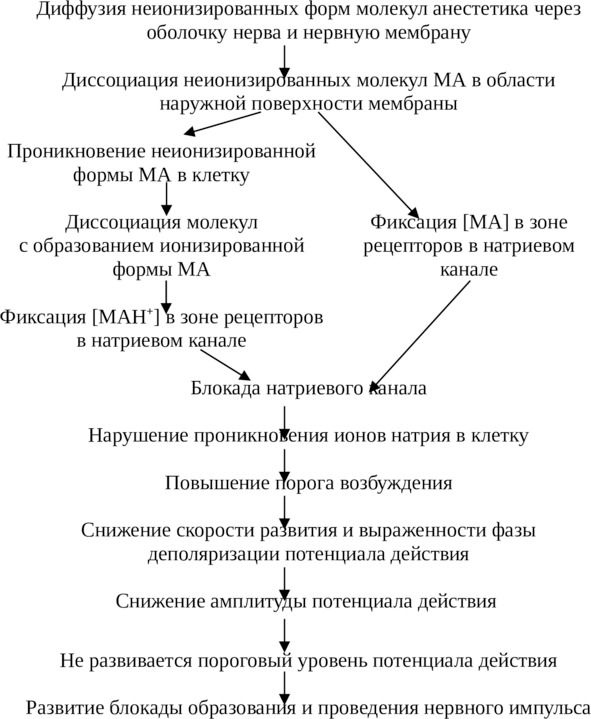
СХЕМА 1
Таким образом, взаимодействие МА с рецепторами приводит к изменению конформации ионного канала и нарушению его функциональной активности. Это приводит к блокаде транспорта ионов натрия и калия через мембрану клеток. В результате снижается скорость развития и величина потенциала действия.
При использовании метода молекулярного моделирования показано, что участок молекулы, с которым происходит нековалентное взаимодействие МА с рецептором, состоит из остатков аминокислот тирозина, фенилаланина, серина, валина и трех остатков изолейцина. Таким образом, данный участок представлен остатками гидрофобных аминокислот.
Существует мнение, что кроме описанного механизма действия, под влиянием местных анестетиков нарушается проницаемость клеточной мембраны для ионов кальция и калия. Уменьшение проницаемости мембраны для этих ионов объясняется изменением поверхностного натяжения фосфолипидов (липидной фазы), образующих ее наружный поверхностный слой.
Показано, что тетракаина гидрохлорид снижает концентрацию ионов кальция внутри клетки, тормозя их высвобождение из саркоплазматического ретикулума клеток скелетных мышц крыс. Это связано с нарушением открытия кальциевых каналов, регулируемых рианодониновыми рецепторами, в присутствии тетракаина гидрохлорида.
Механизм взаимодействия местных анестетиков с N-холинорецепторами.
N-холинорецепторы относятся к рецепторам третьего типа, при стимуляции которых происходит изменение проницаемости ионных каналов, в том числе, натриевых. Показано, что на трансмембранном домене М2 расположены места связывания (сайты) для неконкурентных ингибиторов рецепторов, обращенные в просвет ионного канала. В состав этих сайтов входит остаток серина. Местные анестетики являются представителями неконкурентных блокаторов N-холинорецепторов и, присоединяясь к остатку серина, блокируют вход ионов натрия в клетку, на которой расположены N-холинорецепторы.
Механизм антиаритмического действия.
В механизме антиаритмического действия местноанестезирующих средств основное значение имеет нарушение поступления ионов натрия в кардиомиоциты. Однако определенный вклад в развитие данного эффекта вносит изменение проницаемости наружной мембраны кардиомиоцитов для ионов кальция и калия, причем уменьшение поступления ионов калия связывают со снижением открытия несопряженных К+-каналов.
В ранних исследованиях с помощью конформационного анализа показано, что гидрофобная часть молекулы лидокаина и его производных взаимодействует с участком натриевого канала с образованием электростатических связей. В исследованиях Sunami A. с соавторами (1997) выявлено, что гидрофильный участок молекулы МА присоединяется к S6 сегменту IV домена избирательного фильтра Na+-канала. Однако нельзя полностью отвергать результаты более ранних исследований, так как возможно, что молекула препарата связывается с определенными компонентами ионного канала при участии как гидрофильного, так и гидрофобного участка.
Отмечается, что нарушение проницаемости клеточной мембраны для ионов натрия и, соответственно, анти-аритмический эффект МА могут быть связаны с блокадой Nа+—К+-зависимой АТФазы. Данный фермент осуществляет энергозависимый транспорт ионов натрия, эндогенным ингибитором которого является оубаин, а известными экзогенными блокаторами – сердечные гликозиды (дигоксин). Наиболее вероятным местом взаимодействия препаратов с ферментом является центр связывания, к которому присоединяется оубаин. Однако возможно присоединение МА и к другим структурам Nа+—К+-зависимой АТФ-азы.
Механизм центрального анальгетического и противосудорожного действия.
При изучении механизмов центрального противосудорожного и анальгетического действия МА отмечается, что данные эффекты связаны с нарушением проницаемости мембраны для ионов натрия, но опосредуются через изменение функциональной активности различных рецепторов.
Изучение влияния лидокаина на изменение проницаемости мембран для различных ионов проводилось с использованием изолированных нервных окончаний (синаптосом) коры головного мозга крыс. Показано, что препарат ингибирует вератидин- и калийстимулированный вход ионов кальция в клетку, а также нарушает проницаемость мембраны для ионов натрия. По мнению авторов (Ferrendelli J. A., Daniels-McQueen S.) этот эффект лежит в основе противосудорожного и анальгетического действия лидокаина.
Известно, что ГАМК-ергическая система в головном мозге является ведущей в развитии тормозного эффекта, тогда как различные аминокислоты-нейромедиаторы (глутаминовая кислота, аспарагиновая кислота) обладают стимулирующим влиянием на ЦНС. Отмечается, что лидокаин в определенном диапазоне доз (низкие) способен повышать функциональную активность ГАМК-ергической системы или снижать передачу импульса в синапсах, в которых медиатором является глутаминовая кислота. То есть увеличение активности угнетающего компонента приводит к повышению судорожного порога и является одним из компонентов механизма противосудорожного действия препарата.
Развитие потенциала действия в вентральных корешках спинного мозга в ответ на стимуляцию дорсальных корешков происходит при участии различных систем. Выделяют 3 фазы развития потенциала действия в вентральных корешках спинного мозга:
– ранняя фаза длительностью 10 миллисекунд опосредует передачу импульса с Аβ-волокон (моно- и полисинаптический ответ);
– медленная фаза (1,5 сек.) связана с передачей импульса от афферентных нервных волокон при участии рецепторов N-метил-D-аспарагиновой кислоты (NMDA);
– отсроченная фаза обусловлена передачей импульса при участии нейрокининовых (NK) рецепторов.
При применении лидокаина развитие потенциала действия в вентральных корешках значительно снижается в медленную и отсроченную фазу, не изменяя показателя в ранней фазе. Отмечается, что препарат взаимодействует с тетродоксин-резистентными Na+-каналами, связанными с NK- и NMDA-рецепторами. Авторы (Nagy I., Woolf C.J.) считают, что низкие концентрации лидокаина могут селективно нарушать передачу болевого импульса в спинном мозге.
Глава 6. Факторы, влияющие на выраженность действия местных анестетиков
Выраженность действия местноанестезирующих средств определяется:
• физико-химическими свойствами МА;
• связыванием с белками тканей;
• концентрацией МА в месте действия;
• совместным применением с вазоконстрикторами;
• местом введения МА;
• константой диссоциации МА;
• кислотностью (рН) среды;
• состоянием (активностью) ионных (натриевых) каналов;
• содержанием ионов кальция в экстрацеллюлярной среде;
• количеством ионов калия во внеклеточной жидкости;
• беременность.
Физико-химические свойства местных анестетиков. Большее влияние на скорость развития (латентный период) местноанестезирующего эффекта оказывает величина и липофильность молекулы МА. Чем меньше размер молекулы и больше ее липофильность, тем эффект развивается быстрее. Липофильное вещество легче проникает через мембрану нервного волокна. Лидокаин, прокаин гидрохлорид и мепивакаин сравнительно менее липофильны, чем тетракаин гидрохлорид, этидокаин и бупивакаин. Выраженность действия (глубина и длительность анестезии) у трех последних препаратов значительно выше. Следует отметить, что этот эффект наиболее выражен в опытах in vitro, тогда как в условиях in vivo корреляция между липофильностью и выраженностью действия незначительна. Например, в опытах на изолированном нерве действие лидокаина почти в два раза больше, чем прилокаина и мепивакаина, а этидокаина, чем бупивакаина. При исследовании в условиях целого организма выраженность анестезирующего эффекта лидокаина, прилокаина и мепивакаина практически одинаково, так же как этидокаина и бупивакаина.
Связыванием с белками тканей. Высокая степень связывания МА с белками тканей приводит к увеличению продолжительности действия и снижает всасывание препаратов в кровь. Наиболее изучено взаимодействие местных анестетиков с белками плазмы крови. Предполагается, что степень связывания МА с белками плазмы крови аналогична процессам, происходящим в мембране клеток. Степень связывания с белками плазмы крови наиболее высокая у бупивакаина и этидокаина (94%, 93%), а у прокаина гидрохлорида – около 55%. Длительность блокады плечевого сплетения при использовании бупивакаина продолжается около 10 часов, а при применении прокаина гидрохлорида – в течение 30—60 минут. Этот пример демонстрирует наличие прямой зависимости между степенью связывания препарата с белками и длительностью анестезии.
Концентрация соединения в месте действия. Выраженность местноанестезирующего эффекта МА прямо пропоциональна концентрации (дозе) соединения в месте действия. Чем выше содержание в ткани препарата, тем скорость развития и величина потенциала действия меньше (рисунок 2). То есть эффект будет быстрее начинаться, будут более выражены его глубина и продолжительность. Например, при повышении концентрации бупивакаина с 0,125% до 0,5% раствора (объемы равны, доза от 100 до 150 мг) при эпидуральном введении анестезия развивается значительно быстрее и более выражена.
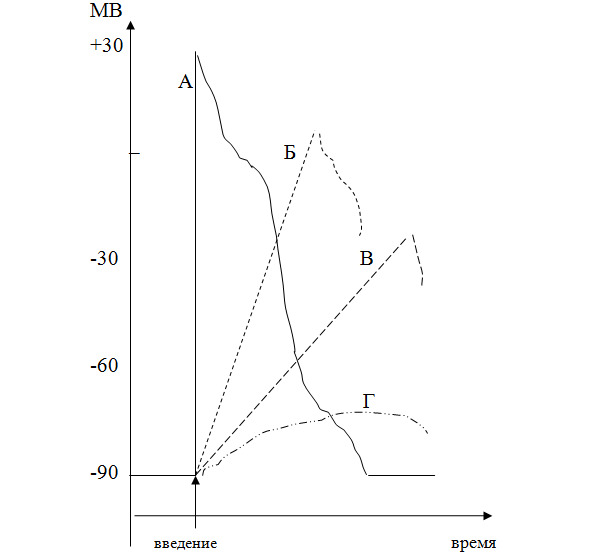
Рис. 2. Влияние концентрации местного анестетика на развитие потенциала действия в нервном волокне
(Примечание:
А – развитие потенциала действия в норме; Б,В,Г – концентрация местного анестетика возрастает в последовательности Б <В <Г.
Ось абсцисс – потенциал внутренней поверхности мембраны.)
Совместное применение с вазоконстрикторами. Снижение абсорбции МА в системный кровоток при совместном применении с сосудосуживающими средствами (эпинефрин, фенилэфрин и т.д.) приводит к увеличению времени, в течение которого МА находятся в месте введения. Однако влияние вазоконстрикторов на выраженность анестезии зависит от ряда причин:
• применяемого препарата;
• вида анестезии;
• места введения.
Так совместное введение МА и эпинефрина приводит к увеличению длительности местной анестезии при:
• проведении инфильтрационной анестезии;
• блокаде периферических нервных стволов;
• эпидуральной блокаде с использованием прокаина гидрохлорида, мепикаина и лидокаина;
• эпидуральной блокаде при родах с использованием 0,125% и 0,25% раствора бупивакаина;
• субарахноидальной блокаде при применении тетракаина гидрохлорида.
В то же время применение эпинефрина вместе с МА не изменяет длительности местной анестезии при эпидуральной блокаде:
• при родах с использованием 0,5% и 0,75% раствора бупивакаина;
• при применении этидокаина и прилокаина.
Способ и место введения. В зависимости от способа и места введения МА начало и продолжительность действия значительно варьируют. При субарахноидальном и подкожном введении эффект развивается наиболее быстро, но он непродолжительный. Самое медленное развитие анестезии и большая продолжительность отмечаются при проведении блокады плечевого сплетения. Это наглядно видно при применении бупивакаина:

Различия сроков наступления и продолжительности анестезии определяется анатомическими особенностями данной области и во многом зависят от васкуляризации ткани.
Константа диссоциации местноанестезирующих препаратов. Важным параметром, влияющим на выраженность эффектов местных анестетиков, является константа диссоциации (рКа) соединения. В том случае, если данный показатель является низким (7,6—7,8), то количество неионизированных молекул ЛС будет высоким при физиологических значениях рН. Следовательно, значительное их число проникнет внутрь клетки и будет способно взаимодействовать с местом связывания на рецепторе, расположенным ближе к внутренней поверхности мембраны. Действие таких препаратов развивается быстро и достаточно хорошо выражено, но сравнительно непродолжительно. Показано, что время наступления обезболивания находится в прямой зависимости от количества препарата в неионизированной форме (таблица 2). То есть процентное содержание МА в неионизированной форме при его введении в ткани с рН 7,4 обратно пропорционально рКа соединения. Например, константа диссоциации мепивакаина, лидокаина и этидокаина составляет 7,7. При введении препаратов в ткани с рН 7,4 около 65% общего количества их молекул переходит в ионизированную форму, а 35% – остаются неионизированными. Тетракаин гидрохлорид имеет рКа 8,6. Поэтому в тканях с рН 7,4 только 5% молекул этого препарата остается в неионизированном виде, а 95% – переходит в катионную форму. Величина рКа бупивакаина равна 8,1, и в тканях с нормальным рН только около 15% молекул присутствуют в неионизированной форме, а 85% – в виде катиона. Следовательно, при введении лидокаина, мепивакаина и этидокаина эффект будет развиваться быстро, а действие прокаина гидрохлорида и тетракаина гидрохлорида наступает медленно. Бупивакаин занимает промежуточное положение между этими группами препаратов как по величине константы диссоциации, так и по наступлению анестезии.
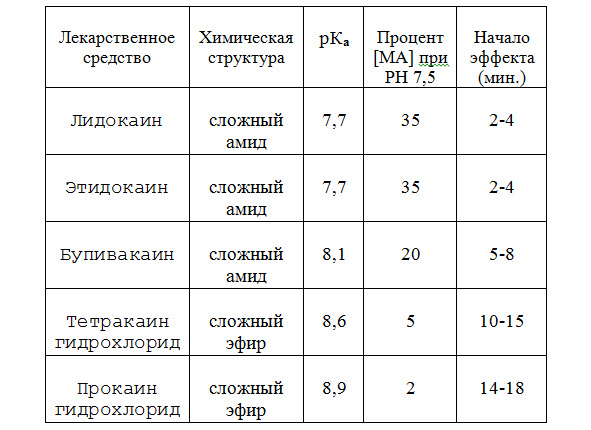
Таблица 2. Взаимосвязь между константой диссоциации местноанестезирующих средств и продолжительностью интервала времени, необходимого для развития нарушения проведения нервного импульса в изолированном нерве
Кислотность среды. Изменение кислотности тканей оказывает значительное влияние на длительность латентного периода и выраженность действия МА. Например, в очаге воспаление рН сдвинуто в кислую сторону и равно 5,0—6,0. Низкое рН тканей вызывает увеличение диссоциации молекул местных анестетиков. Это уменьшает поступление препаратов в клетку, что сопровождается замедлением развития анестезирующего эффекта и его ослаблением. Сдвиг кислотности в щелочную сторону оказывает противоположное действие – более быстрое развитие блокады проведения нервного импульса и усиление выраженности (глубины и продолжительности) анестезии. Введение МА на фоне насыщенного раствора двуокиси углерода или натрия бикарбоната приводит к развитию внутриклеточного алколоза, что создает благоприятные условия для диссоциации молекул МА внутри клетки. Катионные формы МА, с одной стороны, взаимодействуют с рецептором, расположенным в натриевом канале, вызывая нарушение его функциональной активности, а, с другой, не диффундируют из клетки, что поддерживает высокое содержание препарата в ней. Повышение рН среды оказывает действие при применении различных препаратов (лидокаина, бупивакаина) и проведении различных видов анестезии (блокада плечевого сплетения, эпидуральная анестезия).
Состояние (активность) ионных (натриевых) каналов. Ионные каналы, расположенные на наружной клеточной мембране, могут находиться в трех состояниях:
• закрытое состояние или состояние покоя – основное состояние, при котором внутренняя поверхность мембраны заряжена отрицательно;
• открытое состояние или активное состояние – ионные каналы открыты и по ним в данный момент происходит ток ионов;
• инактивированное состояние – развивается после прекращения тока ионов и продолжается до полного восстановления отрицательного заряда внутренней поверхности мембраны клетки.
Аффинность МА к специфическим рецепторам высокая в том случае, если канал находится в активном или инактивированном состоянии. Способность местных анестетиков взаимодействовать с рецепторами ионных каналов, находящихся в состоянии покоя, резко снижается. Состояние ионного канала особенно важно для связывания ионизированной формы ([МАН+]) местного анестетика с рецептором.
Ионный состав внеклеточной жидкости. Большое влияние на эффективность местных анестетиков оказывает ионный состав внеклеточной жидкости, в частности изменение содержания ионов кальция (Са2+) и калия (К+).
Повышение концентрации ионов кальция приводит к снижению (блокаде) анестезирующего действия МА. Это вероятно связано с двумя причинами:
1. в присутствии ионов кальция увеличивается положительный заряд наружной поверхности мембраны (потенциал повышается), что способствует развитию состояния покоя ионных каналов;
2. местные анестетики и ионы кальция взаимодействуют с одними рецепторами, расположенными внутри натриевого канала, а избыток последних затрудняет присоединение МА к месту связывания.
Таким образом, ионы кальция являются антагонистами местноанестезирующих средств.
Увеличение количества ионов калия в экстрацеллюлярной жидкости способствует деполяризации мембраны, что повышает активность натриевых каналов. Повышение содержания ионов калия способствует развитию деполяризации мембраны и инактивации Na+-каналов. Это приводит к увеличению аффинности рецепторов к МА и развитию более выраженного местноанестезирующего эффекта. Следовательно, ионы калия проявляют свойства агонистов местных анестетиков. Однако не отмечается изменения сократимости миокарда и dV/dtmax при высоком и низком содержании ионов калия в присутствии больших концентраций бупивакаина и ропивакаина.
Беременность. Известно, что местная анестезия у беременных женщин развивается быстрее и при использовании более низких доз МА, чем у небеременных. Отмечается две основные причины этого явления:
• анатомические изменения – расширение вен эпидурального пространства приводит к снижению объема эпидурального и субарахноидального пространства, что приводит к более быстрому продольному распространению препаратов;
• гормональные изменения повышают чувствительность нервных волокон к действию МА, начиная с первых месяцев беременности.
В связи с этим при проведении анестезии беременным дозу МА необходимо уменьшать.
Глава 7. Выраженность анестезирующего эффекта препаратов в зависимости от типа нервного волокна
Местноанестезирующие средства блокируют проведение нервного импульса во всех нервных волокнах, но в различных концентрациях и с неодинаковой скоростью развития эффекта. Действие МА на нервные волокна зависит от:
• диаметра нервного волокна;
• наличия и толщины миелиновой оболочки;
• частоты и длительности деполяризации;
• от локализации в нервном пучке.
Наиболее чувствительны к действию местных анестетиков нервные волокна с маленьким диаметром без миелиновой оболочки, в которых скорость проведения импульса и длительность деполяризации большие. Этими свойствами обладают Адельта– и С-волокна, при участии которых осуществляется передача, в том числе и болевых ощущений. К Адельта-типу также относятся нервные волокна, участвующие в передаче температурной чувствительности. Преганглионарные (вегетативные) нервные волокна представлены В-типом, имеют тонкую миелиновую оболочку и скорость проведения импульса в них достаточно высокая. Нарушение проведения нервного импульса по данным нервам приводит, как правило, к развитию нежелательных побочных эффектов при применении МА. Другие виды чувствительности передаются при помощи нервных волокон, относящихся к Аβ– и Ау-типам и покрытых миелиновой оболочкой. Скорость проведения импульса и длительность деполяризации в них практически на порядок ниже, чем в волокнах Адельта – и С-типа. Поэтому тактильная и другие виды чувствительности исчезают позже болевой и температурной. Аксоны соматических нервов и проприоцептивные нервные волокна относятся к Аα-типу. Они покрыты плотной миелиновой оболочкой и скорость проведения нервного импульса в них самая низкая. МА не проникают сквозь шванновскую оболочку двигательных нервов и блокируют проведение импульса только в перехватах (узлах) Ранвье. Для прекращения проведения импульса по этим нервным волокнам необходимо распространение действия МА на три последовательно расположенных узла. При одинаковом диаметре блокада проведения импульса развивается раньше в нервных волокнах, покрытых миелиновой оболочкой, по сравнению с безмиелиновыми волокнами. С этим связано более быстрое наступление блокады в преганглионарных В-волокнах, чем в безмиелиновых С-волокнах. В таблице 3 суммированы сведения о типах нервных волокон и их чувствительности к действию местноанестезирующих средств.
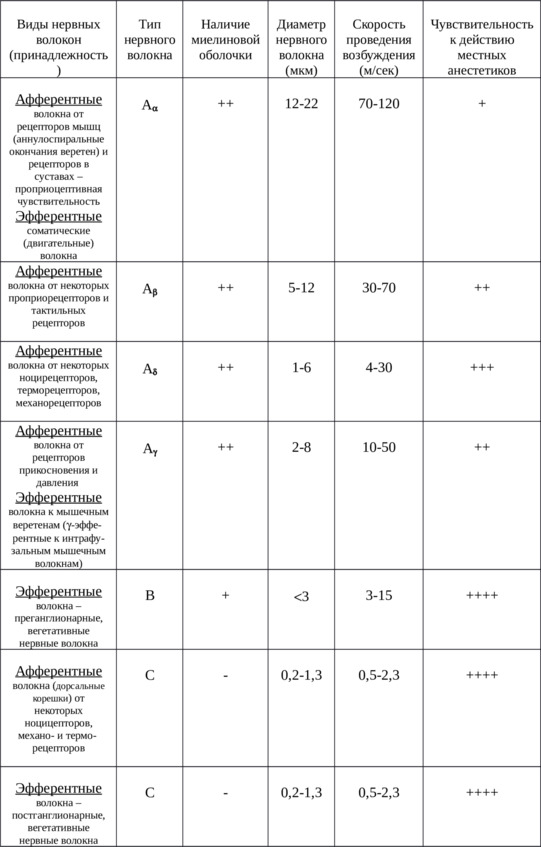
Таблица 3. Характеристика нервных волокон и чувствительность
к действию местноанестезирующих средств
Описанная последовательность блокады проведения нервного импульса в различных нервных волокнах может несколько изменяться в том случае, если нерв входит в состав крупного нервного ствола. Двигательные нервы, как правило, располагаются на его периферии, а чувствительные – в центре. В этом случае вначале нарушается проведение импульса в соматических нервных волокнах (двигательная блокада), а позднее – нарушается чувствительность. В конечностях чувствительные нервные волокна, иннервирующие проксимальные отделы, располагаются на наружной поверхности нерва, а дистальные отделы – в центре. Поэтому при проведении инфильтрационной блокады крупного нерва (седалищный, бедренный и другие нервы) на первом этапе нарушение чувствительности развивается в проксимальных отделах, а на втором – в дистальных, по мере проникновения МА в центр нерва.



