
Полная версия
Психофизиология. Психологическая физиология с основами физиологической психологии. Учебник
Таблица 1.1.
Основные разделы головного мозга

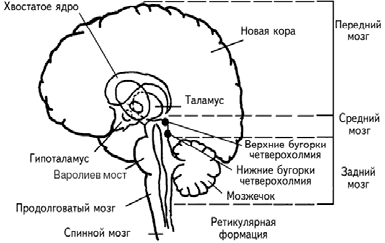
Рис. 1.3. Схематическое расположение подкорковых ядер и структур (Спрингер, Дейч, 1983).
Спинной мозг, который можно рассматривать как продолжение заднего мозга, является центральным коммутатором (переключателем), передающим сообщения из ЦНС на периферию и обратно (рис. 1.4).

Рис. 1.4. Строение спинного мозга. Дорсальные корешки несут сенсорную информацию в мозг, вентральные корешки – эфферентные команды к мышцам (Kalat, 1992).
Периферическая нервная система состоит из соматической и вегетативной (автономной). Соматическая нервная система обеспечивает контроль сокращений поперечно-полосатых мышц, т. е. всей скелетной мускулатуры. Ее нейроны находятся в передних рогах спинного мозга, а их аксоны через передние корешки спинного мозга направляются к скелетным (поперечно-полосатым) мышцам. Там, в области двигательной пластинки мышечного волокна, аксон образует синапс. Соматическая нервная система представлена однонейронным путем (рис. 1.5).
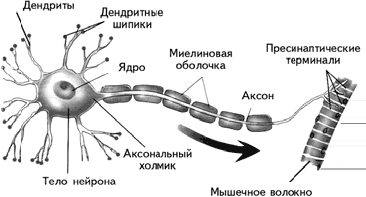
Рис. 1.5. Строение мотонейрона.
Вегетативная нервная система иннервирует гладкую мускулатуру и управляет деятельностью внутренних органов, поэтому ее еще называют висцеральной. Деление периферической нервной системы на соматическую и вегетативную достаточно условно, поскольку в ЦНС существует значительное перекрытие проекций той и другой, и соматические и вегетативные реакции являются равноправными компонентами любой поведенческой реакции.
Вегетативная нервная система состоит из двух анатомически обособленных систем, являющихся функциональными антагонистами – симпатической и парасимпатической (рис. 1.6). В отличие от соматической нервной системы, имеющей однонейронный путь, пути в вегетативной нервной системе являются двухнейронными. Волокна симпатической нервной системы выходят из грудного и поясничного отделов спинного мозга, где лежит первый симпатический нейрон. Затем они сходятся к симпатическим ганглиям, расположенным вдоль позвоночника, где находится второй симпатический нейрон (рис. 1.6).
Волокна парасимпатической нервной системы начинаются в спинном мозге выше или ниже места выхода симпатических нервов (пара – около, лат.) из черепного и крестцового отдела, а затем сходятся в ганглиях, расположенных не вдоль позвоночного столба, а вблизи от иннервируемого органа (рис. 1.6).

Рис. 1.6. Автономная нервная система и органы, иннервируемые ею (Carlson, 1992).
Особенности расположения ганглиев этих двух систем предполагают различие оказываемого ими эффекта. Действие симпатической нервной системы более диффузно, а парасимпатической – более специфично, поскольку связано только с изменениями в органе, рядом с которым находится ганглий. Эти системы различаются и медиаторами, участвующими в синаптической передаче. Основным медиатором для симпатической нервной системы является адреналин, а для парасимпатической – ацетилхолин.
Результаты активности этих двух систем во многом противоположны. Если основная функция симпатической нервной системы состоит в мобилизации организма на борьбу или бегство, то парасимпатическая нервная система преимущественно обеспечивает поддержание гомеостаза. Активация симпатической нервной системы лежит в основе поведения человека, рвущегося в бой. Возбуждение парасимпатической нервной системы обеспечивает пищеварение у человека, лежащего на диване после сытного обеда (вспомните тест Александра Македонского с горящим факелом, описанный во введении).
Симпатическая нервная система возбуждает, а парасимпатическая – тормозит деятельность сердца, первая ослабляет двигательную активность кишечника, вторая ее усиливает. В то же время они могут действовать и заодно: вместе увеличивают двигательную активность слюнных и желудочных желез, хотя состав секретируемого сока в зависимости от доли участия каждой системы меняется. В табл. 1.2 представлены эти различия в результатах деятельности симпатической и парасимпатической нервных систем.
Симпатическая и парасимпатическая системы возникли в эволюции не одновременно. Известно, что у миксин и миног (ранних представителей позвоночных) парасимпатическая система развита достаточно хорошо, но у них отсутствуют даже зачатки симпатической нервной системы. Полного своего развития симпатическая нервная система достигает только у амфибий (Родионов, 1996).
Таблица 1.2.
Особенности симпатической и парасимпатической нервной системы (Бабский и др., 1979).

Первичность парасимпатической нервной системы по отношению к симпатической обнаруживается еще и в том, что при экспериментальном удалении парасимпатической иннервации все ее функции практически перестают выявляться, тогда как при устранении симпатических влияний ни одна из функций не выпадает полностью, поскольку возникает компенсация за счет корковых воздействий на них.
В начале двадцатого века Уолтер Кеннон проводил обширные исследования симпатического отдела вегетативной нервной системы. С тех пор считается, что симпатическая нервная система расширяет диапазон выносливости организма при экстремальных воздействиях, а функционирование организма на базовом уровне обеспечивается парасимпатической нервной системой.
Итак, особенностями функционирования вегетативной нервной системы являются реципрокное взаимодействие ее компонентов (парасимпатического и симпатического), параллельное существование нескольких путей обеспечения функций (отсутствие единого центра), зависимость характера ее реакции от исходного состояния человека, нейрохимическая гетерогенность.
Центральными структурами, включенными в регуляцию активности периферических звеньев вегетативной нервной системы, являются ряд областей переднего, промежуточного мозга и мозгового ствола, которые контролируют преганглионарные симпатические и парасимпатические волокна. К важнейшим ее компонентам относятся инсуларная и медиальная префронтальная кора, центральные ядра миндалины и задние ядра конечной полоски, гипоталамус, околоводопроводное серое вещество мозгового ствола, парабрахиальный регион моста, ядра одиночного тракта, промежуточная ретикулрная медуллярная зона и вентролатеральная медула (Чуприков, Палиенко, 2004).
Клетки мозга
Особенностью живого организма является использование короткоживущих материалов для построения долгоживущих систем. Решение этой на первый взгляд неразрешимой задачи найдено в постоянном обновлении организма. Каждая клетка, каждый орган в нем находятся в состоянии хронического «ремонта», во время которого старые молекулы заменяются новыми. В результате этого структура в целом (например, клетка) живет многие годы, тогда как молекулы вновь и вновь сменяются новыми. Особенно интенсивны эти процессы в мозге, который обновляется на 80 % всего лишь за две недели.
Ведущее значение в деятельности любой клетки принадлежит мембране. В особой мере это относится к нервной системе. В организме человека ее функциями являются интеграция и коммуникация. Эти функции осуществляются через мембрану: прохождение нервного импульса вдоль аксона, приводящее к возникновению потенциала действия за счет переноса ионов через аксональную мембрану; передача информации от одной клетки к другой представляет собой химические и электрические явления на синаптической мембране; гормональная регуляция связана с восприятием управляющих сигналов – гормонов – через синаптические рецепторы на мембране (Хухо, 1990). Толщина ее составляет в среднем 8 нанометров (нм), что меньше чем 0,00001 мм. В 1934 г. исследователи Дж. Даниэли и Й. Даусон предложили модель, согласно которой клеточная мембрана выглядела как сэндвич (разрезанная булка с маслом внутри). Наружные слои модели составляли белки, а внутри «сэндвича» помещались фосфолипиды (сложные жироподобные молекулы) (Климов, Никульчева, 1995).
Современное представление о структуре мембраны введено С. Зингером и Г. Николсоном, предложившими жидкомозаичную модель мембраны (Singer, Nicolson, 1972). Согласно их гипотезе белки мембраны погружены в гель из двойного слоя фосфолипидов. Эти молекулы имеют два конца, из которых один растворим в воде, а другой нет. Фосфолипиды двух слоев повернуты друг к другу своими нерастворимыми в воде концами (рис. 1.7). Молекулы фосфолипидов, находясь в жидком кристаллическом состоянии, подвижны и могут проникать из слоя в слой (так называемая «флип-флоп диффузия»; flip – щелчок, flop – шлепок, англ.) или меняться местами с соседями (латеральная диффузия). У бактерий одна молекула фосфолипидов завершает полный цикл движения вокруг клетки примерно за 1 сек. – нетрудно представить себе подвижность живой клетки и ее частей (Климов, Никульчева, 1995). Жидкомозаичная модель клеточной мембраны – не более чем модель. Это значит, что она является рабочей гипотезой, в настоящее время наиболее адекватно описывающей мембрану. Любой хорошо запланированный эксперимент может ее изменить или даже отвергнуть (Хухо, 1990). В этом учебнике достаточно часто будет встречаться описание моделей, поэтому следует всегда помнить об относительной надежности этих описаний.

Рис. 1.7. Строение мембраны нейрона (Kalat, 1992).
В каждой клетке тела, кроме клеток крови и генеративных клеток, набор генов одинаков. Однако все разнообразие функционирования клеток определяется набором экспрессирующихся генов (находящихся в активном состоянии, при котором синтезируется продукт, кодируемый данным геном). В каждой клетке эти работающие гены составляют лишь небольшую часть генома. В мозге избирательная генная экспрессия обнаружена в амакриновых клетках в сетчатке, клетках Пуркинье в мозжечке, мотонейронах в спинном мозге.
В процессах метаболизма универсальным источником питания мозговой ткани служит глюкоза. Независимо от того, поступила ли она из кишечника или образовалась в печени, глюкоза с током крови попадает во все ткани организма и используется ими для формирования богатых энергией связей, а также как первичный предшественник углеводов. В клетку глюкозу переносит белок, погруженный в клеточную мембрану. Пять форм такого белка уже достаточно хорошо изучены.
Нейроны
Известны два типа клеток мозга: нейроны и глия. Клеточная теория мозга была сформулирована в 1891 году. Она сменила ретикулярную теорию, согласно которой нервная система представлялась синцитием – гигантской плазматической сетью, не разделенной на отдельные ячейки. Сантьяго Рамон-и-Кахаль, экспериментально подтвердивший клеточную структуру мозга, назвал нейроны «загадочными бабочками души, чьих крыл биение в один прекрасный день – как знать? – прольет свет на тайны психической жизни» (Фишбах, 1992) (рис. 1.8). Человек рождается с окончательным количеством нейронов, не способных к дальнейшему делению при обычных условиях.
С. Рамон-и-Кахаль изучал нейроны, используя метод их фиксации, предложенный Камилло Гольджи. Утверждают, что итальянский врач К. Гольджи открыл этот метод у себя на кухне при свете свечи. Это был метод фиксации клетки двухромовокислым калием и импрегнации серебром (Шеперд, 1987). До К. Гольджи зафиксировать нейроны смог Зигмунд Фрейд. С 1876 по 1881 годы он работал с Эрнстом Брюкке – директором института физиологии при Венском университете, физиологом школы Германа Л. Ф. Гельмгольца. Фрейд предложил метод фиксации нейронов с помощью хлористого золота. Он оказался более дорогостоящим и поэтому менее привлекательным для исследователей.

Рис. 1.8. Фотография нейрона, выполненная Ленарт Нилсон (Kalat, 1992).
Преимущество метода Гольджи заключалось в том, что серебро, полностью пропитывая нейроны, не проникает в окружающие их глиальные клетки (рис. 1.9). Воспользовавшись этим методом, С. Рамон-и-Кахаль смог увидеть отдельные нейроны и высказал предположение, что мозг образован дискретными единицами. Он впервые описал нейроны как поляризованные клетки, которые с помощью сильно разветвленных многочисленных отростков – дендритов (dendros – дерево, греч.) – получают сигналы и через единственный неразветвленный длинный отросток – аксон (axon – ось, греч.) – посылают информацию другим клеткам (рис. 1.10). Аксон может ветвиться, и его ветви называются коллатералями. В настоящее время доказано, что у нейрона может быть более одного аксона.
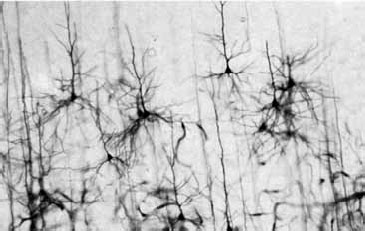
Рис. 1.9. Нейроны. Препарат, представленный на рисунке, получен Дж. Роббинс из лаборатории Д. Хьюбела в Медицинской школе Гарвардского университета (Фишбах, 1992)
C. Рамон-и-Кахаль обнаружил фундаментальное различие между клетками с короткими аксонами, взаимодействующими с соседними клетками, и клетками с длинными аксонами, проецирующимися (посылающими сигналы) в другие участки мозга, и продемонстрировал разнообразие нервных клеток (рис. 1.11).
В 1906 г. С. Рамон-и-Кахалю и К. Гольджи была присуждена Нобелевская премия за открытия, сделанные в исследовании структуры мозга. Парадоксально, что С. Рамон-и-Кахаль получил премию за создание клеточной теории мозга, тогда как К. Гольджи, не разделявший эту точку зрения, даже в Нобелевской речи подчеркнул свою уверенность в том, что глия не является клеточной структурой.

Рис. 1.10. Коммуникация нейронов (Фишбах, 1992).
Нейроны имеют самую разнообразную форму и размер, колеблющийся от 1 до 1000 мкм (т. е. они могут различаться по величине в 1000 раз).
Помимо структурных и молекулярных особенностей, еще более тонкие различия выявляются между нейронами при изучении входов последних (всех поступающих сигналов и аппарата их приема) и проекций (всех посылаемых сигналов и аппарата их передачи), которые зависят от функциональной активности клеток. Места соединений нейронов друг с другом называются синапсами.
Дегенерация и гибель некоторых клеток, волокон и синаптических терминалей – естественная часть процесса развития. В 1949 г. В. Хамбургер и Р. Леви-Монтальчини обнаружили, что в течение определенного короткого периода в самом начале эмбрионального развития дегенерирует большое число клеток в спинальных ганглиях и моторных областях спинного мозга. Ученые показали, что это происходит примерно в тот момент, когда волокна, берущие начало в этих структурах, устанавливают свои связи на периферии. Но особое внимание эти данные привлекли к себе только через 10 лет, когда было показано, что в некоторых случаях численность гибнущих нейронов достигает 75 %. Отмечается совпадение момента гибели с временем иннервации клетками той или иной области мозга своих органов-мишеней (мишень – место воздействия). Было сделано предположение, что при иннервации между аксонами возникает конкурентная борьба за мишени, и те клетки, которые проигрывают в этом процессе, гибнут (Фишбах, 1992).
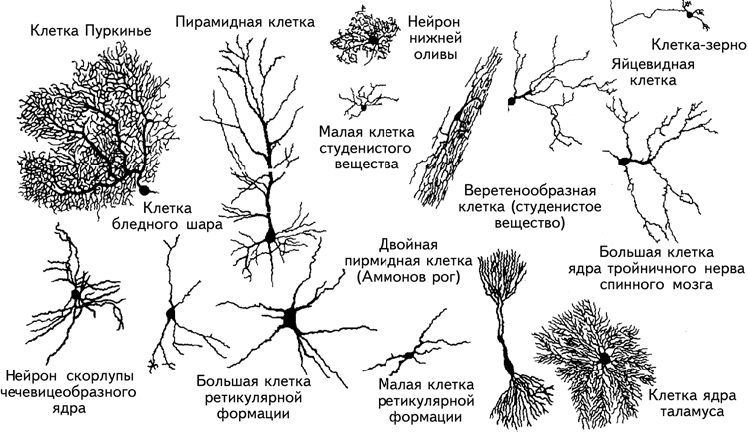
Рис. 1.11. Разнообразные формы нейронов (Фишбах, 1992).
В. Маунткасл, изучая соматосенсорную кору, и Д. Хьюбел и Т. Визел, занимавшиеся зрительной корой, обнаружили, что нейроны с одинаковыми функциями сгруппированы в виде колонок, пронизывающих толщу коры головного мозга. В зрительной коре такой модуль, клетки которого реагируют на линии определенной ориентации, имеет в поперечнике около 0,1 мм. Модуль может включать более 100 тыс. клеток, преобладающее большинство которых образует локальные нейронные сети, выполняющие ту или иную функцию (Фишбах, 1992).
Многие нейроны имеют цвет. Яркость его зависит от функции нейрона. Наиболее интенсивный цвет отмечается на уровне аксонального холмика (место отхода аксона от тела нейрона).
Глия
Нейроны составляют лишь 25 % от всех клеток мозга, остальные 75 % клеток относятся к нейроглии (glia – клей, греч.). Это название было дано в 1846 г. Р. Вирховым, полагавшим, что глия – это цементирующая основа для объединения нервных клеток. В среднем глиальные клетки составляют по величине примерно 1/10 размера нейрона. В отличие от нейронов они способны делиться. Именно благодаря им происходит увеличение объема мозга ребенка, составляющего при рождении примерно четверть мозга взрослого. Возникновение опухолей в мозге также связано не с активностью нейронов, а с бесконтрольным делением глиальных клеток.
Глиальные клетки имеют множество функций, но они не передают информацию, как это делают нейроны (рис. 1.12). Мембранный потенциал глиальных клеток выше, чем у нейронов, и определяется разностью концентраций ионов калия во внутри- и внеклеточном пространстве. Это отличает их от нейронов, мембранный потенциал которых формируется как разностью концентраций ионов калия, так и ионов натрия. При возбуждении нейрона из него одновременно выходят ионы К+ и Na+, что ведет к изменению мембранного потенциала расположенных рядом глиальных клеток. Последние частично поглощают ионы калия, функционируя как калиевый буфер, поддерживающий постоянную внеклеточную концентрацию этих ионов. Повышение внеклеточной концентрации калия могло бы снизить порог возбуждения нейрона, что вело бы к его спонтанной активации. Возможно, что именно этот механизм включается при возникновении эпилептических припадков (Хухо, 1990). Выделяют следующие функции глии.
1. Два типа глиальных клеток образуют миелиновую оболочку для аксонов: олигодендроциты формируют ее в головном и спинном мозге, а Шванновские клетки – в периферической нервной системе. Они обертываются вокруг аксона, изолируя его и ускоряя проведение импульса. Отростки одной глиальной клетки обертываются вокруг разных аксонов, что может способствовать интеграции работы сразу нескольких нейронов.
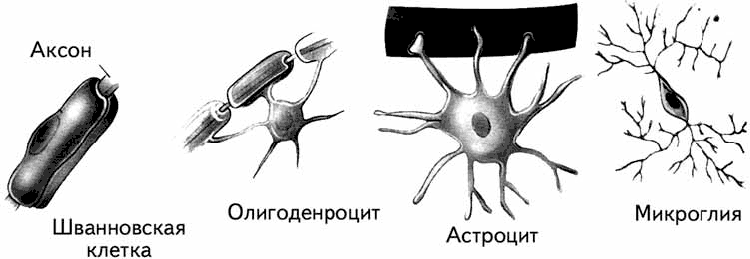
Рис. 1.12. Формы некоторых глиальных клеток.
2. Астроглия и микроглия очищают мозг от погибших нейронов и от ненужного материала, поглощая его.
3. Астроглия также имеет опорную функцию, заполняя промежутки между нейронами и формируя тем самым внутренний скелет.
4. Радиальная глия помогает миграции нейронов и направляет аксоны в сторону расположения их мишеней в период эмбрионального развития. Аналогичным образом Шванновские клетки при повреждениях направляют восстанавливающийся аксон к месту иннервации. Они участвуют и в самом востановлении поврежденных нервов. Было показано, что после повреждения аксона Шванновская клетка может заменять утраченное нервное окончание в мышце и даже выделять медиатор (Хухо, 1990). В зрелом мозге радиальная глия перерождается в другие виды глии, осуществляя опорную функцию.
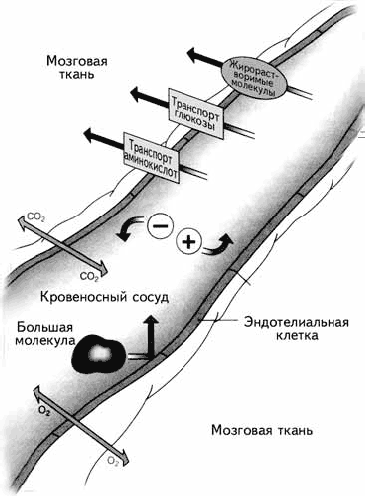
Рис. 1.13. Гематоэнцефалический барьер
5. Астроглия формирует уникальный защитный слой между нейроном и кровеносным сосудом, так что все вещества из крови могут попасть в нейрон только через глиальную клетку. Этот барьер называется гематоэнцефалическим (haima – кровь, enkephalos – мозг, греч.). Гематоэнцефалический барьер могут преодолевать только маленькие молекулы, например ионы, глюкоза, незаменимые аминокислоты и жирные кислоты (рис. 1.13). Благодаря этому большие молекулы, токсины, вирусы и микробы не могут проникнуть в нейрон, что приводит к значительному повышению толерантности (устойчивости) мозга к вирусным инфекциям.
Существует только одна область мозга, где происходит нарушение гематоэнцефалического барьера, – гипоталамус. В нем находятся клетки, секретирующие либерины и статины, управляющие выделением гормонов из гипофиза. Сосуды непосредственно подходят к секретирующим нейронам, выделяющим свои биологически активные вещества прямо в кровь. Ввиду функциональной необходимости гематоэнцефалический барьер в этом месте нарушается. Гипоталамус можно назвать «ахиллесовой пятой» мозга, поскольку только здесь возможно проникновение инфекций в нервную систему человека.
Наличие гематоэнцефалического барьера при инфекционных поражениях мозговой ткани может препятствовать ее лечению путем введения антибиотиков в кровь. Молекулы лекарства не могут попасть в мозг в нужном количестве и не имеют возможности подойти непосредственно к очагу инфекции. Единственным выходом из этой ситуации остается пункция: лекарство вводится в позвоночный канал, связанный с желудочками мозга, через которые и попадает к очагу инфекции.
Передача информации в ЦНС
Информация в мозге передается по аксонам в виде коротких электрических импульсов, называемых потенциалами действия (ПД). Их амплитуда составляет около 100 мВ, длительность – 1 мс. ПД возникают в результате движения положительно заряженных ионов натрия через клеточную мембрану из внеклеточной жидкости внутрь клетки по специальным натрий-калиевым каналам. Концентрация натрия в межклеточном пространстве в 10 раз больше внутриклеточной.
Существует пассивный и активный транспорт ионов в нейрон. Пассивный (то есть не связанный с расходом энергии) происходит через раздельные Na+ и К+ каналы в мембране аксона. Активный транспорт связан с деятельностью Na+, К+ – насоса, который перекачивает ионы из менее концентрированного раствора в более концентрированный за счет энергии, высвобождаемой при гидролизе АТФ.
В состоянии покоя поддерживается трансмембранная разность потенциалов около 70 мВ (цитоплазма заряжена отрицательно относительно внешней среды). Мембрана практически непроницаема для Na+, тогда как К+ проходит сквозь нее и формирует потенциал покоя. Положительные заряды компенсируются неспособными выйти за пределы клетки анионами. Они и создают суммарный отрицательный заряд. Этот процесс продолжается до тех пор, пока формирующийся внутри клетки отрицательный заряд не будет сдерживать выходящие из нее ионы К+. Устанавливается состояние, при котором число входящих и выходящих ионов К+ уравновешивается.
Несмотря на то, что натрий-калиевый насос выбрасывает ионы натрия из клетки, они очень медленно проникают в клетку. Физическая или химическая стимуляция, деполяризующая мембрану, т. е. снижающая разность потенциалов, увеличивает ее проницаемость для ионов натрия. Поток ионов натрия внутрь клетки еще сильнее деполяризует мембрану (рис. 1.14). Если нейрон возбуждается достаточно интенсивно, то натрий-калиевый насос не успевает предоставить нужное количество натрия для деполяризации, и в этом нейрону помогает глиальная клетка (рис. 1.12).
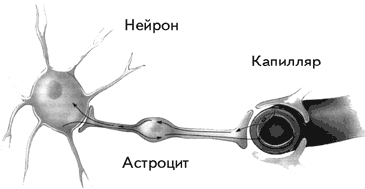
Рис. 1.14. На высоте активности нейрона, когда потребности в ионах натрия больше, чем это обеспечивает натрий-калиевый насос, астроцит действует как насос, перекачивая натрий из ближайшего сосуда (Kalat,1992).
Когда достигается некоторое критическое значение потенциала, называемое пороговым, на уровне аксонального холмика нейрона возникает ПД – распространяющийся по аксону потенциал. При этом положительная обратная связь на уровне мембраны нейрона приводит к регенеративным сдвигам, в результате которых знак разности потенциалов изменяется на противоположный, т. е. внутреннее содержимое клетки становится заряженным положительно по отношению к внешней среде. Приблизительно через 1 мс проницаемость мембраны для натрия падает, натрий-калиевый насос выбрасывает натрий из клетки, и трансмембранный потенциал возвращается к своему значению в состоянии покоя – 70 мВ.
После каждого такого разряда нейрон становится на некоторое время рефрактерным (неспособным к активации), т. е. натриевая проницаемость мембраны в этот период не может изменяться. Это кладет предел частоте генерации ПД – не более 200 раз в секунду. Максимальная скорость распространения нервного импульса составляет приблизительно 100 м/сек. Это более чем в миллион раз меньше скорости, с которой электрический сигнал движется по медной проволоке. Таким образом, скорость распространения ПД сравнительно низка.
Синаптическая передача информации









