
Полная версия
Акушерство
Аномалии девственной плевы и вульвы могут проявляться в виде сплошной девственной плевы, встречающейся при атрезии входа во влагалище или его аплазии. Гипо- и эписпадия приводят к деформации вульвы. В результате во влагалище или в преддверие влагалища может открываться просвет прямой кишки. При атрезии девственной плевы может образоваться гематокольпос, гематометра, гематосальпинкс, что обнаруживается только после наступления менструаций.
Аномалии развития влагалища могут проявляться в виде агенезии, аплазии или атрезии вследствие воспаления, перенесенного в анте- или постнатальный период. Во влагалище, развивающемся из слияния каудальных концов парамезонефральных протоков, может быть перегородка от сводов влагалища до девственной плевы. Иногда во влагалище бывает поперечная перегородка.
Аномалии развития матки встречаются нередко. Они чрезвычайно разнообразны (рис. 10). Удвоение матки и влагалища при их обособленном расположении (uterus didelphus) формируется при отсутствии слияния правильно развитых парамезонефральных протоков. Обе матки хорошо функционируют. Беременность может развиваться как в одной, так и в другой матке. Uterus duplex et vagina duplex – аномалия развития похожа на предыдущую, но матка и влагалище на определенном участке соединены более тесно с помощью фиброзно-мышечной перегородки. Одна из маток может быть по величине меньше другой и в функциональном отношении неполноценной. С этой же стороны может быть атрезия гимена и (или) внутреннего маточного зева. Возможно раздвоение шейки и тела матки при общем влагалище (uterus bicornis bicollis) или раздвоение тела при общей шейке матки и общем влагалище (uterus bicornis unicollis).
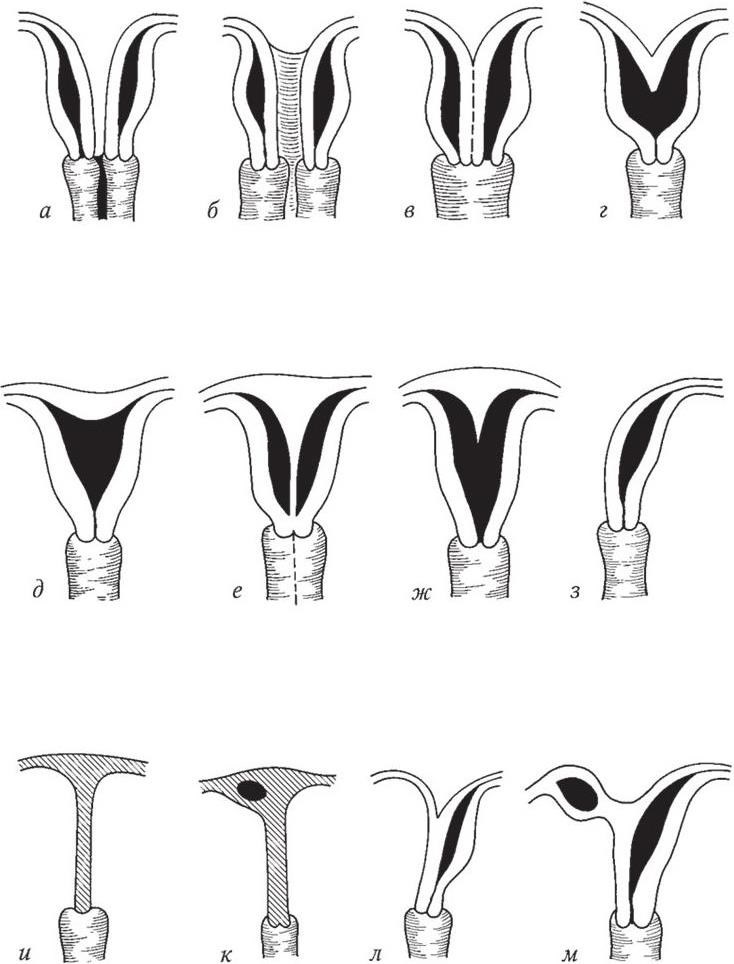
Рис. 10. Аномалии развития матки:
а – uterus didelphus; б – uterus duplex et vagina duplex; в – uterus bicornis bicollis; г – uterus bicornis unicollis; д – uterus arcuatus; е – uterus septus duplex; ж – uterus subseptus; з – uterus unicornis; и, к, л, м – uterus bicornis rudimentarius
Встречается аномалия развития, обусловленная недоразвитием одного из парамезонефральных протоков, что приводит к формированию рудиментарногорога. Полость рудиментарного рога может сообщаться или не сообщаться с полостью матки.
При глубоком поражении одного из парамезонефральных протоков возникает редкая патология — однорогая матка (uterus unicornis). У больных при этом, как правило, имеется один яичник и одна почка. Может быть аномалия развития, при которой влагалище и матка представляют собой тонкие соединительнотканные зачатки – синдром Майера – Рокитанского – Кюстера – Мюлле – ра – Хаусера (uterus bicornis rudimentarius solidus).
Аномалии развития маточных труб встречаются редко. Может наблюдаться удвоение маточных труб, недоразвитие или отсутствие одной маточной трубы. Эта патология, как правило, сочетается с аномалиями развития матки.
Аномалии развития яичников возникают, когда в процессе антенатального развития у плода имеет место асимметрия развития яичников: преобладание в размерах и в функциональном отношении правого яичника. Яичник может отсутствовать с одной стороны. Нередко эта патология сочетается с однорогой маткой. Очень редко могут отсутствовать оба яичника: на их месте находят фиброзные тяжи. Такая аномалия развития характерна для дисгенезии гонад. Аномальные яичники могут располагаться в несвойственных им местах (например, в паховом канале).
МОЛОЧНЫЕ ЖЕЛЕЗЫ
Молочные железы – сложный в анатомическом и функциональном отношении орган. Они расположены на передней грудной стенке между III и IV ребрами. Тело железы имеет форму выпуклого диска с неровной поверхностью спереди, где находятся выступы и углубления, заполненные жировой клетчаткой. Задняя поверхность железы прилегает к фасции большой грудной мышцы. Паренхима железы представлена сложными альвеолярно-трубчатыми железами, собранными в мелкие дольки, из которых формируются крупные доли. Каждая доля имеет выводной проток. Некоторые протоки могут соединяться перед выходом на поверхность соска, поэтому число отверстий на соске может быть от 12 до 20. Паренхима железы заключена в соединительнотканный футляр, образованный расслоением поверхностной грудной фасции, покрывающей спереди большую грудную и зубчатую мышцы (см. цв. вкл., рис. 1). Под передним листком расщепленной поверхностной фасции имеется большое количество жировой ткани, окружающей молочную железу снаружи и проникающей между ее долями. От фасциального футляра в глубь железы распространяются соединительнотканные тяжи и перегородки. Они пронизывают всю ткань железы и образуют ее мягкий остов, в котором располагаются жировая клетчатка, молочные протоки, кровеносные и лимфатические сосуды, нервы. Между железистыми дольками паренхимы имеется более нежная и рыхлая соединительная ткань, лишенная жировой клетчатки. Внутридольковые перегородки продолжаются кпереди, за пределы фасциального футляра железы, к глубоким слоям кожи в виде соединительнотканных тяжей – связок Купера.
Молочная железа снабжается кровью ветвями внутренней грудной и подмышечной артерий, а также ветвями межреберных артерий.
Глава 4
МЕНСТРУАЛЬНЫЙ ЦИКЛ И ЕГО РЕГУЛЯЦИЯ. ФИЗИОЛОГИЧЕСКИЕ ПРОЦЕССЫ В ОРГАНИЗМЕ ЖЕНЩИНЫ В РАЗЛИЧНЫЕ ПЕРИОДЫ ЖИЗНИ
МЕНСТРУАЛЬНЫЙ ЦИКЛ И ЕГО РЕГУЛЯЦИЯ
М е н с т р у а л ь н ы й ц и к л – одно из проявлений сложного биологического процесса в организме женщины, характеризующегося циклическими изменениями функции половой (репродуктивной) системы, сердечно-сосудистой, нервной, эндокринной и других систем организма. Нормальный менструальный цикл включает три компонента: 1) циклические изменения в системе гипоталамус – гипофиз – яичники; 2) циклические изменения в гормонально-зависимых органах (матке, маточных трубах, влагалище, молочных железах); 3) циклические изменения (колебания функционального состояния) нервной, эндокринной, сердечно-сосудистой и других систем организма (рис. 11).
Изменения в организме женщины на протяжении менструального цикла носят двухфазный характер, что связано с ростом и созреванием фолликула, овуляцией и развитием желтого тела в яичниках. Наиболее выраженные циклические изменения происходят в слизистой оболочке матки (эндометрии). Биологическое значение изменений, происходящих на протяжении менструального цикла, состоит в осуществлении репродуктивной функции (созревание яйцеклетки, ее оплодотворение и имплантация зародыша в матке). Если оплодотворения яйцеклетки не происходит, функциональный слой эндометрия отторгается, из половых путей появляются кровянистые выделения, называемые менструацией. Появление менструаций свидетельствует об окончании циклических изменений в организме. Длительность одного менструального цикла определяют от первого дня наступившей менструации до первого дня следующей менструации. У 54 % здоровых женщин длительность менструального цикла составляет 26 – 29 дней, у 20 % – 23 – 25 дней, у 18 % – 30 – 35 дней. Циклы длительностью менее 23 дней встречаются редко. Идеальным считается менструальный цикл длительностью 28 дней.
Репродуктивная система является функциональной, как и сердечно-сосудистая, дыхательная, нервная и другие системы организма. Теория функциональных систем была создана в 1930 – 1934 гг. П. К. Анохиным. Функциональная система – динамическая организация структур и процессов организма, включающая отдельные компоненты независимо от их анатомической, тканевой и физиологической принадлежности. Она является интегральным образованием, включающим центральные и периферические звенья и «работающим» по принципу обратной связи, т. е. обратной афферентации (постоянная оценка конечного эффекта). Деятельность репродуктивной системы направлена на воспроизводство, т. е. существование вида.
Репродуктивная система функционирует по иерархическому типу. В ней существует пять уровней, каждый из которых регулируется вышележащими структурами по механизму обратной связи.
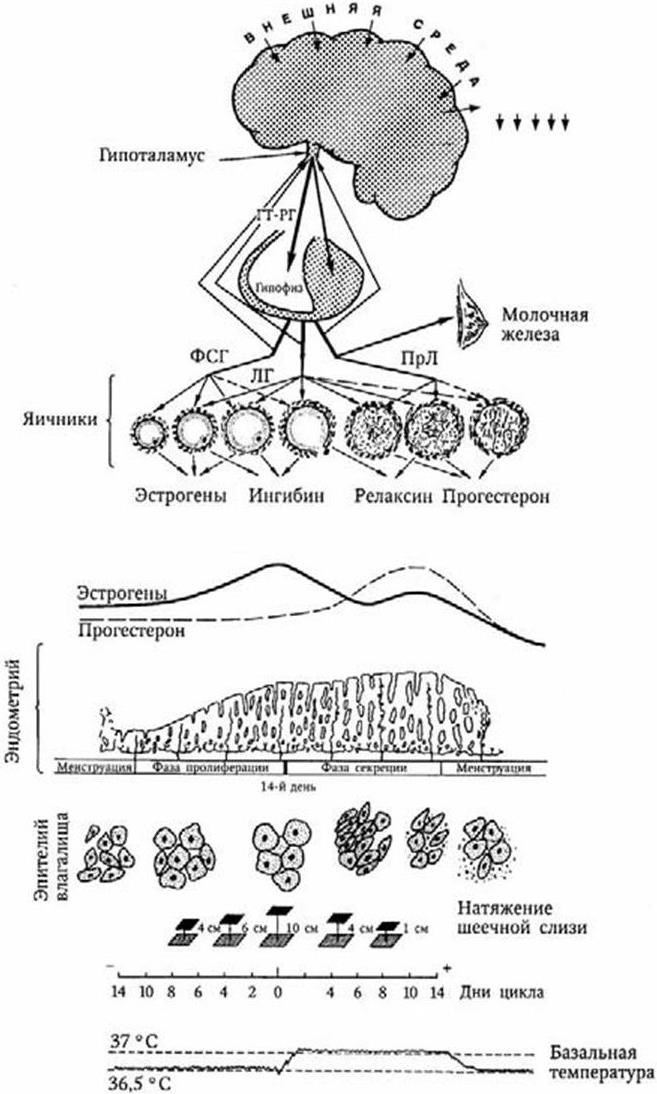
Рис. 11. Регуляция менструального цикла
I уровень – ткани-мишени (половые органы, молочные железы, волосяные фолликулы, кожа, кости, жировая ткань). Клетки этих органов и тканей содержат рецепторы, чувствительные к половым гормонам. Содержание стероидных рецепторов в эндометрии изменяется в зависимости от фазы менструального цикла. В плазме содержатся цитозолрецепторы, обладающие строгой специфической чувствительностью к экстрадиолу, прогестерону, тестостерону. Молекула стероидного гормона захватывается цитозолрецептором, и образовавшийся комплекс транслоцируется в ядро клетки. Здесь возникает новый комплекс с ядерным белковым рецептором. Этот комплекс связывается с хроматином, регулирующим транскрипцию (рис. 12). К I уровню репродуктивной системы относится также внутриклеточный медиатор – цАМФ (циклический аденозинмонофосфат), регулирующий метаболизм в клетках тканей-мишеней. К этому же уровню относятся простагландины (межклеточные регуляторы). Их действие реализуется через цАМФ.
Как уже указывалось, наиболее выраженные циклические изменения происходят в эндометрии. По характеру этих изменений выделяют фазу пролиферации, фазу секреции и фазу кровотечения (менструация).
Фаза пролиферации – фолликулиновая (5 – 14-й дни цикла), может быть короче или длиннее на 3 дня. Она начинается после менструации и заключается в разрастании желез, стромы и сосудов.
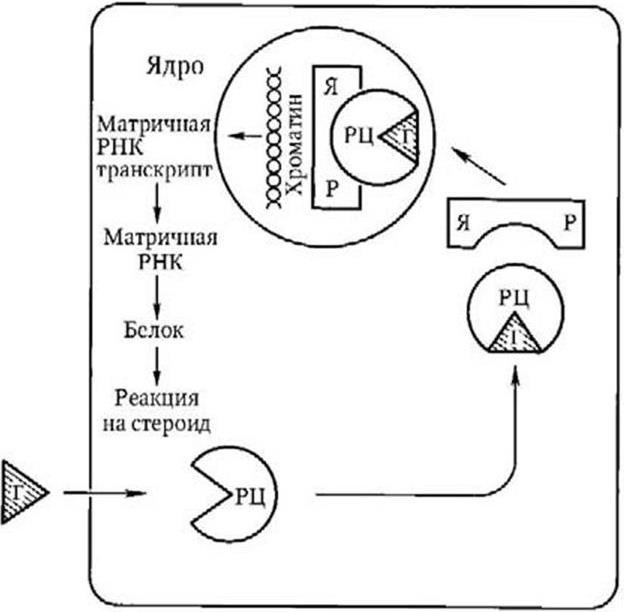
Рис. 12. Взаимодействие стероидного гормона и клетки органа-мишени:
Г – гормон; РЦ – рецептор цитоплазматический; ГРЦ – комплекс гормон – рецептор цитоплазматический; ЯР – ядерный рецептор; ЯРРЦГ – комплекс ядерный рецептор – рецептор цитоплазматический – гормон
Под влиянием постепенно повышающейся концентрации эстрадиола в ранней (5 – 7-й день) и средней (8 – 10-й день) стадиях фазы пролиферации происходит рост желез и разрастание стромы. Железы эндометрия имеют вид прямых или несколько извитых трубочек с прямым просветом. Между клетками стромы располагается сеть аргирофильных волокон. Спиральные артерии мало извиты. В поздней стадии фазы пролиферации (11 – 14-й день) железы эндометрия становятся извитыми, иногда они штопорообразны, просвет их несколько расширен. В эпителии некоторых желез обнаруживаются мелкие субнуклеарные вакуоли, содержащие гликоген. Спиральные артерии, растущие из базального слоя, достигают поверхности эндометрия, они несколько извиты. Сеть аргирофильных волокон концентрируется в строме вокруг желез эндометрия и кровеносных сосудов. Толщина функционального слоя эндометрия к концу фазы пролиферации составляет 4 – 5 мм.
Фаза секреции (лютеиновая) длится 14 дней (±1 день) и непосредственно связана с активностью желтого тела. Она характеризуется тем, что эпителий желез начинает вырабатывать секрет, содержащий кислые гликозаминогликаны, гликопротеиды, гликоген. В ранней стадии фазы секреции (15 – 18-й день) появляются первые признаки секреторных превращений. Железы становятся более извитыми, просвет их несколько расширен. Во всех железах эндометрия появляются крупные субнуклеарные вакуоли, оттесняющие ядро к центру клетки. В вакуолях обнаруживается гликоген. В поверхностных слоях эндометрия иногда могут наблюдаться очаговые кровоизлияния, произошедшие во время овуляции и связанные с кратковременным снижением уровня эстрогенов.
В средней стадии фазы секреции (19 – 23-й день), когда имеет место максимальная концентрация прогестерона и повышение уровня эстрогенов, функциональный слой эндометрия становится более высоким (его толщина достигает 8 – 10 мм) и отчетливо разделяется на 2 слоя. Глубокий (губчатый, спонгиозный) слой, граничащий с базальным, содержит большое количество сильно извитых желез и небольшое количество стромы. Плотный (компактный) слой составляет 1/4—1/5 толщины функционального слоя. В нем меньше желез и больше соединительнотканных клеток. В просвете желез находится секрет, содержащий гликоген и кислые мукополисахариды. Наивысшая степень секреции обнаруживается на 20 – 21-й день. К 20-му дню в эндометрии обнаруживается максимальное количество протеолитических и фибринолитических ферментов. На 20 – 21-й день цикла в строме эндометрия возникают децидуальноподобные превращения (клетки компактного слоя становятся крупными, округлой или полигональной формы, в их цитоплазме появляется гликоген). Спиральные артерии резко извиты, образуют «клубки» и обнаруживаются во всем функциональном слое. Вены расширены. В средней стадии фазы секреции происходит имплантация бластоцисты. Самые лучшие условия для имплантации представляют структура и функциональное состояние эндометрия на 20 – 22-й день (6 – 8-й дни после овуляции) 28-дневного менструального цикла. Поздняя стадия фазы секреции (24 – 27-й день) в связи с началом регресса желтого тела и снижением концентрации продуцируемых им гормонов характеризуется нарушением трофики эндометрия и постепенным нарастанием в нем дегенеративных изменений. Уменьшается высота эндометрия (примерно на 20 – 30 % по сравнению со средней стадией фазы секреции), сморщивается строма функционального слоя, усиливается складчатость стенок желез, и они приобретают звездчатые или пилообразные очертания. Из зернистых клеток стромы эндометрия выделяются гранулы, содержащие релаксин. Последний способствует расплавлению аргирофильных волокон функционального слоя, подготавливая менструальное отторжение слизистой оболочки. На 26 – 27-й день цикла в поверхностных слоях компактного слоя наблюдаются лакунарное расширение капилляров и очаговые кровоизлияния в строму. Состояние эндометрия, подготовленного таким образом к распаду и отторжению, называется анатомической менструацией и обнаруживается за сутки до начала клинической менструации.
Фаза кровотечения (менструация) включает десквамацию и регенерацию эндометрия. В связи с регрессом, а затем и гибелью желтого тела и резким спадом содержания гормонов в эндометрии нарастают гипоксия и те расстройства, которые начались еще в поздней стадии фазы секреции. В связи с длительным спазмом артерий наблюдается стаз крови, образование тромбов, повышенная проницаемость и ломкость сосудов, кровоизлияния в строму, лейкоцитарная инфильтрация. Развивается некробиоз ткани и ее расплавление. Вслед за длительным спазмом сосудов наступает их паретическое расширение, сопровождающееся усиленным притоком крови и разрывом стенки сосудов. Происходит отторжение (десквамация) некротизированных отделов функционального слоя эндометрия. Полное отторжение обычно заканчивается на 3-й день цикла.
Регенерация (3 – 4-й день цикла) происходит после отторжения некротизированного функционального слоя из тканей базального слоя (краевых отделов желез). В физиологических условиях на 4-й день цикла вся раневая поверхность слизистой оболочки эпителизируется.
II уровень репродуктивной системы – яичники. В них происходит рост и созревание фолликулов, овуляция, образование желтого тела, синтез стероидов. Основная масса фолликулов (90 %) претерпевает атретические изменения. И лишь небольшая часть фолликулов проходит цикл развития от примордиального до преовуляторного фолликула, овулирует и превращается в желтое тело. У человека на протяжении одного менструального цикла развивается только один фолликул. Будущий доминантный фолликул в первые дни менструального цикла имеет диаметр 2 мм, а к моменту овуляции (в среднем за 14 дней) увеличивается до 21 мм. Объем фолликулярной жидкости увеличивается в 100 раз.
Количество клеток гранулезы увеличивается с 0,5 × 106 до 50 × 106.
Этапы развития доминантного фолликула. Примордиальный фолликул состоит из яйцеклетки, окруженной одним рядом уплощенных клеток фолликулярного эпителия (рис. 13). В процессе созревания фолликула яйцеклетка увеличивается в размере, клетки фолликулярного эпителия размножаются и округляются, образуется зернистый слой фолликула (stratum granulosum). В гранулезных клетках зреющего фолликула имеются рецепторы к гонадотропным гормонам, определяющие чувствительность яичников к гонадотропинам и регулирующие процессы фолликуло- и стероидогенеза. В толще зернистой оболочки за счет секреции и распада клеток фолликулярного эпителия и транссудата из кровеносных сосудов появляется жидкость. Яйцеклетка оттесняется жидкостью к периферии, окружается 17 – 50 рядами клеток гранулезы. Возникает яйценосный холмик (cumulus oophorus). В граафовом пузырьке яйцеклетка окружена стекловидной оболочкой (zona pellucida). Строма вокруг зреющего фолликула дифференцируется на наружную (tunica externa thecae folliculi) и внутреннюю покрышки фолликула (tunica interna thecae folliculi). Зреющий фолликул превращается в зрелый.
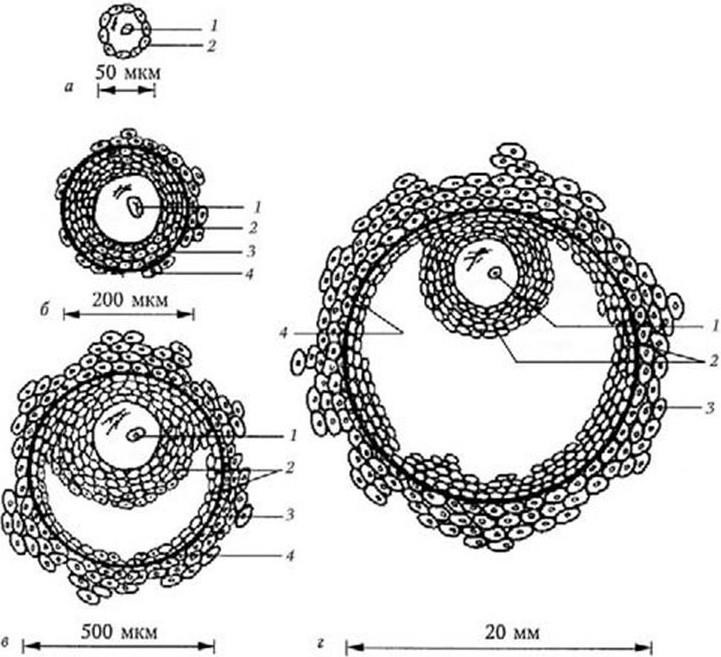
Рис. 13. Развитие доминантного фолликула в течение менструального цикла:
а – примордиальный фолликул; б, в – зреющий фолликул; г – зрелый фолликул:
1 – яйцеклетка; 2 – клетки фолликулярного эпителия; 3 – наружная покрышка фолликула; 4 – внутренняя покрышка фолликула
В фолликулярной жидкости резко увеличивается содержание эстрадиола (E2) и фолликулостимулирующего гормона. Подъем уровня Е2 стимулирует выброс лютеинизирующего гормона и овуляцию. Фермент коллагеназа обеспечивает изменения в стенке фолликула (истончение и разрыв). Играют роль в разрыве преовуляторного фолликула простагландины (ПГF2α и ПГE2) и протеолитические ферменты, содержащиеся в фолликулярной жидкости, а также окситоцин и релаксин.
На месте разорвавшегося фолликула образуется желтое тело, клетки которого секретируют прогестерон, эстрадиол и андрогены. Полноценное желтое тело образуется только тогда, когда в преовуляторном фолликуле содержится достаточное количество гранулезных клеток с высоким содержанием рецепторов ЛГ.
Стероидные гормоны продуцируются клетками гранулезы, клетками theca folliculi interna и в меньшей степени клетками theca folliculi externa. Клетки гранулезы и тека-клетки участвуют в синтезе эстрогенов и прогестерона, а клетки theca folliculi externa – в синтезе андрогенов (см. цв. вкл., рис. 2).
Исходным материалом для всех стероидных гормонов является холестерол, образующийся из ацетата или липопротеидов низкой плотности. Он поступает в яичник с током крови. В синтезе стероидов на первых этапах участвуют ФСГ и ЛГ, ферментные системы – ароматазы. Андрогены синтезируются в тека-клетках под влиянием ЛГ и с током крови попадают в гранулезные клетки. Конечные этапы синтеза (превращения андрогенов в эстрогены) происходят под влиянием ферментов.
В клетках гранулезы образуется белковый гормон – ингибин, тормозящий выделение ФСГ. В фолликулярной жидкости, желтом теле, матке и маточных трубах обнаружен окситоцин. Окситоцин, секретируемый яичником, оказывает лютеолитическое действие, способствуя регрессу желтого тела. Вне беременности в клетках гранулезы и желтого тела очень мало релаксина, а в желтом теле при беременности его содержание возрастает во много раз. Релаксин оказывает токолитическое действие на матку и способствует овуляции.
III уровень – передняя доля гипофиза (аденогипофиз). В аденогипофизе секретируются гонадотропные гормоны: фолликулостимулирующий, или фоллитропин (ФСГ); лютеинизирующий, или лютропин (ЛГ); пролактин (ПрЛ); другие тропные гормоны: тиреотропный гормон, или тиротропин (ТТГ); соматотропный гормон (СТГ); адренокортикотропный гормон, или кортикотропин (АКТГ); меланостимулирующий гормон, или меланотропин (МСГ); липотропный гормон (ЛПГ). ЛГ и ФСГ являются гликопротеидами, ПрЛ – полипептидом.
Железой-мишенью для ЛГ и ФСГ является яичник. ФСГ стимулирует рост фолликула, пролиферацию клеток гранулезы, образование рецепторов ЛГ на поверхности клеток гранулезы. ЛГ стимулирует образование андрогенов в тека-клетках. ЛГ и ФСГ способствуют овуляции. ЛГ стимулирует синтез прогестерона в лютеинизированных клетках гранулезы после овуляции.
Основная роль пролактина – стимуляция роста молочных желез и регуляция лактации. Он оказывает гипотензивное действие, дает жиромобилизующий эффект. Повышение уровня пролактина тормозит развитие фолликулов и стероидогенез в яичниках.
IV уровень репродуктивной системы – гипофизотропная зона гипоталамуса: вентромедиальные, дорсомедиальные и аркуатные ядра. В этих ядрах образуются гипофизотропные гормоны. Выделен, синтезирован и описан рилизинг-гормон – люлиберин. Выделить и синтезировать фоллиберин до настоящего времени не удалось. Поэтому гипоталамические гонадотропные либерины обозначают ГТ-РГ, так как рилизинг-гормон стимулирует выделение как ЛГ, так и ФСГ передней доли гипофиза.
ГТ-РГ гипоталамуса из аркуатных ядер по аксонам нервных клеток попадает в терминальные окончания, тесно соприкасающиеся с капиллярами медиальной возвышенности гипоталамуса. Капилляры формируют портальную кровеносную систему, объединяющую гипоталамус и гипофиз. Особенностью этой системы является возможность тока крови в обе стороны, что важно в осуществлении механизма обратной связи. Нейросекрет гипоталамуса оказывает биологическое действие на организм различными путями.
Основной путь – парагипофизарный – через вены, впадающие в синусы твердой мозговой оболочки, а оттуда в ток крови. Трансгипофизарный путь – через систему воротной вены к передней доле гипофиза. Обратное влияние на гипоталамус (стероидный контроль половых органов) осуществляется через вертебральные артерии. Секреция ГТ-РГ генетически запрограммирована и происходит в определенном пульсирующем ритме с частотой примерно один раз в час. Этот ритм получил название цирхорального (часового). Он формируется в пубертатном возрасте и является показателем зрелости нейросекреторных структур гипоталамуса. Цирхоральная секреция ГТ-РГ запускает гипоталамо-гипофизарно-яичниковую систему. Под влиянием ГТ-РГ происходит выделение ЛГ и ФСГ из передней доли гипофиза.
В модуляции пульсации ГТ-РГ играет роль эстрадиол. Величина выбросов ГТ-РГ в преовуляторный период (на фоне максимального выделения эстрадиола) значительно выше, чем в раннюю фолликулиновую и лютеиновую фазы. Частота выбросов остается прежней. В дофаминергических нейронах аркуатного ядра гипоталамуса есть рецепторы эстрадиола.
Основная роль в регуляции выделения пролактина принадлежит дофаминергическим структурам гипоталамуса. Дофамин (ДА) тормозит выделение пролактина из гипофиза. Антагонисты дофамина усиливают выделение пролактина.
V уровень в регуляции менструального цикла – надгипоталамические церебральные структуры. Воспринимая импульсы из внешней среды и от интерорецепторов, они передают их через систему передатчиков нервных импульсов (нейротрансмиттеров) в нейросекреторные ядра гипоталамуса.
В эксперименте показано, что в регуляции функции гипоталамических нейронов, секретирующих ГТ-РГ, ведущая роль принадлежит дофамину, норадреналину и серотонину. Функцию нейротрансмиттеров выполняют нейропептиды морфиноподобного действия (опиоидные пептиды) – эндорфины (ЭНД) и энкефалины (ЭНК). Они регулируют гонадотропную функцию гипофиза. ЭНД подавляют секрецию ЛГ, а их антагонист – налоксон – приводит к резкому повышению секреции ГТ-РГ. Считают, что эффект опиоидов осуществляется за счет изменения содержания ДА (ЭНД снижают синтез ДА, вследствие чего стимулируется секреция и выделение пролактина).
В регуляции менструального цикла участвует кора большого мозга. Имеются данные об участии амигдалоидных ядер и лимбической системы в нейрогуморальной регуляции менструального цикла. Электрическое раздражение амигдалоидного ядра (в толще больших полушарий) вызывает в эксперименте овуляцию. При стрессовых ситуациях, при перемене климата, ритма работы наблюдаются нарушения овуляции. Нарушения менструального цикла реализуются через изменение синтеза и потребления нейротрансмиттеров в нейронах мозга.
Таким образом, репродуктивная система представляет собой суперсистему, функциональное состояние которой определяется обратной связью входящих в нее подсистем. Регуляция внутри этой системы может идти по длинной петле обратной связи (гормоны яичника – ядра гипоталамуса; гормоны яичника – гипофиз), по короткой петле (передняя доля гипофиза – гипоталамус), по ультракороткой (ГТ-РГ – нервные клетки гипоталамуса). Обратная связь может быть как отрицательной, так и положительной. При низком уровне эстрадиола в раннюю фолликулярную фазу усиливается выделение ЛГ передней долей гипофиза – отрицательная обратная связь. Овуляторный пик выделения эстрадиола вызывает выброс ФСГ и ЛГ – положительная обратная связь. Примером ультракороткой отрицательной связи может служить увеличение секреции ГТ-РГ при снижении его концентрации в нейросекреторных нейронах гипоталамуса.

