 полная версия
полная версияРекомендации ESPEN-ESPGHAN-ECFS по диетотерапии при муковисцидозе у младенцев, детей и взрослых

Коллектив авторов
Рекомендации ESPEN-ESPGHAN-ECFS по диетотерапии при муковисцидозе у младенцев, детей и взрослых
Обоснование. Недостаточность питания часто сопровождает муковисцидоз (MB) и может быть как его признаком, так и сопутствующей патологией. Нутритивный статус пациента тесно связан с функцией легких и выживаемостью, поэтому диетотерапия входит в стандарт лечения MB. Рекомендации ESPEN, ESPGHAN и ECFS посвящены различным аспектам диетотерапии при MB.
Методы. Настоящие рекомендации разработаны международной междисциплинарной рабочей группой в соответствии с официально утвержденными стандартами. Уровень доказательности и сила рекомендаций определялись с помощью системы GRADE. Все утверждения обсуждались и экспертные оценки обрабатывались с помощью метода согласования «Дельфи» (Delphi). Затем утверждения рассматривались ESPGHAN и ECFS. Окончательное решение об утверждении рекомендации принимали члены ESPEN с помощью интернет-голосования.
Результаты. Рабочая группа рекомендует начинать диетотерапию как можно раньше после установления диагноза, с последующим регулярным наблюдением и обучением пациента/родственников. Оптимальным питанием для младенцев считается исключительно грудное вскармливание; если оно невозможно, рекомендуется стандартная молочная смесь для искусственного вскармливания. Потребление энергии должно быть адаптировано так, чтобы достигнуть нормальных (для соответствующего возраста) показателей массы тела и роста. В ряде случаев показано раннее начало заместительной терапии панкреатическими ферментами и витаминотерапии, с последующим регулярным контролем. При сохранной функции поджелудочной железы рекомендуется ежегодная оценка ее состояния по содержанию панкреатической эластазы в кале. Рекомендуется дополнительное потребление натрия и оценка соотношения натрий-кереатинин в моче, в соответствии с фракционной экскрецией натрия. При подозрении на дефицит железа необходимо исключить фоновый воспалительный процесс. У пациентов старше 10 лет необходимо оценивать толерантность к глюкозе. Минеральную плотность костей оценивают у пациентов старше 8-10 лет. При нарушении физического развития или низком нутритивном статусе сначала рекомендуются пероральные добавки к пище, затем – зондовое энтеральное питание полимерными смесями. В ряде случаев показано дополнительное введение цинка. Препараты полинасыщенных жирных кислот, средства для лечения остеопороза, препараты гормона роста, стимуляторы аппетита и пробиотики не рекомендуются, до проведения дополнительных исследований.
Заключение. Диетотерапия и нутритивная поддержка должны быть неотъемлемым компонентом лечения MB. Обеспечивать нормальное физическое развитие детей и поддерживать удовлетворительный нутритивный статус взрослых— основные цели междисциплинарных центров по лечению муковисцидоза.
1. Введение
1.1 Разработка рекомендаций по диетотерапии при муковисцидозе
Разработка обновленных рекомендаций по питанию и нутритивной поддержке больных муковисцидозом (младенцев, детей и взрослых) была начата Европейской ассоциацией клинического питания и метаболизма (European Society for Clinical Nutrition and Metabolism, ESPEN). В рабочую группу входили врачи, диетологи, педагоги, обладающие экспертными знаниями в области муковисцидоза, а также координатор (SMS); все они являются авторами настоящих рекомендаций.
Последние Кокрейновские систематические обзоры показали, что рандомизированных контролируемых исследований, посвященных эффектам диетотерапии при MB, недостаточно[1][2][3][4][5][6][7][8]. Поэтому многие клинические руководства по нутритивной поддержке основаны на согласованных мнениях экспертов[9][10][11]. При составлении рекомендаций эксперты использовали систему GRADE, позволяющую определить уровень доказательности и силу рекомендации; методические принципы описаны в отдельном документе[12]. В апреле 2012 года была проведена встреча в Стокгольме (Швеция). Настоящие рекомендации представляют собой обновление Единых европейских рекомендаций по питанию для больных муковисцидозом[13].
Поиск литературы осуществлялся в базе данных Pub Med, а также в Кокрейновской библиотеке (публикации до 2014 года). Использовался следующий поисковый запрос: cystic fibrosis AND (nutrition* OR diet* OR nourishment OR nutrient OR nutriment OR malnutrition OR malnourishment OR undernourishment OR calorie* OR lipid* OR trace OR vitamin* OR protein* OR taurine OR pancreatic enzyme replacement therapy OR PERT OR fatty OR micronutrient* OR antioxidant* OR probiotic* OR supplement* OR insulin OR enteral OR parenteral OR EN OR TPN OR PN).
Уровень доказательности определялся с помощью ряда факторов, в частности, по количеству и типу научных исследований[14][15][16][17][18]. Качество доказательств, на которых основана рекомендация и уровень достоверности эффекта оценивались от высокого до очень низкого (Таблица 1)[19]. Доказательства, основанные на достоверных результатах мета-анализа большого числа рандомизированных контролируемых исследований, считались доказательствами высшего качества. Следующий уровень качества присваивался доказательствам, основанным на результатах как минимум одного хорошо спланированного рандомизированного контролируемого исследования. Доказательства среднего и низкого уровня качества были получены в ходе контролируемых исследований, проведенных без рандомизации, в когортных исследованиях или исследованиях типа «случай-контроль», а также в нескольких исследованиях серии случаев. Доказательства, основанные на клиническом опыте экспертов или полученные в описательных исследованиях, считались доказательствами очень низкого качества. При наличии ограничений, связанных с качеством исследования, а также противоречивых результатов, неточностей в данных или попусков данных, или же при высокой вероятности систематических ошибок сообщения информации уровень доказанности понижался. Постоянство и согласованность результатов или убедительные доказательства, подтверждающие наличие связи, приводили к повышению уровня доказанности (Таблица 1).

Сила рекомендации определялась по результатам общего обсуждения, в ходе которого высказывались и обсуждались мнения экспертов, оценивалось соотношение пользы и риска для рекомендации, а также связанные с ней затраты. Также рассматривались подтверждающие данные, после чего применялся метод согласования «Дельфи» (Delphi) и проводилось голосование. Обсуждение рекомендации продолжалось до тех пор, пока не достигалось соглашение (Таблица 2).

Наконец, полный список утверждений был разослан всем членам ESPEN (2639 человек) по электронной почте в виде файла; письмо сопровождалось просьбой подтвердить каждое утверждение или отклонить его (в последнем случае необходимо было дать обоснование). Упомянутый файл заполнили 50 членов ESPEN, доля одобренных утверждений составила от 61 до 100 %. Комментарии, основанные на литературных источниках, были учтены в итоговой версии рукописи. Европейскому обществу специалистов в области детской гастроэнтерологии, гепатологии и питания (ESPGHAN) и Европейскому обществу специалистов в области муковисцидоза (ECFS) – соавторам данных рекомендаций – для оценки была предоставлена итоговая версия рукописи; для ESPGHAN производилась внешняя оценка.
Следует отметить, что данный проект основывался на правилах для рекомендаций ESPEN[20], тогда как ESPGHAN и ECFS, придерживающиеся собственных правил, отнесли данный проект к установочным документам.
1.2 Потребности в питательных веществах при муковисцидозе
1.2.1 Описание проблемы: муковисцидоз и недостаточное питание
Муковисцидоз (MB) – угрожающее жизни генетически-обусловленное заболевание. MB распространен преимущественно среди представителей европеоидной расы, однако может встречаться и у представителей других рас или этнических групп[21][22]. В Европе уровень заболеваемости MB составляет 1 на 3500 новорожденных европеоидной расы[23]. Средняя распространенность MB в США и странах Европейского союза идентична и составляет 0,74 и 0,80 на 10000 населения соответственно[24].
Характерный для MB фенотип обусловлен мутациями в гене, кодирующем белок CFTR (МВТР) (Муковисцидозный белок-регулятор – МВТР). Результат этих мутаций – дефицит или дисфункция белка CFTR, который нарушает транспорт ионов натрия и хлора через мембрану различных клеток, в том числе эпителиальных[25][26]. Как следствие, изменяется транспорт жидкостей, и слизистые секреты становятся более вязкими. В результате нарушается функция легких и поджелудочной железы, а также печени, желчного пузыря и кишечника[27][28]. В легких вязкая слизь «приклеивается» к поверхности дыхательных путей, что ухудшает мукоцилиарный клиренс и увеличивает риск воспаления и инфекции. Вязкий секрет поджелудочной железы закупоривает ее внутренние протоки, что затрудняет поступление пищеварительных ферментов в тонкую кишку и нарушает всасывание питательных веществ[29].
Муковисцидоз связан с низким нутритивным статусом как напрямую (факторы, обусловленные мутациями, лежащими в основе заболевания), так и косвенно (высокие энергетические потребности, потери энергии, ускоренный обмен незаменимых жирных кислот [НЖК], а также сниженное потребление и нарушенное всасывание питательных веществ)[30][31][32][33][34]. У детей низкий нутритивный статус приводит к задержке роста и развития[35]. У детей и взрослых с MB ухудшение функции легких связано со снижением нутритивного статуса, что сопровождается увеличением смертности[36][37]. С другой стороны, между хорошим нутритивным статусом и улучшением функции легких тоже есть непосредственная связь; в результате клинические исходы становятся благоприятнее, а выживаемость повышается[38][39][40]. Хотя за последние двадцать лет нутритивный статус пациентов с MB значительно улучшился, в некоторых случаях оптимальное питание все еще не налажено[41]. Ранее начало лечения (например, если диагноз MB устанавливается при скрининге новорожденных) имеет ряд преимуществ. Так, оно дает возможность минимизировать дефицит питательных веществ и сопровождается улучшением нутритивного статуса.
1.2.2 Активная тактика
Чтобы максимально улучшить исход заболевания, для каждого пациента с MB, в ходе лечения необходимо уделять внимание диетотерапии. Для этого группа экспертов, представленная ESPEN, ESPGHAN и ECFS, систематически анализирует медицинскую литературу и обобщает современные данные об эпидемиологии, патофизиологии, профилактике и лечению недостаточности питания, связанной с MB. Группа ESPEN-ESPGHAN-ECFS рекомендует придерживаться основанных на доказательствах рекомендаций, посвященных питанию и нутритивной поддержке больных муковисцидозом (младенцев, детей и взрослых).
1.3 Причины недостаточности питания при MB
Недостаточность питания при MB возникает из-за несоответствия между энергетическими потребностями и фактическим потреблением пищи; кроме того, она осложняется мальабсорбцией. На сегодняшний день стандартом диетотерапии при MB является высококалорийная диета с высоким содержанием жиров в сочетании с заместительной терапией панкреатическими ферментами (ЗТПФ) и приемом жирорастворимых витаминов[42]. Согласно последним исследованиям, также необходимы рекомендации по увеличенному потреблению белков, чтобы поддерживать безжировую массу тела и улучшить долгосрочные исходы заболевания[43]. Аналогичные данные есть и для НЖК: предполагается, что увеличенное потребление НЖК (например, линолевой кислоты) может улучшить выживаемость и физическое развитие[44].
1.3.1 Стандартная характеристика достаточного питания при MB
Питание младенцев и детей, страдающих MB, считается достаточным, если их показатели физического развития не отличаются от нормативных значений для здоровых сверстников. Для взрослых, страдающих MB, «пороговой величиной» является целевое значение индекса массы тела (ИМТ), рассчитанное отдельно для женщин и мужчин[45].
Тем не менее, целевых значений ИМТ недостаточно для полноценной характеристики нутритивного статуса старших детей и взрослых с MB. Engelen и соавторы указывают на все более высокую распространенность избыточного веса и ожирения – факторов, затрудняющих оценку нутритивного статуса[46][47]. Другими словами, увеличение массы тела не обязательно коррелирует с улучшением функции легких; на самом деле высокая жировая масса (но, соответственно, низкая безжировая масса тела) ухудшает прогноз MB. Таким образом, в будущих рекомендациях по питанию при MB необходимо соотнести пороговые значения ИМТ, характеризующие достаточное питание, с пороговыми значения безжировой массы тела.
1.3.2 Распространенность недостаточности питания при MB
Несмотря на то, что все больше пациентов с MB достигают удовлетворительного нутритивного статуса, недостаточность питания по-прежнему встречается. В соответствии с последним регистром пациентов ECFS (данные 2010 года)[48], в большинстве европейских стран практически половина всех детей и взрослых с MB соответствуют критериям достаточного питания. Однако это означает, что около половины пациентов не достигли удовлетворительного нутритивного статуса. Аналогичные тенденции наблюдаются и в США, где медиана возрастного ИМТ (по шкале процентилей) у детей с MB увеличилась с 41,0 в 2001 г. до 51,3 в 2011 г., а медиана ИМТ для взрослых с MB увеличилась с 21,2 до 22,1 кг/м2 (нормальные значения для здоровых взрослых составляют от 18,5 до 25)[49]. При этом по данным на 2005 год, представленным в отчете по регистру пациентов Фонда муковисцидоза США (CFFoundationPatientRegistryReport), приблизительно четверть детей находились ниже 10-го процентиля (масса тела в соответствии с возрастом и полом), и 22 % взрослых в возрасте 18–30 лет имели недостаточную массу тела[50].
1.3.3 Причины недостаточного питания
При MB к недостаточному питанию приводит комплекс причин: потери энергии, высокие энергетические потребности и нарушенное поступление питательных веществ[51]. Основная причина потери энергии— мальабсорбция, которая часто является следствием нарушенного пищеварения. В свою очередь, нарушенное пищеварение обусловлено недостаточным поступлением панкреатических ферментов в просвет кишечника (недостаточность экзокринной функции поджелудочной железы)[52]. В случаях, когда нарушения пищеварения сопровождаются метаболическими изменениями, потери энергии усугубляются. Примерами таких состояний могут быть воспалительный процесс в кишечнике, избыточный рост бактерий в тонкой кишке, недостаточная секреция бикарбоната, нарушенная секреция инсулина в сочетании с инсулинорезистентностью различной степени (сахарный диабет, ассоциированный с MB)[53] и нарушение функции печени (заболевание печени, ассоциированное с с MB)[54][55].
Более того, энергетические потребности у пациентов, страдающих MB и панкреатической недостаточностью, выше, чем энергетические потребности здоровых людей. Ряд измерений подтверждают это: так, у пациентов с MB отмечается более высокий расход энергииосновного обмена[56]. Такие показатели существенно коррелируют с панкреатической недостаточностью, хотя механизм этой взаимосвязи остается неясным[57]. Также высокие энергетические потребности можно объяснить хроническим воспалительным процессом в легких и инфекциями, которые сопровождают MB[58][59][60].
Потребление энергии у пациентов с MB, в особенности детей и подростков, часто недостаточно для компенсации дефицитов, возникающих из-за неэффективного энергообмена и повышенных энергетических потребностей. Психосоциальные аспекты, такие как стресс и невыполнение медицинских рекомендаций, могут усугублять энергетический дефицит[61]. Снижать аппетит и затруднять поступление питательных веществ могут и другие дополнительные факторы: воспалительные процессы в легких; дискомфорт, связанный с нарушениями работы желудочного-кишечного тракта (гастроэзофагеальный рефлюкс, запор, синдром дистальной интестинальной обструкции, избыточный рост бактерий); побочные эффекты лекарственных препаратов[62][63][64].
1.3.4 Каковы последствия недостаточного питания?
Недостаточное питание влияет на функцию дыхательной мускулатуры, снижает толерантность к физическим нагрузкам и ухудшает функцию иммунной системы[65]. В то время как патофизиология MB напрямую связана с низким потреблением энергии, по сравнению с энергетическими потребностями, существуют и другие патофизиологические механизмы, за счет которых при MB поражаются различные органы таким образом, что функции легких ухудшаются, нарушение физического развития усугубляется, качество жизни снижается, продолжительность жизни сокращается[66]. У младенцев и детей младшего возраста, страдающих MB, низкий нутритивный статус приводит к задержке роста. Это подтверждается низкими возрастными показателями массы тела и роста по шкале процентилей[67][68][69]. Без лечения такая недостаточность питания, связанная с MB и возникшая в раннем детстве, может привести к серьезным последствиям – например, нарушениям когнитивной функции[70]. Тяжелая недостаточность питания в младенческом и детском возрасте характеризуется значительным ухудшением функции легких[71] и низкой выживаемостью[72].
По мере прогрессирования MB у детей старшего возраста и взрослых возникают различные метаболические осложнения, которые приводят к дефициту питательных веществ. Это, в свою очередь, еще сильнее ухудшает качество жизни[73] и увеличивает риск смерти[74]. Например, ассоциированный с MB сахарный диабет (недостаток инсулина и/или инсулинорезистентность) провоцирует и усиливает недостаточность питания за счет уменьшения анаболических эффектов инсулина[75][76][77]. Аналогично, ассоциированное с MB поражение печени или стеатоз печени связаны с отдельными видами дефицита питательных веществ – например, жирорастворимых витаминов, НЖК и кальция[78][79][80]. Это ухудшает недостаточность питания в целом и вносит свой вклад в другие нарушения, такие как остеопения и остеопороз[81][82][83].
Таким образом, неблагоприятные последствия недостаточности отдельных питательных веществ у пациентов с MB – младенцев, детей и взрослых – многообразны и весь комплекс таких последствий является основанием для ранней и агрессивной диетотерапии, которая должна начинаться в раннем детском возрасте и продолжаться пожизненно[84][85].
1.4. Общие рекомендации по диетотерапии при муковисцидозе
В настоящем документе даны шесть основных рекомендаций по скринингу и оценке недостаточности питания, а также по диетотерапии при муковисцидозе (Таблица 3). Дополнительные исследования и усиление доказательной базы необходимы для многих рекомендаций; тем не менее, мы призываем исследователей уделить особое внимание изучению новых способов коррекции нарушений, связанных с питанием при MB. В первую очередь к этим способам относятся препараты жирных кислот, препараты для лечения остеопороза, противовоспалительные препараты, анаболические средства и пробиотики.

2. Систематический подход к оценке и мониторингу нутритивного статуса при МВ
Вне зависимости от возраста пациентов, муковисцидоз сопровождается риском недостаточности питания; таким образом, для улучшения исходов заболевания необходимы регулярные и детальные оценки нутритивного статуса. В случаях, когда диагноз MB установлен при неонатальном скрининге, диетотерапия позволяет поддерживать нормальные показатели физического развития даже до того, как проявляется характерный для MB фенотип[86][87][88].
В этом разделе обсуждаются методы, которое позволяют выявить маркеры низкого нутритивного статуса (Таблица 4). Как было сказано выше, традиционно низкий нутритивный статус диагностировали с помощью нормативных антропометрических показателей: масса и длина тела (возрастные показатели по шкале процентилей) у младенцев и детей младше 2 лет[89][90], ИМТ у детей старше 2 лет и взрослых[91]. Международные нормы роста и массы тела или ссылки на соответствующие источники доступны на сайте Всемирной организации здравоохранения (ВОЗ)[92]. Кроме того, низкий нутритивный статус сопровождается ухудшением функции легких и панкреатической недостаточностью. Для оценки и контроля нутритивного статуса можно использовать сывороточные маркеры и анализ состава тела.
2.1 Оценка физического развития и ИМТ в зависимости от возраста
Питание младенцев и детей, страдающих MB, считается достаточным, если их показатели физического развития не отличаются от нормативных показателей для популяции здоровых сверстников (Таблица 4). В идеале таблицы физического развития должны быть скорректированы в соответствии с национальной и этнической принадлежностью пациента. Если такая коррекция невозможна, следует использовать стандарты физического развития ВОЗ (www.who.int/childgrowth/standards/en/). Для младенцев и детей младшего возраста цель – достичь к двум годам жизни показателей массы и длины тела, соответствующих 50-му процентилю здоровой популяции сверстников. Для детей старшего возраста и подростков (от 2 до 18 лет) целевым показателем является индекс массы тела (ИМТ), соответствующий как минимум 50-му процентилю здоровой популяции. Для взрослых (старше 18 лет) пациентов с MB целевые значения ИМТ составляют > 22 кг/м2[93] для женщин и > 23 кг/м2[94] для мужчин.
2.2 Оценка нутритивного статуса и функций, связанных с питанием
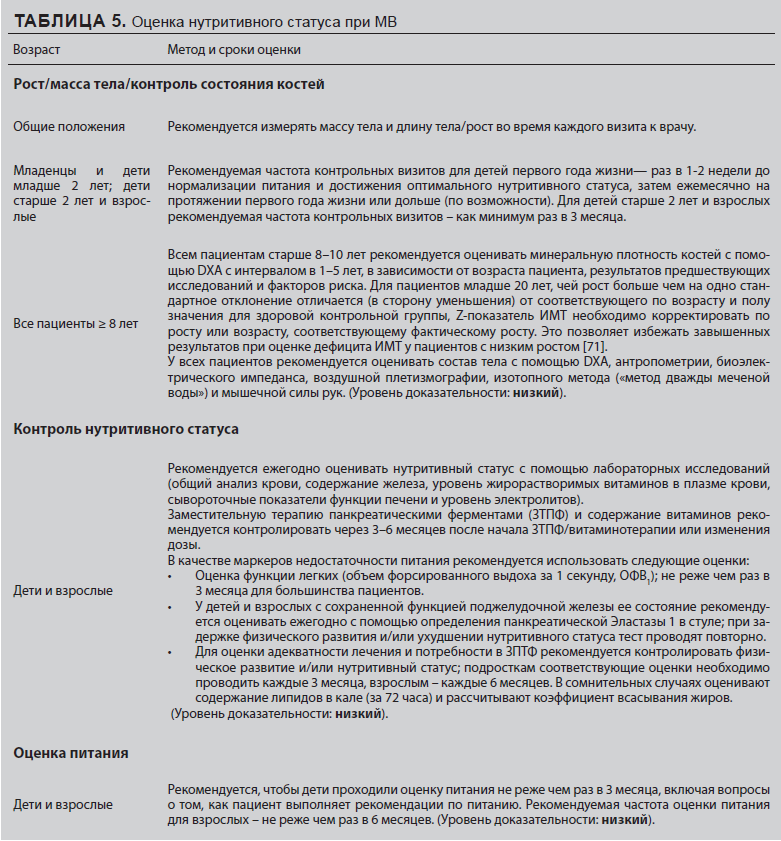
В этом разделе даны рекомендации по контролю нутритивного статуса и срокам его оценки (Таблица 5).
2.2.1 Сывороточные маркеры, характеризующие нутритивный статус
К факторам риска и биохимическим маркерам, характеризующим нутритивный статус, относятся общий анализ крови, содержание железа, уровень жирорастворимых витаминов в плазме крови, сывороточные показатели функции печени и уровень электролитов[95][96][97][98][99]. Также можно контролировать уровень фосфолипидов в плазме крови или содержание жирных кислот в эритроцитах, если соответствующие исследования доступны[100][101].
2.2.2 Состав тела
Состав тела можно оценить с помощью различных методов: двухэнергетическая рентгеновская абсорбциометрия (DXA), антропометрия, биоимпеданс, воздушная плетизмография, изотопный метод («метод дважды меченой воды») и оценка силы захвата кисти. Однако не все перечисленные методы сертифицированы для MB. Безжировая масса тела (БМТ) и степень минерализации костей (СМК) являются более чувствительными индикаторами дефицита питательных веществ, чем ИМТ; низкие значения этих показателей – предикторы нарушения функции легких как у детей[102], так и взрослых с MB[103][104]. Согласно Европейским рекомендациям по минерализации костей при муковисцидозе, всем пациентам старше 8-10 лет показано проведение DXA (денситометрии) для оценки минеральной плотности костей[105]. DXA рекомендуется проводить с интервалом в 1–5 лет, в зависимости от возраста пациента, результатов предшествующих исследований и факторов риска (например, отсутствие физической активности, терапия глюкокортикоидами)[106][107]. Для пациентов младше 20 лет, чей рост больше чем на одно стандартное отклонение отличается (в сторону уменьшения) от соответствующего по возрасту и полу значения для здоровой контрольной группы, Z-показатель ИМТ необходимо корректировать по росту или возрасту, соответствующему фактическому росту. Это позволяет избежать завышенных результатов при оценке дефицита ИМТ у пациентов с низким ростом[108].
2.2.3 Электролиты
Контроль содержания натрия в соответствии с рекомендациями из раздела 2с.
2.2.4 Анализ питания
Анализ питания необходим пациентам из группы риска нутритивной недостаточности, особенно детям школьного возраста, которые могут пропускать основные или дополнительные приемы пищи (например, из-за школьных занятий). Удобным инструментом для качественной оценки является анализ суточного фактического питания. Для количественной оценки потребления энергии и питательных веществ может потребоваться более длительный анализ фактического питания – например, за 3–5 дней[109]. Поскольку достаточное и полноценное питание при MB крайне важно, рекомендуется, чтобы дети младшего возраста и подростки проходили оценку питания не реже чем раз в 3 месяца[110][111], а взрослые – не реже чем раз в 6 месяцев, включая вопросы о том, как пациент выполняет рекомендации по питанию.









