
Полная версия
Тропические и паразитарные болезни
У беременных женщин это заболевание протекает исключительно тяжело. На фоне геморрагического синдрома при лихорадке Эбола у них бывают самопроизвольные аборты, преждевременные роды. У мужчин поражение сосудов мошонки может приводить к развитию орхита.
При выздоровлении отмечается длительная реконвалесценция с астенией, выпадение волос и др. Летальность при лихорадке Марбург составляет 20–22 %, при лихорадке Эбола – до 90 % (во время вспышки 2014 г. – около 55 %).
Диагностику следует проводить с брюшным тифом, малярией, лептоспирозом, риккетсиозами, возвратным тифом, менингитами, другими ГЛ. Диагноз подтверждается вирусологически и серологически. Материал от пациентов (кровь, мочу, носоглоточную слизь и др.) вносят в культуру клеток Vero или морским свинкам. Идентификация вируса проводится в РИФ, ИФА, ПЦР. Эти методы также применимы и для прямого обнаружения вирусов в исследуемом материале. Антитела обнаруживают путем непрямой иммунофлюоресценции; диагностический титр 1: 64.
Лечение симптоматическое, патогенетическое, в том числе регидратация, коррекция солевого баланса и др. Показано введение плазмы реконвалесцентов и интерферона.
Прогноз при геморрагической лихорадке Марбург неблагоприятный, летальность достигает 30 %. Прогноз при лихорадке Эбола тяжелый, летальность превышает 50 %.
Профилактика. Для предупреждения вторичных заражений в семье необходима срочная госпитализация больных; в стационарах – размещение пациентов в стационарных или переносных изоляторах, защитная одежда персонала (защитные лицевые экраны, маски или респираторы), дезинфекция выделений пациентов, профилактика парентеральных заражений.
Специфическая профилактика лихорадки Эбола до 2014 г. не применялась, разработана вакцина, которая проходит фазу клинических испытаний.
Арбовирусные болезни
Арбовирусные болезни – многочисленная группа трансмиссивных зоонозов. Протекают с общетоксическим синдромом, поражением ЦНС, геморрагическим синдромом и нарушением функции различных внутренних органов.
К группе арбовирусных относятся те заболевания, которые передаются с помощью членистоногих. Термин «арбовирусы» был признан официальным в 1963 г. ВОЗ. Дословно он расшифровывается как «вирусы, передающиеся членистоногими» (англ, «arthropod borne viruses»). Актуальность изучения этих заболеваний определяется, прежде всего, высокой потенциальной эпидемичностью арбовирусных лихорадок, необычайно высокой летальностью при некоторых заболеваниях, достигающей иногда 80 % и более, трудностями в диагностике, лечении и профилактике.
Возбудители болезней – арбовирусы – экологическая группа РНК-содержащих вирусов. Число открываемых арбовирусов непрерывно растет. Вследствие комплекса геобиоценологических условий арбовирусные болезни наиболее распространены в странах с тропическим климатом, однако встречаются и в умеренных климатических зонах. Они были обнаружены практически во всех географических зонах, за исключением полярных регионов.
Арбовирусные инфекции у позвоночных протекают, как правило, бессимптомно. Вирусемия стимулирует иммунный ответ организма, который резко ограничивает ее продолжительность. При арбовирусных инфекциях, отличных от городской желтой лихорадки, лихорадки денге, флеботомной лихорадки, от инфекций, вызываемых вирусами чикунгунья, о’нъонг-нъонг, Майяро, оропуш, а возможно, и вирусом Росс-Ривер, инфекция у человека представляет собой случайное событие, связанное лишь с основным жизненным циклом вируса. Следовательно, выделение вируса у насекомого-переносчика или выявление заболевания у естественного хозяина (позвоночного животного) может быть средством раннего обнаружения вируса, что позволяет контролировать эпизоотическую обстановку.
Большинство арбовирусных инфекций человека протекает бессимптомно. Если заболевание возникает, то клиническая картина в различных случаях варьирует как по признаку преобладающего синдрома, так и по тяжести его выраженности. Чаще всего заболевание оканчивается самостоятельно и характеризуется лихорадкой, головной болью, недомоганием, миалгией. Как самостоятельный симптом может выступать сопутствующая лимфаденопатия.
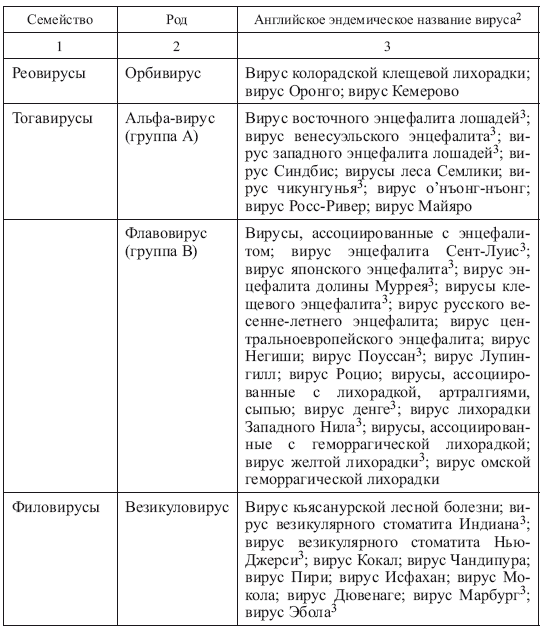
В зависимости от преобладания клинико-патогенетического синдрома различают арбовирусные системные лихорадочные болезни, геморрагические лихорадки, энцефалиты и энцефаломиелиты. Более 250 антигенно различных арбовирусов сгруппированы в пять семейств (табл. 2). Геном большинства вирусов представлен односпиральный РНК, хотя некоторые из них (представители семейства Reoviridae) содержат двуспиральную РНК.
Таблица 2.
Таксономическая категория экологической группы арбовирусов[1]

Флеботомная лихорадка
Флеботомная лихорадка – острая вирусная эндемическая болезнь. Проявляется кратковременной лихорадкой, миалгиями, характерным конъюнктивитом, поражением нервной системы и нередко экзантемой.
Синонимы: москитная лихорадка, лихорадка паппатачи.
Этиология. Возбудители флеботомной лихорадки относятся к роду Phlebovirus семейства Bunyaviridae. Из 23 описанных видов этого рода у людей выделены 6 (Napoli, Sicilian, Chag-ress, Candiru, Punto-Toro, Rift-Valley). Типовым вирусом является вирус сицилийской флеботомной лихорадки. К вирусам чувствительны некоторые лабораторные животные; у новорожденных белых мышей они вызывают летальную инфекцию.
Эпидемиология. Флеботомная лихорадка – зоонозная трансмиссивная эндемическая болезнь, склонная к эпидемическому распространению.
Основным резервуаром вирусов считаются москиты, у которых возможна трансовариальная передача возбудителей. Самки москитов становятся способными к передаче вируса чувствительным организмам спустя 6–8 дней после инфицирующего кровососания. Больные люди становятся источниками возбудителей в конце инкубационного и в лихорадочном периоде. Возможна парентеральная передача вирусов некачественно обработанными медицинскими инструментами. В тропической и субтропической зонах заболеваемость флеботомной лихорадкой имеет двухволновой характер соответственно лету москитов.
Восприимчивость к флеботомной лихорадке всеобщая. В эндемических очагах болеют преимущественно дети и приезжие лица. У взрослых коренных жителей формируется гомологичный иммунитет, у определенной части которых возможны повторные заболевания, связанные с дефектами иммуногенеза или заражением гетерологичным вариантом вируса. Среди приезжих лиц могут возникать эпидемические вспышки болезни, особенно в период военных действий.
Географическое распространение. Нозоареал флеботомной лихорадки соответствует ареалу москитов и захватывает районы, расположенные от 20 до 45 с. ш. (Средиземноморье, Средний и Ближний Восток, Центральная и Южная Азия, Центральная и Южная Америка).
Патогенез. Проникший при укусе москита в организм человека вирус размножается в клетках системы мононуклеарных фагоцитов (СМФ) в течение 3–7 дней, затем выходит в кровь, обусловливая клиническое проявление инфекционного процесса. Обладая определенной нейро- и вазотропностью, вирус фиксируется в клетках ЦНС, симпатическом отделе вегетативной нервной системы, вызывая нарушение их функции, явления церебральной гипертензии. Наблюдается поражение мелких сосудов, скелетной мускулатуры. Фиксация вируса в костном мозге приводит к лейкопении с относительным лимфомоноцитозом. Изменения внутренних органов изучены мало ввиду доброкачественного течения болезни, редко заканчивающегося смертью. Циркуляция вируса стимулирует выработку антител, формирование иммунитета к нему Известны случаи повторных заболеваний в течение одного эпидемического сезона.
Клиническая картина. Инкубационный период флеботомной лихорадки продолжается 3–7 дней.
Стадия разгара. Заболевание развивается остро, часто внезапно. У больных появляется озноб, в течение первых суток повышается температура тела до 39–40 °C и остается повышенной в течение 2–3, а иногда 4–5 дней. Пациенты жалуются на интенсивную головную боль, распространенные мышечные и суставные боли. Особенно интенсивны они в поясничных и икроножных мышцах. Характерны боли в области глазных яблок, в глазницах, надбровной области.
При осмотре пациента определяются одутловатость и гиперемия лица, шеи, верхней части груди, напоминающая «солнечную эритему». Обычно присутствуют конъюнктивит, фотофобия. Патогномоничным симптомом считается симптом Тауссига, заключающийся в резкой болезненности, появляющейся при надавливании на глазные яблоки, а также при их движении или при попытке поднять веко. Почти всегда у пациентов с флеботомной лихорадкой отмечается ограниченная инъекция сосудов наружного (или внутреннего) угла склер в виде треугольника, обращенного вершиной к радужной оболочке, – симптом Пика. На открытых участках кожи видны следы укуса москитов в виде папул, окруженных венчиком гиперемии. При загрязнении места укусов могут нагнаиваться.
На 2-3-й день болезни иногда наблюдается экзантема: мелкопапулезная, кореподобная, уртикарная или эритематозная, исчезающая без следа после снижения температуры тела. Возможно появление простого герпеса. Часто выявляются гиперемия зева, отечность нёбного язычка, редко с точечными геморрагиями.
Больным флеботомной лихорадкой в течение первых суток свойственна тахикардия, которая на 2-4-й день сменяется относительной или абсолютной брадикардией, сохраняющейся в течение 10–15 дней апирексии. Артериальное давление обычно понижено. Язык, как правило, сухой, обложен белым налетом. Живот безболезненный. Размеры печени и селезенки не изменены.
С первых дней болезни выявляются признаки поражения нервной системы в виде головной боли, гиперестезии, лабильности вегетативной нервной системы, нередко менингеальных симптомов, в тяжелых случаях болезни возможны бред, потеря сознания.
Гемограмма в начальном периоде болезни характеризуется лейкопенией с постепенным нарастанием количества лимфоцитов и моноцитов, анэозинофилией, нейтропенией с преобладанием молодых элементов. Скорость оседания эритроцитов (СОЭ) не изменяется. Спинномозговая пункция выявляет повышение внутричерепного давления, в цереброспинальной жидкости увеличено количество белка и положительны пробы Панди и Нонне – Апельта.
В анализах мочи обнаруживается преходящая протеинурия. На 3-4-й день болезни температура критически снижается до нормальной или субнормальной, что сопровождается выраженной потливостью, некоторым улучшением самочувствия, уменьшением болевого синдрома. Заболевание переходит в стадию реконвалесценции.
Период выздоровления. При флеботомной лихорадке продолжается от нескольких дней до 2–3 недель и характеризуется выраженной астенизацией больных, часто психической депрессией, невралгиями, повышенной потливостью. В этой стадии могут выявляться брадикардия, артериальная гипотензия, изредка отмечается кратковременное повышение температуры тела. Иногда наблюдаются повышение давления цереброспинальной жидкости и увеличение в ней содержания альбумина, в периферической крови могут сохраняться лейкопения, анэозинофилия и относительный лимфомоноцитоз. У некоторых пациентов возможны разнообразные симптомы поражения системы органов дыхания, желудочно-кишечного тракта (ЖКТ), обусловленные, как правило, обострением хронических заболеваний или присоединением ассоциированной инфекции.
Диагностика. Диагноз болезни устанавливают на основании комплекса эпидемиологических и клинико-лабораторных данных, верифицируют выделением вируса из крови в лихорадочный период болезни или обнаружением антител в ИФА, РТГА и PH в парных сыворотках крови, начиная с 5-6-го дня болезни.
Дифференциальный диагноз флеботомной лихорадки проводят с малярией, гриппом, клещевыми боррелиозами, лептоспирозом, риккетсиозами, другими арбовирусными болезнями.
Лечение, Пациентам с флеботомной лихорадкой назначают патогенетические и симптоматические средства. В начальном периоде болезни показаны щадящая диета, постельный режим, анальгетические препараты, сосудистые аналептики. В случаях выраженной церебральной гипертензии необходимы лечебная спинномозговая пункция, применение диуретических препаратов. Выписка пациентов проводится на 14-21-й день болезни. В стационарах проводят комплекс противомоскитных мероприятий.
Прогноз, Благоприятный, летальные исходы наблюдаются редко.
Профилактика, Предупреждение флеботомной лихорадки осуществляют путем уничтожения москитов и мест их выплода, защиты людей от их нападения, а также создания невосприимчивости населения к вирусу через вакцинацию. Используют скарификационный метод введения формализованной или сухой вакцины.
Японский энцефалит
Японский энцефалит – вирусная трансмиссивная эндемичная болезнь. Характеризуется развитием тяжелого менингоэнцефалита, общетоксического синдрома с высокой лихорадкой, отличается чрезвычайной летальностью.
Японский энцефалит – одно из относительно новых вирусных заболеваний, впервые выявлено в 1924 г. в Японии. Японский энцефалит (ЯЭ) является серьезной проблемой здравоохранения во многих странах мира, в частности Азии, так как заболеваемость этой инфекцией колеблется от десятков до тысяч на 100 000 населения, а летальность достигает 20–25 % и более. Примерно в 30 % случаев заболевание завершается нейропсихическими осложнениями. Официально регистрируемая заболеваемость далеко не полностью отражает истинную распространенность инфекции из-за большого количества стертых и бессимптомных форм.
Этиология, Возбудитель японского энцефалита, выделенный в 1934 г., относится к семейству флавовирусов, содержит в своем геноме РНК. Характеризуется малыми размерами (15–20 мкм), антигенными подтипами (Накаяма и Джагар-01), выраженной изменчивостью по признаку вирулентности и иммуногенности, слабой устойчивостью к факторам внешней среды. Быстро инактивируется при нагревании, применении дезинфектантов, ультрафиолетового облучения (УФО). В организме переносчиков может сохраняться до 6 мес.
Эпидемиология. Источники инфекции в природе – птицы (воробьи, цапли, фазаны, бакланы и др.), которые инфицируют комаров и в ряде случаев иксодовых клещей, паразитирующих на морских птицах. Циркуляция вируса в пределах одного вида комаров может происходить трансовариально. Занос инфекции на ту или иную территорию осуществляется перелетными птицами, а комары Culex tritaeniorhynchus, С. pipiens, С. togoi обеспечивают передачу другим пернатым, свиньям, домашним животным (лошадям, буйволам), у которых развивается вирусоносительство и бессимптомная инфекция, достаточная для инфицирования комаров иных видов.
Заражение человека происходит при укусе комаров (инокуляция со слюной) летом в период с мая по сентябрь, а в некоторых странах тропического пояса и круглогодично.
Географическое распространение. Заболевание встречается в Японии, Китае, Индии, Корее, Непале, Таиланде, Вьетнаме, Бангладеш, на Тайване, Филиппинах, в Малайзии, а также в Приморском крае России (рис. 3).
Восприимчивость людей считается высокой. Первое заражение вирусом обычно происходит в детстве, поэтому дети считаются наиболее восприимчивыми и чаще поражаются клинически выраженными формами. У взрослых заражение может приводить к носительству вируса, соотношение больных и носителей в очагах составляет 1: 200-1: 1000. В странах, где дети иммунизируются, как правило, болеют взрослые и лица, впервые прибывшие на территорию природного очага. Также поражается сельское население, работающее в открытой местности (рисовые поля и др.).
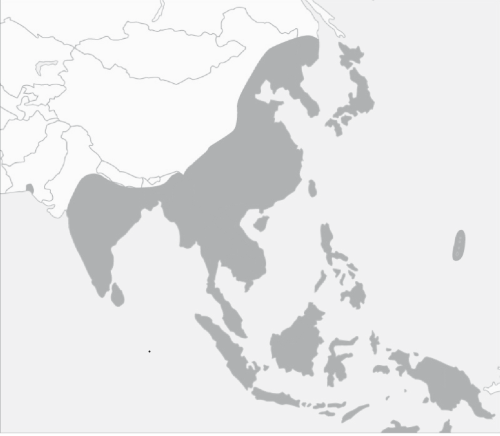
Рис. 3. Распространение японского энцефалита в мире (Atlas of Tropical Medicine and Parasitology, 2006)
Патогенез. Попав в кровь со слюной комара, вирус распространяется гематогенным путем по всему организму и, вследствие нейротропности, проникает в ЦНС, поражая эндотелий сосудов мозга, базальные ядра и другие структуры. В результате накопления (размножения) вируса в мозговой ткани возникает вторичная вирусемия, совпадающая с окончанием инкубационного периода и продолжающаяся до 4-5-го дня болезни.
Клиническая картина. Инкубационный период колеблется от 4 до 21 дня, чаще 10–15 дней. Заболевание характеризуется острым началом, резкой головной болью, ознобом и подъемом температуры тела до 39–40 °C. В первые дни могут наблюдаться тошнота, рвота, головокружение, сонливость, расстройство сознания и менингеальные симптомы.
Неврологическая симптоматика проявляется ригидностью мышц затылка, повышением мышечного тонуса. При лихорадке и общемозговых явлениях появляются моно- и гемипарезы, параличи чаще верхних конечностей и лицевого нерва, судороги. С 3^-го дня болезни возникают симптомы очагового поражения нервной системы, нарастает угнетение сознания, вплоть до коматозного. Иногда бывают бред, галлюцинации, психомоторное возбуждение.
Повышение мышечного тонуса экстрапирамидного и пирамидного характера является причиной вынужденного положения больного в постели: на спине или на боку с запрокинутой головой, согнутыми ногами и руками. У детей могут превалировать боли в животе, понос, судороги. Смерть обычно наступает в первые 10 дней болезни. Период реконвалесценции затягивается.
Нейропсихические осложнения включают паркинсонизм, моторные расстройства, эмоциональную неустойчивость, снижение интеллекта.
Диагностика. Диагноз ЯЭ на догоспитальном этапе должен базироваться на клинических, эпидемиологических, серологических данных. Помимо сбора сведений о жалобах и объективных данных, необходимо подробное выяснение эпидемиологического анамнеза. Он включает сведения о пребывании пациента в странах и на территориях, неблагополучных вследствие широкого распространения ЯЭ в период максимальной плотности переносчика.
С учетом клинических и эпидемиологических данных проводится неврологическая диагностика, назначается лабораторное исследование крови на наличие антител к вирусу. Выявление специфических антител класса IgM методом ИФА позволяет быстро подтвердить диагноз японского энцефалита на ранних сроках болезни, идентифицировать скрытые формы инфекции. Кроме того, обнаружение антител к вирусу ЯЭ позволяет дифференцировать заболевание с другими флавовиру-сами. Иммунологическая диагностика ЯЭ основывается также на выявлении четырехкратного прироста антител в РСК, торможении гемагглютинации или нейтрализации.
В летальных случаях диагноз устанавливается и подтверждается выделением вируса из мозговой ткани путем заражения мышей, либо обнаружением вирусного антигена с помощью иммунофлюоресцентного метода.
Лечение. Применяются сыворотка реконвалесцентов, гипериммунная лошадиная сыворотка или гамма-глобулин, симптоматические средства. Серотерапию необходимо проводить в самые ранние сроки болезни. Сыворотки реконвалесцентов по 20–30 мл или гипериммунную сыворотку лошадей по 15–20 мл вводят внутримышечно или внутривенно ежедневно в течение 3–4 дней в первые 5–7 дней болезни. В остром периоде рекомендуется использовать гамма-глобулин ежедневно по 3–6 мл 3 раза в день. Проводится терапия отека (набухания) головного мозга, дезинтоксикационная и симптоматическая терапия. Пациентам в стадии реконвалесценции необходимо усиленное питание. Они должны находиться в течение 3–4 недель на постельном режиме и не менее 1,5 мес. в стационаре. После выписки из лечебного учреждения за ними устанавливается диспансерное наблюдение.
Прогноз. ЯЭ отличается тяжелым течением. Нарастание симптомов происходит в течение 3–5 сут. Температура тела держится от 3 до 14 дней и падает литически. Летальный исход отмечается в 40–70 % случаев, обычно в первую неделю болезни. Однако смерть может наступить и в более поздние сроки в результате присоединившихся осложнений. В благоприятных случаях возможно полное выздоровление с длительным периодом астении.
Профилактика. В случае выявления больного ЯЭ осуществляется его госпитализация в инфекционную больницу по клиническим и эпидемиологическим показаниям (изоляция от комаров), так как исход заболевания может зависеть от своевременности лечебных мероприятий, в частности введения специфического гамма-глобулина.
Больной ЯЭ источником инфекции для людей не является, поэтому в очаге не проводятся мероприятия карантинного характера. Основные профилактические меры – защита населения от нападения комаров с помощью индивидуальных средств (применение репеллентов, защитных сеток, пологов) и борьба с переносчиком (мелиорация, дренирование рисовых полей, размещение свиноферм вдали от жилья человека и др.).
Наиболее кардинальное средство профилактики ЯЭ – специфическая профилактика, проводимая среди животных и людей. Группами с высоким риском заражения являются дети и подростки.
Для прививок используют сухую инактивированную вакцину из мозга инфицированных мышей, которую вводят двукратно с интервалом в 1–4 недели в дозе 1,0 мл подкожно. Наибольший эффект дает введение третьей дозы по схеме: вторая прививка – через 7 дней после первой, а третья – через 30 дней. Через год рекомендуется бустер-инъекция препарата. Вируснейтрализующие антитела после трех доз в высоком титре сохраняются в течение 6-12 мес., а после дополнительной прививки – в течение 3 лет.
Иммунизацию рекомендуется проводить жителям природного очага, а также туристам, посещающим эндемичные страны в сезон передачи ЯЭ, и лабораторным работникам.
Вакцинация животных (свиней, лошадей) осуществляется вакциной (живой или убитой), полученной на почках сирийских хомяков. Она предупреждает развитие у животных вирусемии и тем самым заражение комаров.
Защитная эффективность мозговой вакцины в различных наблюдениях колеблется от 76 до 94 % и зависит от антигенных вариантов вируса, циркулирующего в данной местности.
Лихорадка денге
Лихорадка денге – острая вирусная болезнь. Протекает с лихорадкой, интоксикацией, миалгией и артралгией, экзантемой, лимфаденопатией, лейкопенией, в некоторых случаях с геморрагическим синдромом. Относится к трансмиссивным зоонозам.
Синонимы: костоломная лихорадка, суставная лихорадка, лихорадка «жирафов», пятидневная лихорадка, семидневная лихорадка, финиковая болезнь, англ. – dengue fever, break bone fever, итал. – denguero).
Этиология. Возбудители лихорадки денге относятся к вирусам семейства Togaviridae рода Flavivirus (арбовирусы антигенной группы В). Содержат РНК, имеют двухслойную липидную оболочку из фосфолипидов и холестерола, размеры вириона – 40–45 нм в диаметре. Инактивируется при обработке протеолитическими ферментами, прогревании выше 60 °C, под влиянием УФО. Известно четыре типа вируса денге, различных в антигенном отношении. Остальные вирусы денге имеют антигенное родство с вирусами желтой лихорадки, японского энцефалита и энцефалита Западного Нила. Вирус размножается на культурах тканей и клетках почек обезьян, хомяков и др. В сыворотке крови больных вирус сохраняется при комнатной температуре до 2 мес., а высушенный – до 5 лет.
Эпидемиология. В последние годы наблюдается значительное повышение заболеваемости в различных регионах. Сообщалось о вспышках лихорадки денге в Китайской Народной Республике, Вьетнаме, Индонезии, Таиланде и на Кубе. Причины подъема заболеваемости остаются неясными, несмотря на исследование данной проблемы.
Источник инфекции – больной человек, обезьяны и, возможно, летучие мыши. Передача инфекции человеку осуществляется комарами Aedes aegypti, обезьянам – A. albopictus. Комар A. aegypti становится заразным через 8-12 дней после питания кровью больного человека и остается инфицированным до 3 мес. и более. Вирус способен развиваться в теле комара лишь при температуре воздуха не ниже 22 °C.
Географическое распространение. Лихорадка денге наблюдается в тропических и субтропических районах (от 42° с.ш. до 40° ю.ш.). Она встречается в странах Южной и Юго-Восточной Азии, Океании, Африки, бассейна Карибского моря (рис. 4). Заболевают преимущественно дети, а также вновь прибывшие в эндемичный район лица.

