
Полная версия
Реальные пути увеличения продолжительности жизни человека
И, наконец, имеется серьёзный материал о возникновении патологии внутренних органов и развитии хронических заболеваний, вызванных травмами позвоночника. Наш позвоночник является проводником симпатических трактов и нервов. Внутри позвоночного столба проходит спинной мозг, в составе которого имеются нервные клетки – нейроны, и нервы, принадлежащие симпатической нервной системе.
В каждом спиномозговом нерве, выходящем из позвоночника, имеются моторные нервы, по которым осуществляется управление мышцами, и чувствительные нервы, несущие в мозг информацию о состоянии отдельных участков нашего тела. В каждом нервном корешке и спиномозговом нерве имеются также нервы симпатической нервной системы, управляющие моторикой и секреторными функциями внутренних органов. Травмирование симпатических нервов также способно вызвать нейротрофические эффекты, которые возникали в описанных выше экспериментах. Любое хроническое заболевание – гастрит, язвенная болезнь, колит, энтероколит, нефрит и нарушения в состоянии и деятельности сердца могут быть вызваны нарушениями симпатической иннервации при компрессии (сдавлении) или раздражении спиномозговых симпатических нервов в том или ином сегменте позвоночника.
Симпатические нервные волокна – аксоны имеют ряд морфологических особенностей, благодаря которым возможны патологические влияния на состояние и проводимость симпатических нервов со стороны мышечного корсета позвоночника. Симпатические нервные волокна в отличие от всех волокон центральной нервной системы, моторных и сенсорных, не имеют прочной миелиновой оболочки, образованной десятками оборотов мембраны вокруг волокна и предохраняющей их от сдавления или раздражения. Нарушения симпатической иннервации могут вызываться не только травмами, но и «жесткими» мышцами, между которыми проходят симпатические нервные волокна после выхода нерва из позвоночника.
2.6. Четвёртый фактор, сокращающий продолжительность жизни человека
2.6.1. Влияние стрессов на физиологические параметры организма
Процесс адаптации связан с формированием общего адаптационного синдрома (ОАС) – комплекса реакций, возникающего в целостном организме под действием различных повреждающих факторов и обеспечивающего приспособление организма к данным условиям.
Общий адаптационный синдром – неспецифическая реакция организма на разнообразные сильнодействующие факторы, в том числе и факторы среды, запускающие формирование срочной адаптации. Интенсивность ОАС зависит от силы действующего фактора. Общий адаптационный синдром нередко обозначают как стрессреакцию. Стресс – это комплекс физиологических реакций, возникающих в организме человека и животных под действием стимула, несущего угрозу – стрессора.
Проявления стресса (триада Селье):
– увеличение массы надпочечников;
– инволюция (обратное развитие) тимуса и лимфатических узлов;
– появление кровоточащих язв в желудке и двенадцатиперстной кишке.
Общий адаптационный синдром проходит ряд стадий развития:
Стадии стресса по Г. Селье
Стадия тревоги (alarm reaction). Разделяется на две фазы: шок и противоток. Шок характеризуется торможением активности ЦНС, снижением АД, мышечного тонуса, температуры тела, уровня глюкозы в крови, сопротивляемостью организма и т. д. Противошок характеризуется повышением резистентности организма и мобилизацией функциональных его резервов (срочная фаза адаптации);
Стадия резистентности – характеризуется максимальной устойчивостью организма к стрессору, формированием долговременной адаптации и системного структурного следа;
Стадия истощения – возникает при действии сильных и длительных стрессоров, которые приводят к истощению функциональных резервов организма, после чего он, как правило, погибает. Стадийность в развитии ОАС прослеживается при хроническом действии стрессора на организм. Наиболее острые явления происходят во время стадии тревоги. Именно в этот период секретируется наибольшее количество катехоламинов и глюкокортикоидов (важнейший из них у человека – кортизол). В этой стадии могут развиться и наиболее опасные для организма повреждения, которые весьма часто сопутствуют стрессу. В стадии тревоги в связи с выбросом в кровь большого количества глюкокортикоидов подавляется воспалительная реакция, но общий уровень сопротивляемости организма снижен. Если стрессор продолжает действовать, острые явления исчезают и организм переходит в фазу резистентности. В этот период гормоны секретируются в меньших количествах, но резистентность организма к различным повреждениям в этот период повышена. В третьей стадии сопротивляемость снижается, и это уже свидетельствует о печальном прогнозе. Когда речь идет о резистентности, имеется в виду, прежде всего, сопротивляемость неспецифическая. Организм, переживший стресс, становится устойчивым не только к тому фактору, который вызвал стресс, но и к некоторым другим.
Механизм формирования ОАС (стресса)
Гормоны, выделяемые при стрессе, оказывают многообразное действие на организм. Один из основных эффектов кортизола – повышение уровня сахара в крови за счет стимуляции глюконеогенеза – синтеза глюкозы из неуглеводных источников, в частности из аминокислот. Концентрация глюкокортикоидов в крови во время стресса может возрасти в десятки раз.
Наряду с этим, во время стресса активируется симпатическая нервная система и усиливается выброс в кровь из мозговой зоны надпочечников катехоламинов – адреналина, норадреналина. Под влиянием катехоламинов идет распад гликогена в печени и в крови повышается концентрация глюкозы. Кроме того, адреналин является сильным липолитическим фактором, стимулирующим распад жира с образованием свободных жирных кислот. Основной эффект катехоламинов – мобилизация энергетических и структурных резервов организма, и в этом смысле они работают синергично с глюкокортикоидами.
2.6.2. Основные эффекты глюкокортикоидов и катехоламинов при стрессе
Значение стресса, очевидно, заключается в том, что после пережитой «встряски» организм приобретает резистентность к самым разнообразным факторам. Ну и, наконец, стресс, как полагает Ф. З. Меерсон, за счет своего катаболического эффекта может стимулировать и процесс дезадаптации, т.е. стирание старых, утративших свое значение системных структурных следов. Стресс, как правило, вызывает образование язв в ЖКТ, очаги повреждений можно обнаружить и в сердечной мышце – и у стрессированных животных, и у стрессированных людей. Сильное эмоциональное потрясение на фоне, казалось бы, полного здоровья зачастую вызывает развитие тяжелого инфаркта. Инфаркт можно вызвать искусственно, вводя экспериментальным животным чрезмерно высокие дозы адреналина. Что же является основой всех этих повреждений вне зависимости от места их возникновения?
Начальным этапом является тканевая ишемия, одной из причин которой может быть сосудистый спазм, вызванный активацией симпатической нервной системы и высоким уровнем катехоламинов в крови. Недостаток кислорода инициирует образование активных кислородных метаболитов (АКМ), отличающихся огромной реакционной способностью. Несмотря на достаточно короткий период их существования, АКМ успевают прореагировать с липидами биомембран, образуя так называемые продукты перекисного окисления липидов (ПОЛ). Эти продукты, обладая детергентными свойствами, способны заметно нарушать свойства биомембран: меняется их текучесть, нарушается проницаемость для ионов натрия и кальция. Увеличение натриевой проницаемости приводит к деполяризации мембраны, что еще в большей степени усиливает проницаемость мембраны для кальция. Появление кальция в клетке активирует целый ряд ферментов, в том числе и фосфолипазы. Фосфолипазы еще больше усиливают деградацию мембранных фосфолипидов, что может завершиться дезорганизацией клетки и ее гибелью. Под влиянием фосфолипаз могут разрушаться лизосомы, содержащие весьма активные протеазы, появление которых в цитоплазме ускоряет процесс гибели клеток. Именно в результате развертывания подобного негативного «сценария» и появляются язвы на слизистой желудка и очаги некроза (инфаркты) в сердце.
У человека стресс наиболее часто возникает на фоне эмоциональных переживаний и практически всегда, когда они сочетаются со страданиями физическими. Все патологии условно можно разделить на три группы: нарушения психического здоровья, которые затем реализуются в психосоматические нарушения; заболевания, сопровождающиеся различными морфофункциональными повреждениями (формирование язв, инфаркты); патологии, связанные с подавлением иммунной системы, – это рост опухолей и развитие инфекций.
Подводя итог, необходимо отметить, что негативные последствия стресса – это довольно обширный список патологий, возникающих как в ближайшем постстрессовом периоде, так и в отдаленном будущем.
Несмотря на высокую степень патогенности стрессовых ситуаций, они не всегда сопровождаются развитием заболеваний, особенно тех, которые протекают с повреждением тканей. Для большинства стрессовых ситуаций средней напряженности правилом на выходе скорее является благополучный исход, а не болезнь.
2.6.3. Стрессы вызывают спастические состояния в межпозвонковых мышцах
В течение нашей оздоровительной практики мы многократно наблюдали возникновение мышечных блоков в позвоночнике после перенесённых стрессов. Например, аварийная ситуация на дороге приводила на следующий день к сильным болям в спине и невозможностью управлять автомобилем в течение двух недель. У одной из наших пациенток стрессовые ситуации приводили к образованию мышечных блоков в верхнегрудном отделе позвоночника и стенокардии, на устранение которых требовалось несколько сеансов массажа и две недели времени.
2.7. Пятый фактор, сокращающий продолжительность жизни человека
Кислотность крови2.7.1. ГипоалкалозО кислотности крови человек не задумывается никогда, хотя это важнейший показатель гомеостаза, нарушение которого приводит к смерти. Крайние пределы pH, совместимые с жизнью, это 7,0 – 7,8. В норме кровь должна иметь слабощелочную реакцию – 7,36 – 7,42 артериальная кровь и 7,26 – 7,36 венозная кровь. Межклеточная жидкость тканей также слегка щелочная – 7,26 – 7—38 (Киеня А. И., Бандажевский Ю. И., 1997). Все ферменты человека кроме желудочного фермента – пепсина работают только в нейтральной и щелочной среде. При переходе кислотности крови в кислую область, рушится иммунитет, нарушаются все механизмы гомеостаза и синтеза белков, ферментов и гормонов. Это явление называется ацидозом. Ацидоз – термин, неправильно применяемый по отношению к пониженной щелочности жидкостей организма. Жидкости организма обычно слегка щелочные. Снижение щелочности более правильно называть гипоалкалозом. Гипоалкалоз определяет состояние организма, характеризующееся дефицитом постоянных щелочей в организме, что ведет к росту выделения мочевины и повышению кислотности мочи. Кровь в норме в течение всей жизни никогда не бывает кислой. Щелочные кровь и лимфа необходимы для жизни и здоровья. Достаточно иметь даже нейтральное состояние крови, чтобы быстро вызвать смерть. Физиологическое соотношение между щелочью и кислотой в организме, называемое кислотно-щелочным равновесием, составляет 80:20, т. е. 80% щелочи и 20 – кислоты. Это соотношение поддерживается так называемыми буферными солями – натрием, калием, кальцием и магнием, за счет которых каждая сторона пополняет запасы по мере необходимости. Когда этот буфер, или «колесо равновесия», в порядке, любой избыток кислот в организме быстро нейтрализуется. И только при нехватке этих солей могут возникнуть осложнения. Нарушение соотношений между ними и сдвиг кислотно-щелочного равновесия в сторону кислотности неправильно называют ацидозом. Организм ни минуты не терпит присутствия внутри себя свободной кислоты, за исключением желудка время процесса пищеварения. Все кислоты немедленно «связываются» щелочами, что делает их безвредными. Организм использует любой резерв, имеющийся в его распоряжении, для того, чтобы сохранить свою щелочность, ибо клетки могут функционировать только в щелочной среде и не могут в кислой.
Поскольку мы обеспечиваем организм кислотами и щелочами через пищу, вопрос о соотношении между кислыми и щелочными (базовыми) продуктами крайне важен. Если принять излишек кислой пищи или накопить большое количество кислых остаточных продуктов белкового метаболизма или расхода слишком большой части щелочей организма в результате развития кислого брожения в желудочно-кишечном тракте или же потребления излишней кислотообразующей и бедной щелочами пищи и медицинских кислых препаратов. Результат будет один и тот же: начало – пониженное содержание щелочей, а конец – нарушение функций пропорционально степени гипоалкалоза с прогрессирующим развитием в направлении серьезного органического заболевания и смерти.
Симптомами гипоалкалоза являются усталость, головные боли, потеря аппетита, сонливость, общая нервозность, повышенная кислотность желудка, кислотная потливость, плохое настроение, частые недомогания вроде простуды и другие явления. Гипоалкалоз тормозит рост молодых, делает слабыми взрослых, снижает жизненную активность. Он оказывает огромное отрицательное влияние на состояние беременных женщин и выработку у них материнского молока. Он предрасполагает к туберкулезу, раку, воспалению легких, аппендициту, кори и прочим болезням. Хроническая усталость часто есть не что иное, как кислотная токсемия, которая, если её не устранить, по мере развития и распространения будет иметь своими результатами преждевременное старение, функциональные расстройства, органические заболевания и в итоге преждевременную смерть. Кровь, лишенная нормальной щелочности, не в состоянии нейтрализовать или скорректировать кислые продукты «усталости», которые и получают возможность отравлять организм. Здоровье, сила, юность, рост и сохранение организма зависят от определенного уровня щелочности. Старость, которую мы сегодня знаем, это преждевременная старость – болезнь, которая не имеет какой-то определенной органической формы. Это есть результат самоотравления, аутоинтоксикации, т. е. накопления кислых отходов. Наконец, гипоалкалоз приводит к повышенной свёртываемости крови и образованию тромбов, инсультов и инфарктов.
2.7.2. Пищеварение и кислотность крови
О пищеварении человек также редко задумывается, считая, что если желудок не реагирует болью на состав пищи, то всё хорошо. В пищеварительной системе имеется более сотни параметров, контролируемых системами саморегуляции, нарушения которых приводят к утрате здоровья, хроническим заболеваниям не только органов ЖКТ, но и печени, лёгких, почек и желёз внутренней секреции. Забегая вперёд, мы должны сказать, что именно с нарушения функций желудка, его систем саморегуляции и адаптационных механизмов начинаются все остальные заболевания, включая онкологические.
Для понимания важности сохранения нормального функционирования желудочно-кишечного тракта, мы приведём небольшой ряд цифровых показателей (по Семёнову Н. В., 1971).
Слюна. Количество в сутки – 1,4 – 1,5 литра. Кислотность pH – 5,6 – 7,6. Амилаза – фермент, расщепляющий углеводы, – до 150 мг.
Желудок. Количество 2 – 3 литра в сутки. Кислотность pH – 1,49 – 1,80. Скорость секреции – 0,7 – 9,5 мл /мин. Пепсин. 4119 (0 – 8335) гемоглобиновых единиц в час.
Панкреатический сок. Количество 600 – 700 мл в сутки. Кислотность pH – 8,6 – 9,0.
Сок тонкого кишечника. Количество – 1 литр в сутки. Кислотность pH – 6,5 (5,07 – 7,07).
Сок толстого кишечника. Количество в сутки, средний отдел – 840 мл (270 – 1550), нижний отдел – 555 мл (420 – 705).
Минимальный объём выделяемых соков составляет 6,0 литров жидкости, максимальный – 8,5 литров. Но это ещё не всё. Тонкий кишечник вырабатывает до 1 литра лимфы, которая по главному лимфатическому сосуду через подключичную вену попадает в кровь. Остальные 8,5 литров плюс 3 литра выпиваемой в сутки жидкости, т.е. 11,5 литров всасываются через слизистую оболочку толстого кишечника в кровеносную систему. Иными словами, через кровеносную систему в сутки прокачивается до 12,5 литров жидкости с переменным составом солей и кислот. Конечно, следует учитывать потовыделение и влажность выдыхаемого воздуха. Они тоже сказываются на объёме циркуляции жидкостей. Естественно, что все соки ЖКТ извлекаются слизистыми оболочками органов ЖКТ из плазмы крови. Таким образом, в организме человека третий круг кровообращения – циркуляция жидкостей через кровеносную систему, т.е. лимфа крови – соки ЖКТ – печень – лимфа крови. В этом круге постоянно меняется состав электролитов и кислотность.
Соляная кислота в желудке вырабатывается из лимфы крови. Именно выработка соляной кислоты желудочным эпителием создаёт щелочную среду крови. Сколько в желудке выделилось соляной кислоты, столько же в крови образовалось щелочи. При снижении кислотообразующей функции желудка снижаются щелочные показатели крови и происходит гипоалкалоз. Это наблюдается при компрессии симпатических нервов в области 6 – 8 грудных позвонков. За секрецию желудочного сока отвечает система блуждающего нерва – вагуса. Нарушение симпатической иннервации приводит к нарушениям регенеративных механизмов в желудке и постепенному снижению числа секреторных клеток. Секреторные клетки замещаются на колбовидные клетки. Начинается атрофический гастрит. Снижение кислотности желудочного сока приводит, с одной стороны, к неполному перевариванию белков и их гниению в кишечнике с образованием токсинов, а, с другой стороны, к гипоалкалозу. Выстраивается патологическая цепь: стресс – возникновение спастических состояний межпозвонковых мышц – компрессия симпатических нервов – нарушение трофической функции нервной системы – нейродистрофические процессы в желудке – нарушение пищеварения – аутоинтоксикация и алкалоз – нарушение гомеостаза и регенеративных процессов во всём организме – преждевременное старение и хронические заболевания.
2.7.3. Преждевременное старение как следствие воздействия 5 важнейших факторов, сокращающих продолжительность жизни
Итак, мы познакомились с 5 важнейшими факторами, вызывающими хроничесие и онкологические заболевания и приводящими к сокращению продолжительности жизни человека:
– токсемия – накопления токсинов и метаболитов в тканях внутренних органов;
– недостаток незаменимых биокомпонентов: незаменимые аминокислоты, незаменимые жирные кислоты, витамины и микроэлементы;
– нарушение трофической функции нервной системы, вызывающие нейродистрофические процессы во внутренних органах;
– стрессы;
– понижение щелочной реакции крови и внутренней среды внутренних органов – гипоалкалоз.
Все клетки нашего организма со временем обновляются путём деления.
Таблица 2. Продолжительность жизни клеток разных органов человека
(По Klima, 1967; Rucker, 1967).
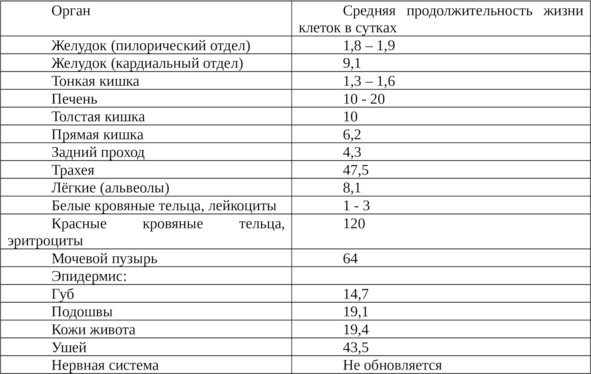
Из приведённых данных следует, что мы всё время разваливаемся и теряем старые клетки, но всё время обновляемся. Этот процесс называется регенерацией. И этот процесс может быть нарушен при нарушении механизмов, управляющих регенерацией. Как было показано выше, автономная нервная система управляет процессами регенерации, а нарушения в её работе приводят к нарушениям регенеративных процессов. Это и есть проявление трофической функции нервной системы. Для обновления нашего тела требуется, с одной стороны, активное воздействие на ткани внутренних органов со стороны автономной нервной системы, с дугой стороны, запас биокомпонентов, необходимых для роста новых клеток: аминокислоты, микроэлементы, жирные кислоты, витамины. Но и этого ещё недостаточно – необходимо отсутствие интоксикации. Наши собственные метаболиты и токсины из кишечника вызывают аутоиммунные процессы, нарушающие регенерацию тканей. С возрастом у человека падает продукция гормонов и ферментов. Это снижает темпы регенерации и закономерно приводит к нормальному старению человека, которое, учитывая опыт долгожительства, должно начинаться в 90 лет или даже позднее.
Важный вывод: Хронические и онкологические заболевания, рассматриваемые как возрастные заболевания, предшествуют нормальному старению и являются результатом нарушения работы основных физиологических систем: питание, очищение от метаболитов и обеспечение регенеративных процессов.
Глава 3. Патофизиологические факторы, приводящие к развитию нервных дистрофий.
Остеохондроз позвоночника – проявление преждевременного старения организма
Предисловие
Остеохондроз позвоночника имеет важнейшее значение для возникновения нейродистрофических процессов во внутренних органах. В следующих главах будет показано, что остеохондроз позвоночника, являясь проявлением преждевременного старения костно-хрящевой ткани, запускает патологическую цепь преждевременного старения внутренних органов и систем. Остеохондроз позвоночника затрагивает и дистрофические процессы в мышечном корсете позвоночника, вызывая фиброз мышечной ткани, нарушение кровообращения в сегментах спинного мозга и приводит к необратимым компрессиям симпатических нервов, иннервирующих внутренние органы. Следствием этого являются хронические заболевания и преждевременное старение организма в целом.
МРТ исследования, функциональные пробы, термография спины и мануальная диагностика показали, что в областях позвоночника, имеющих болевые синдромы, существуют долговременные спастические состояния межпозвонковых мышц. Спастические состояния проявляются как мышечные блоки – области позвоночника с нарушенной подвижностью позвонков вплоть до полной неподвижности. Ранее считалось в соответствии с теорией остеохондроза позвоночника проф. Я. Ю. Попелянского, что это функциональные блоки, защищающие повреждённые дистрофическим процессом позвонки и межпозвонковые диски от дальнейшего разрушения. Первичным процессом считались дистрофические процессы в позвонках и дисках, а вторичными явлениями считались функциональные мышечные блоки, болевые синдромы в спине, корешковые синдромы, болевые синдромы в конечностях и внутренних органах. Анализ сотен МРТ исследований с учетом возрастного аспекта показал, что первичными процессами являются спастические состояния межпозвонковых мышц, вызванные функциональными нарушениями в работе сократительного аппарата мышц. Эти нарушения имеют обратимый характер, но если их вовремя не устранить, то они приводят к необратимым дистрофическим изменениям тканей позвоночника – остеохондрозу позвоночника, дистрофическим изменениям в структуре и патологии мышц позвоночника. Эти изменения проходят в течение нескольких лет и вызваны нарушением трофики позвонков и дисков. Жесткие спазмированные мышцы позвоночника приводят к компрессии кровеносных сосудов, питающих как позвонки и межпозвонковые диски, так и сегменты спинного мозга, вызывая ишемию. Таким образом, остеохондроз позвоночника это преждевременное старение тканей позвоночника и мышц позвоночника при этом это необратимое состояние.
Следствием спастических состояний межпозвонковых мышц является компрессия симпатических нервов, иннервирующих внутренние органы. А. Д. Сперанским и возглавляемым им отделом нервной трофики института Экспериментальной Медицины было доказано, что симпатические нервы ответственны за регуляцию метаболизма тканей внутренних органов. Компрессия этих нервов вызывает дистрофические процессы во внутренних органах. Наоборот, раздражение этих нервов приводит к кровоизлияниям и образованию язв во внутренних органах. На протяжении нескольких месяцев компрессия симпатических нервов является обратимым процессом. С исчезновением спастических состояний мышц компрессия исчезает. Остеохондроз позвоночника приводит к ухудшению состояния мышц – возникает фиброз, мышцы теряют сократимость и сохраняют свою жесткость. Компрессия симпатических нервов становиться необратимой, вызывая функциональные нарушения в работе внутренних органов и их преждевременное старение. Ведущими Российскими геронтологами доказано, что ослабление нервного контроля над деятельностью внутренних органов способствует прогрессу возрастных заболеваний (Фролькис В. В., Мурадян Х. К., 1988). Все эти вопросы будут подробно рассмотрены в этой главе и в следующих главах.
3.1. Актуальность проблемы остеохондроза позвоночника
Количество дней нетрудоспособности вследствие болей в области опорно-двигательного аппарата и позвоночника лидирует в списке больничных листов. И, если раньше заболевания позвоночника относились к старшим возрастным группам, то ныне болезни, связанные с позвоночником, сильно помолодели. По данным московского центра мануальной терапии 70% людей нуждаются в услугах массажиста или мануального терапевта (Ситель А. Б., 2005). Проф. Я. Ю. Попелянский (Попелянский Я. Ю., 1989) заявляет: «По количеству дней нетрудоспособности среди всех хронических заболеваний человека на первом месте стоят радикулиты пояснично-крестцовые и шейно-грудные».





