
Полная версия
Виноградная водка. Записки практика
.

Эта энергия частью расходуется на поддержание температуры тела дрожжевого грибка44, но и не только для этого, т. к. биологические системы должны запасать энергию в каком-то виде так, чтобы впоследствии использовать её в химических реакциях для обеспечения своей жизнедеятельности. Например, как было отмечено выше, энергия необходима дрожжевому грибку для синтеза белка из его составных частей – аминокислот.
Сахароза (в быту сахар) – дисахарид – тростниковый или свекловичный сахар, представляет собой белые сладкие на вкус кристаллы, хорошо растворимые в воде. В сахарном тростнике содержится 14—16% сахара, в клубнях сахарной свёклы – 16—20%, а в некоторых сортах до 27%.
Сахар впервые начали выделывать свыше 2500 лет назад. Ещё раньше в Индии умели разводить сахарный тростник и его сладкий сок употребляли в пищу. Позднее из этого сока стали получать выпариванием твёрдый сахар-сырец коричневого цвета. Твёрдый сахар белого цвета впервые научились получать в Иране. Для этой цели сок сахарного тростника сгущали нагреванием в котлах, подливая к нему молоко. При этом красящие примеси уходили в пену. От иранцев искусство делать белый сахар перешло в Египет. Тысячу лет тому назад египетский сахар завозили в Европу и продавали в аптеках как лекарственное средство. В XVI веке сахарный тростник стали разводить в Америке на острове Куба и в Мексике. Долгое время в Америке производили только тростниковый сахар-сырец и привозили его в приморские города Европы, где он очищался на рафинадных заводах. В России первый сахарно-рафинадный завод, перерабатывающий привозной тростниковый сахар, был построен в Петербурге в 1719 г.
В середине XVIII века было выяснено, что в свёкле и многих других растениях, произрастающих в самой Европе, тоже находится сахар, причём в количествах, достаточных для промышленного производства.
Первый завод в Европе по производству сахара из свёклы был построен в Германии в 1799 г. Однако это производство вскоре заглохло и возродилось вновь только в двадцатых годах XIX века. В России первый завод по производству свекловичного сахара был построен в 1802 г в Тульской губернии, а в 1805 г. в России было добыто из сахарной свёклы всего 5 тонн сахара [18], поскольку себестоимость продукта была крайне велика – фунт сахара стоил 2 руб, а корова – 5 руб. Однако по мере усовершенствования технологии цена непрерывно снижалась и упала до 14 коп. за фунт. По объёму производства сахара Россия накануне Первой мировой войны занимала 2-ое место в мире после Германии.
При попадании сахара (сахарозы) в организм человека или при внесении сахара в бродильную жидкость, содержащую дрожжи, он под действием фермента дрожжей инвертазы присоединяет молекулу воды и распадается на глюкозу и фруктозу:
,
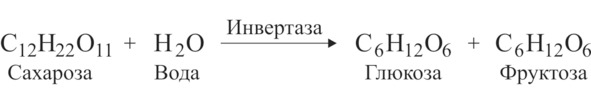
которые, в свою очередь, распадаются на спирт и углекислый газ как было описано выше45. В течение дня организм здорового и непьющего человека способен синтезировать из пищи от 1 до 9 г этилового спирта [4] и ферментных мощностей организма вполне хватает для его окисления с целью получения энергии. При больших дозах введённого в организм алкоголя ферменты не успевают его окислять. В организме накапливается этиловый спирт и продукт его частичного распада – ядовитый ацетальдегид, что вызывает симптомы обширной интоксикации, называемой в быту похмельем. Считается, что ежедневная доза спиртного, эквивалентная 20 г чистого алкоголя, относительно безопасна для здоровья. Но важна не только доза выпитого алкоголя, но и время его употребления. Тот, кто следит за своим здоровьем, по опыту знает, что не стоит принимать спиртное ранее трёх часов дня и после полуночи46.
Крахмал – полисахарид, состоит из смеси двух других, менее сложных полисахаридов – амилозы (30%) и амилопектина (70%). Представляет собой белый порошок нерастворимый в воде и является важнейшим резервным углеводом всех растений. В природе крахмал вырабатывается растениями и находится у них в клетках в виде зёрен, форма и величина которых в различных растениях разная. Например, клубни картофеля содержат 20% крахмала при содержании воды 75%, а в зёрнах пшеницы до 70% крахмала.
При нагревании с водой зёрна крахмала разбухают и образуют клейстер. При частичном гидролизе крахмала или при нагревании его до температуры 180—200оС крахмал расщепляется на декстрины – твёрдые, но уже растворимые в воде вещества, состоящие из более простых углеводов. По молекулярной массе декстрины занимают промежуточное положение между молекулярными массами глюкозы и крахмала. Блеск накрахмаленной рубашки, появляющийся при её глажении, обусловлен декстринами, образующимися в результате разрушения крахмала горячим утюгом. Блестящая корочка свежеиспечённого хлеба также состоит из декстринов47.
Под влиянием широко распространённого в растительном мире фермента диастазы48 крахмал гидролизуется, присоединяя воду, и образует дисахарид мальтозу или солодовый сахар:

В технике этот процесс называют осахариванием крахмала, независимо от того из чего он получен – картофеля, свёклы, кукурузы или злаковых культур.
В связи с этим, полезно иметь представление о технике получения этилового спирта из крахмала, содержащегося, например, в картофеле [18]49. Клубни картофеля предварительно моют, распаривают под давлением 3—3,5 атм. в конических железных котлах, а затем выдувают через находящуюся снизу котла выдувную трубу. При этом принимают меры для охлаждения, поскольку температуры выше 65оС уничтожают диастазу. Из-за резкого уменьшения давления на выходе из котла оболочки клеток картофеля разрываются, содержащиеся в них зёрна крахмала освобождаются, и образуется вязкая киселеобразная субстанция – клейстер, аналогичный клейстеру из пшеничной или ржаной муки50. После добавления к нему солода происходит гидролизация крахмала по приведённой выше формуле. По окончании этого процесса первоначально густая жидкость становится подвижной, более прозрачной и сладкой на вкус. Её охлаждают до 18—20оС и подвергают спиртовому брожению путём добавления винных дрожжей.
Первые несколько часов выделения спирта почти не происходит – дрожжи интенсивно размножаются, используя находящийся в бродильной жидкости кислород. Примерно через 10 часов их количество увеличивается в 10—14 раз, кислород в бродильном сосуде истощается и начинается процесс интенсивного брожения с выделением тепла. В ходе этого процесса содержащийся в дрожжевых грибках фермент мальтаза расщепляет солодовый сахар мальтозу до виноградного – глюкозы, а другой фермент дрожжей зимаза расщепляет глюкозу до этилового спирта и углекислого газа, как это было описано выше, т.е.:
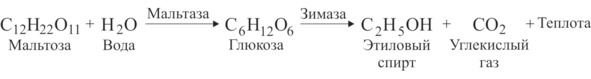
На самом деле формулы спиртового брожения выглядят гораздо сложнее, их запись занимает почти целую книжную страницу [5], но в приведённом упрощённом виде они вполне достаточны для понимания сути происходящих процессов.
Для полноты картины следует упомянуть ещё один углевод, расщепляющийся под действием дрожжей на спирт и углекислый газ. Это весьма полезный в быту дисахарид – лактоза или молочный сахар, открытый в 1612 г. Бартолетти и названный им манна51, т.к. одно время он считался эффективным лечебным средством [8]. Молочный сахар состоит из остатков моносахаридов – глюкозы и галактозы и присутствует в молоке всех млекопитающих. При определённых условиях он сначала гидролизуется под действием фермента ß-галактозиазы в моносахариды, а затем сбраживается в кисломолочные продукты, содержащие незначительные количества спирта. Наиболее известными из них являются кумыс – шипучий пенящийся напиток со спиртовым вкусом и запахом из кобыльего (реже коровьего и верблюжьего) молока с содержанием спирта от 1 до 3%, а также обыкновенный кефир с 0,16—1,22% спирта [17]. При таком содержании спирта в кефире его, как заметил премьер министр РФ В. Путин 13.02.2011 г., «нужно выпить тазик»52, чтобы не пройти водительский тест на алкоголь.
Инулин – полисахарид – содержится в корнях тапинамбура (земляной груши), корнях цикория и др. Представляет собой белый порошок или прозрачные кристаллы. Не растворим в холодной воде. Дрожжи не сбраживают инулин, ферменты солода его не осахаривают. В водной среде при 55—60оС инулин превращается в сбраживаемые сахара под действием находящегося в нём самом фермента инулазы. В 30-е годы прошлого века в СССР была разработана технология получения этилового спирта как из инулина, так и из цикория [27].
Целлюлоза (клетчатка) – полисахарид – представляет собой вещество белого цвета, нерастворимое ни в воде, ни в спирте. Она является главной составляющей частью клеточных стенок растений (отсюда название) и обеспечивает прочность и эластичность растительных тканей. В отличие от других природных полисахаридов, являющихся для растений резервными веществами, которые растения могут преобразовать для своих потребностей в другие вещества, целлюлоза не может быть снова расщеплена в их организме или использована растением каким-либо другим способом.
По своему количеству целлюлоза занимает первое место в мире среди всех остальных природных органических соединений. Гигроскопическая вата, белые хлопчатобумажные и льняные ткани, хорошие сорта фильтровальной бумаги состоят главным образом из целлюлозы (клетчатки). Наиболее чистая природная клетчатка содержится в волосах семян хлопчатника, в которых она составляет 80—90% (при 6—8% воды). Древесина деревьев хвойных пород содержит около 50% клетчатки, лиственных – значительно меньше. Впрочем, чистая целлюлоза находится лишь в молодых клетках растений; по мере старения клеток в них отлагается инкрустирующие вещества, в особенности лигнин – аморфное вещество жёлто-коричневого цвета, вызывающее одревеснение и увеличение прочности растительных клеток.
В организме человека не вырабатывается достаточного количества ферментов (мальтазы и амилазы53) для расщепления целлюлозы до усваиваемой глюкозы – иначе мы не ограничивались бы грушами, а получали удовольствие, откусывая прямо от ствола. Но у травоядных животных есть фермент целлюлаза, вырабатываемый микрофлорой кишечника, под действием которой целлюлоза расщепляется до глюкозы54.
В технике более или менее чистую целлюлозу получают в громадных количествах при производстве бумаги.
В контексте данной книги имеет смысл рассмотреть процесс производства из целлюлозы гидролизного этилового спирта, поскольку его часто используют для фальсификации водки55 вместе с рассмотренным выше синтетическим этиловым спиртом, вырабатываемым из этилена.
Для производства этилового спирта из целлюлозы древесные опилки и другие отходы лесоперерабатывающей промышленности нагревают под давлением с 0,1% раствором серной кислоты. В результате такой обработки целлюлоза расщепляется до глюкозы и образуется сладкий сироп. Этот сироп сбраживают, используя винные дрожжи, и перегоняют в спирт, который по способу производства называют гидролизным спиртом. Он содержит заметное количество вредного для организма метилового спирта и предназначен для использования в технических целях, в частности, для получения синтетического каучука. В среднем из 1 тонны сухого древесного сырья, в том числе вылущенных кукурузных початков, лузги семян подсолнечника, древесных опилок и т. п. можно получить 175 литров этилового спирта. Такое же количество спирта можно выработать из 0,6 тонны зерна или 1,6 тонны картофеля [19]. Хорошим сырьём для производства этилового спирта служат даже корневища злостного сорняка – пырея [27].
В заключение стоит упомянуть об одном слове, давно утратившим свой первоначальный смысл, но имеющим непосредственное отношение к рассматриваемой теме. В обиходе иногда говорят буза, подразумевая под этим что-то простенькое и никчёмное. На самом деле буза – это спиртовой напиток наподобие пива, но без хмеля, который раньше вырабатывали в Крыму и на Кавказе из проса, содержащий 4—6% спирта [5].
И последнее. Как известно пиво тоже представляет собой продукт спиртового брожения. Для его производства нужны ячмень, солод, хмель, вода и пивные дрожжи. Солод превращает крахмал ячменя в солодовый сахар, пивные дрожжи сбраживают его в спиртосодержащий напиток, а хмель придаёт пиву специфический вкус и аромат. Содержание этилового спирта в приготовленном таким способом пиве не превышает 3,5—3,7% об. (только в три раза больше, чем у упомянутого выше кефира!). Поэтому пиво всегда было напитком для утоления жажды, а не для опьянения. Однако в последнее время производители пива стали добавлять в сусло ингредиенты, повышающие при спиртовом брожении содержание в пиве спирта, например, рисовую муку, отходы сахарного производства – мелассу и пр. Такой напиток, строго говоря, нельзя называть пивом. Он стал пьянящим, с тяжёлым похмельем, а при регулярном и длительном употреблении наносящим вред здоровью (вплоть до опухоли поджелудочной железы и рака прямой кишки при регулярном употреблении 0,5 литра в день [4]). Термин «пивной алкоголизм» в ходу у медиков уже лет двадцать. Всё дело в том, что, повышая содержание спирта в пиве путём выбраживания дополнительного количества крахмала, например, крахмала той же рисовой муки, производители тем самым увеличивают и содержание в пиве сивушных масел. Все сивушные масла – высшие спирты – являются наркотиками с наркотическим действием значительно большим, чем у этилового спирта. Но если при производстве этилового спирта из крахмалосодержащего сырья сивушные масла можно отделить перегонкой или очисткой водки на активированном угле, то из пива их удалить невозможно. Они поступают в организм, вызывая сначала привыкание, а затем и алкогольную зависимость.
Из содержания данной главы следует, что использование виноградного сырья для производства этилового спирта в домашних условиях обладает рядом преимуществ по сравнению с его получением из крахмалосодержащего сырья. К числу таких преимуществ относятся:
– простота подготовки сырья и его сбраживание, практически не требующее применения дрожжей и минеральной подкормки56,
– минимальное количество терпимо, чтобы не сказать приятно, пахнущих отходов и, как следствие, простота их утилизации (например, компостирование виноградного жома в дачном хозяйстве),
– незначительное содержание в отгоне сивушных масел из-за отсутствия в сусле посторонних белковых веществ,
– возможность увеличения выхода спирта путём простого добавления в сусло сахара в количествах, не угнетающих брожение,
– наконец, минимальная себестоимость по сравнению с крахмалосодержащим сырьём, т.к. все затраты приходятся только на сбор и транспортировку винограда с дачного участка, а трудоёмкость выращивания винограда весьма незначительна.
Прежде, чем перейти к рассмотрению вопросов, связанных непосредственно с перегонкой спиртосодержащих жидкостей, имеет смысл ознакомиться с особенностями физических процессов кипения и испарения жидкости, и конденсации её паров, которые протекают в перегонном аппарате любой конструкции.
Глава 4. Испарение, кипение, конденсация
Испарение – представляет собой процесс перехода вещества из жидкого состояния в газообразное, т.е. в пар. Испарение происходит за счёт того, что постоянно находящиеся в тепловом движении молекулы жидкости57 в результате соударений с другими движущимися молекулами случайно получают энергию, достаточную для преодоления сил сцепления с жидкостью и покидают её со свободной поверхности. Поэтому испарение возможно при любой температуре, но с возрастанием температуры возрастает интенсивность теплового движения молекул и скорость испарения увеличивается. При переходе в пар молекула должна преодолеть не только силы сцепления с другими молекулами в жидкости, но и совершить работу против молекул уже образовавшегося пара, которые путём таких же случайных соударений могут вернуть её обратно в жидкость. Поскольку обе эти работы совершаются за счёт кинетической энергии молекулы, то в результате испарения жидкость охлаждается. Поэтому, чтобы процесс испарения проходил при постоянной температуре, жидкости необходимо постоянно сообщать некоторое количество теплоты. При процессе обратном испарению – конденсации, т.е. при образовании жидкости из пара, происходит выделение теплоты, и если её не отводить, конденсация прекратится. Примером этому служит паровозный гудок – проходящий через него перегретый пар из котла разогревает корпус гудка и пар, не успевая конденсироваться, вырывается наружу. В результате гудок гудит, а не булькает, разбрасывая брызги.
В закрытом сосуде при заданной постоянной температуре испарение будет происходить до тех пор, пока всё пространство над оставшимся избытком жидкости не будет заполнено её насыщенным паром. Между жидкостью и её насыщенным паром существует динамическое равновесие: число молекул, покидающих жидкость в единицу времени, равно числу молекул пара, возвращающихся за это же время в жидкость. Для жидкостей одного состава каждой температуре соответствует строго определённое давление её насыщенного пара. Отображённые в графическом виде эти зависимости носят название кривые равновесия и являются важнейшими характеристиками состояния вещества. Позднее они понадобятся при рассмотрении процессов дистилляции и ректификации.
Кипением называют процесс испарения жидкости не только с её свободной поверхности, но и по всему объёму внутрь образующихся в ней пузырьков пара [29]. За счёт интенсивного испарения пара внутрь пузырьков они растут, всплывают на поверхность и содержащийся в них насыщенный пар переходит в паровую фазу над жидкостью. Спокойное испарение жидкости переходит в кипение тогда, когда давление насыщенного пара внутри пузырьков в жидкости начинает превышать внешнее атмосферное давление на жидкость. Температура, при которой происходит кипение жидкости, находящейся под постоянным давлением, называется температурой кипения. Температуру, при которой жидкость кипит при атмосферном давлении 760 мм рт. ст., принято называть нормальной температурой кипения. Она является важнейшим параметром чистого вещества в жидком виде.
Если пар кипящей жидкости свободно выходит на воздух, то её температура остаётся постоянной. При этом всё количество подводимого тепла уходит на парообразование, а интенсивность кипения определяется скоростью подачи тепла. При увеличении внешнего давления температура кипения жидкости увеличивается, при уменьшении – понижается, вплоть до того, что если интенсивно откачивать образующиеся пары, то жидкость закипит даже при комнатной температуре. Этим явлением пользуются при перегонке жидкостей, разлагающихся при высокой температуре [31].
Для поддержания кипения к жидкости необходимо постоянно подводить теплоту, которая расходуется на парообразование, вследствие чего кипение неразрывно связано с теплообменом, при котором теплота постоянно передаётся от поверхности нагрева к жидкости. Поскольку скорость теплообмена имеет конечное значение и не так уж велика, в кипящей жидкости устанавливается определённое распределение температуры: у поверхности нагрева, т.е. на дне перегонного сосуда, жидкость несколько перегрета относительно температуры кипения. Величина перегрева зависит как от физико-химических свойств самой жидкости, так и от качества граничащих с ней твёрдых поверхностей. Тщательно очищенные от растворённых газов жидкости при соблюдении особых мер предосторожности можно перегреть в сосудах из гладкого кварцевого стекла на десятки градусов без закипания. Но если такая перегретая жидкость, в конце концов, закипает, то процесс кипения протекает настолько бурно, что напоминает взрыв. Вскипание сопровождается расплёскиванием жидкости и гидравлическими ударами, которые могут вызвать разрушение сосудов58. Так как теплота перегрева расходуется на парообразование, то жидкость быстро охлаждается до температуры насыщенного пара. На практике такое поведение перегретой жидкости называют толчками. При перегонке жидкости с целью разделения на отдельные фракции они, кроме опасности разрушения аппаратуры, нежелательны ещё и тем, что могут забросить жидкие продукты из куба прямо в холодильник, сведя на нет результаты перегонки.
Перегрев объясняется тем, что для образования первоначальных зародышей для парообразования – микроскопических пузырьков газа необходимо преодолеть силы взаимного сцепления молекул внутри жидкости. Однако, при наличии так называемых центров кипения – пузырьков, образующихся из растворённых в жидкости газов и газов, адсорбированных в порах, складках и повреждениях стенок сосудов, а также на мельчайших твёрдых взвешенных в жидкости частицах, перегрев не превышает нескольких долей градуса и кипение имеет устойчивый спокойный характер. В обиходе такое кипение, например, воды в чайнике, называют пузырчатым кипением.
С увеличением температуры поверхности нагрева растворённые в жидкости газы начинают интенсивно выделяться, число центров кипения возрастает, всё большее количество образовавшихся пузырьков всплывает на поверхность жидкости, вызывая её интенсивное перемешивание. Это приводит к значительному росту теплового потока от поверхности нагрева к кипящей жидкости. Соответственно возрастает и количество образующегося пара.
При достижении максимального (критического) значения теплового потока начинается второй режим кипения – переходный. При этом режиме значительная доля поверхности нагрева покрывается сухими пятнами из-за расширяющегося взаимного слияния пузырьков пара. Теплоотдача и скорость парообразования в этих местах резко снижаются, т.к. пар обладает меньшей теплопроводностью, чем жидкость. Наступает кризис кипения. Когда же вся поверхность нагрева обволакивается тонкой паровой плёнкой, наступает третий – плёночный режим кипения. При нём теплота от раскалённой поверхности передаётся к жидкости через паровую плёнку путём теплопроводности и излучения. На практике плёночный режим кипения может быть достигнут, когда при дробной перегонке жидкость, уже освобождённая от взвешенных частиц и растворённых газов при предыдущей перегонке, подвергается нагреву вмонтированными в перегонный куб тепло-электронагревателями – ТЕНами с несообразно большой мощностью. В этом случае прогорание стенки ТЕНа не менее опасно, чем прогорание стенки котла паровой турбины.
Наиболее подходящий для реализации поставленной цели пузырчатый режим кипения, исключающий возникновение толков перегоняемой жидкости в нагреваемом сосуде, может быть достигнут несколькими путями. В лабораторной практике, когда для перегонки используется жаропрочная стеклянная колба с шарообразным дном, применяются так называемые кипелки [31]. Они представляют собой очень тонкие стеклянные трубочки наподобие трубочек, используемых в ртутных медицинских термометрах, запаянные с одного конца. Эти трубочки помещаются в колбу под углом к горизонтали открытым концом вниз, чему способствует форма дна колбы. При нагревании жидкости в колбе воздух в трубочках нагревается, расширяется и крошечными пузырьками выходит наружу, образуя центры парообразования. Практическое использование таких кипелок для решения поставленной задачи представляется нецелесообразным, т.к. дно перегонных аппаратов плоское и надёжно установить на нём хрупкие кипелки под некоторым углом, да ещё в условиях бурлящей при кипении жидкости просто невозможно.
Другой способ организации пузырчатого кипения заключается в том, что в куб перегонного аппарата вносятся твёрдые вещества с развитой поверхностью, на которой адсорбированы кислород, азот и другие, содержащиеся в воздухе газы. Выделяющиеся при нагревании микропузырьки этих газов будут служить центрами парообразования. Примером таких веществ являются битые кусочки старой доброй общепитовской тарелки из керамики, исключая её глазурованные участки59. Недостаток этого способа состоит в его затратности – кусочки керамики так пропитываются остатками жидкости в перегонном кубе (преимущественно сивушными маслами), что полностью избавиться от неприятного запаха невозможно даже путём прокаливания их на огне.
Наконец, третий способ предотвращения перегрева, связанной с ним задержкой кипения и последующими толчками, состоит в организации перегрева в ограниченном объёме. Для этого на дно перегонного аппарата помещают или неглубокие металлические колпачки с зазубренными краями дном вверх, или диск с выпуклой канавкой – так называемый «сторож» для кипячения молока. В этом случае перегрев жидкости происходит в малом объёме между, поверхностью нагрева и дном колпачка (или выпуклостью в диске). Недостатком применения колпачков является их самопроизвольное опрокидывание в бурлящей жидкости зазубренными краями вверх. Диск-«сторож» трудоёмок в изготовлении, т. к. канавка должна быть отформована на обеих его сторонах, тем более, как будет показано ниже, в этом нет никакой необходимости.

