Полная версия
Энциклопедия долгой и здоровой жизни
К трем годам у ребенка формируется уже взрослый состав микрофлоры, который остается относительно стабильным на протяжении жизни. Однако это не значит, что мы не можем на него повлиять. Калорийность питания, состав диеты, воспалительные процессы и старение постоянно меняют соотношение различных видов бактерий.
Иммунное старение, хроническое воспаление и повышенный уровень гормонов стресса с возрастом приводят к снижению числа полезных бактерий, особенно бифидобактерий. Это создает благоприятные условия для развития воспалительных заболеваний кишечника.
Даже небольшие изменения в питании могут существенно повлиять на наших микроскопических помощников. Например, увеличение калорийности рациона в полтора раза способно за несколько дней увеличить количество воспалительных бактерий на 20 %. Но еще более важен состав пищи. Преобладание животной пищи приводит к размножению бактерий, устойчивых к желчи и способных расщеплять белки. Некоторые из этих микроорганизмов могут способствовать развитию воспалительных заболеваний кишечника и даже рака печени.
Роль микрофлоры в регуляции аппетита и пищевого поведения оказалась намного значительнее, чем считалось раньше. Бактерии, которые преобладают при питании животной пищей, снижают выработку гормона голода грелина. А те, что живут на растительной диете, наоборот, поддерживают здоровый аппетит. Недавно ученые обнаружили, что даже обычная кишечная палочка способна влиять на выработку гормонов, регулирующих насыщение, – энтероглюкагона и пептида YY.
Особенно важны для наших микробных помощников пищевые волокна. Хотя наш организм не может их переварить, бактерии превращают их в полезные вещества, обеспечивая нам до 15 % необходимой энергии. Всемирная организация здравоохранения рекомендует потреблять 25–35 граммов волокон ежедневно. При их недостатке уменьшается количество бактерий, производящих короткоцепочечные жирные кислоты, что может привести к различным проблемам со здоровьем.
Известный итальянский исследователь Клаудио Франчески особо отмечает роль короткоцепочечных жирных кислот, которые образуются при переработке пищевых волокон бактериями. Эти вещества не только служат источником энергии для клеток кишечника, но и участвуют в синтезе жирных кислот и глюкозы в печени, регулируют воспаление, контролируют аппетит через воздействие на пептид YY и поддерживают здоровую кислотность в кишечнике.
Бутират – одна из таких кислот – заслуживает особого внимания. Он регулирует работу множества генов, обладает противоопухолевым действием и помогает бороться с возрастной мышечной атрофией. В экспериментах бутират продлевал жизнь дрозофилам и мышам с ускоренным старением, а также улучшал память у мышей с признаками болезни Альцгеймера. Примечательно, что у столетних долгожителей уровень бутирата и других противовоспалительных короткоцепочечных жирных кислот в кишечнике значительно выше, чем у остальных людей.
Помимо производства полезных веществ бактерии помогают нам получать необходимый белок. В присутствии пищевых волокон они синтезируют белок и обеспечивают до 20 % циркулирующих в крови незаменимых аминокислот – лизина и треонина. При этом лизин служит сырьем для производства бутирата, создавая благоприятный цикл взаимодействия между нашим организмом и микрофлорой.
Наши кишечные помощники также делают более доступными для усвоения полифенолы – мощные противовоспалительные и антиоксидантные вещества из растительной пищи. В основном биофлавоноиды усваиваются трудно, но бактерии превращают их в фенольные кислоты, которые легко усваиваются организмом и оказывают благотворное влияние на здоровье.
Однако не все продукты жизнедеятельности бактерий полезны. Помимо уже упомянутого крезола стоит обратить внимание на то, что при расщеплении белков животного происхождения могут образовываться токсичные и канцерогенные вещества: аммиак, триметиламин-N-оксид, различные фенолы и сульфиды.
Аммиак образуется при расщеплении белков кишечными бактериями через процесс деаминирования аминокислот. При избытке белковой пищи и недостатке клетчатки его концентрация может значительно повышаться. Повышенный уровень аммиака вызывает утомляемость, головные боли, может нарушать когнитивные функции. В высоких концентрациях он токсичен для клеток печени и мозга, способствует развитию печеночной энцефалопатии.
Триметиламин-N-оксид (ТМАО) образуется в результате двухступенчатого процесса: сначала кишечные бактерии преобразуют холин и L-карнитин (содержащиеся преимущественно в красном мясе и яйцах) в триметиламин, который затем в печени превращается в ТМАО. Повышенный уровень ТМАО увеличивает риск сердечно-сосудистых заболеваний, способствуя возникновению атеросклеротических бляшек и тромбообразованию.
Фенолы (в том числе индол и скатол) образуются при бактериальном расщеплении аминокислот триптофана и тирозина. В высоких концентрациях они оказывают токсическое действие на клетки кишечника, могут вызывать воспаление и повышать риск развития колоректального рака. Кроме того, они создают дополнительную нагрузку на печень, которая должна их обезвреживать.
Сульфиды образуются при бактериальной ферментации серосодержащих аминокислот (метионина и цистеина). Избыток сульфидов повреждает клетки кишечного барьера, может вызывать воспаление и повышать проницаемость кишечной стенки. Они также способны нарушать энергетический метаболизм клеток кишечника.
Важно отметить, что все эти вещества – естественные продукты метаболизма и проблемы возникают только при их избыточном накоплении. К счастью, при достаточном потреблении пищевых волокон и устойчивого крахмала (амилозы) их негативное влияние существенно снижается. Волокна ускоряют прохождение пищи через кишечник и способствуют размножению полезных бактерий, которые предпочитают углеводы белкам.
Примечательно, что различные виды белков по-разному влияют на микрофлору. Белки красного мяса чаще расщепляются с образованием вредных веществ, чем белки рыбы. Молочные белки тоже дают много аммиака. А вот растительные белки, особенно из бобовых, способствуют росту полезных бифидо- и лактобактерий, которые производят полезные короткоцепочечные жирные кислоты.
Существенное влияние на микрофлору оказывают и жиры. Большое количество насыщенных жиров, будь то животные жиры или пальмовое масло, обедняет состав микрофлоры и снижает производство полезных короткоцепочечных жирных кислот. Кроме того, жирная пища усиливает выработку желчи, избыток которой может способствовать развитию рака толстой кишки.
Интересно, что некоторые продукты могут защищать нас от вредного воздействия определенных веществ. Уже упоминалось, что холин и L-карнитин, которых много в мясе и яйцах, под действием кишечных бактерий могут превращаться в вещества, способствующие атеросклерозу. Однако компоненты средиземноморской диеты – оливковое масло первого отжима, красное вино, винный (бальзамический) уксус – содержат соединение (3,3-диметил-1-бутанол), которое блокирует этот процесс. Возможно, именно поэтому французы, потребляющие много жирной пищи, реже страдают от сердечно-сосудистых заболеваний.
Особого внимания заслуживает роль микробиома в регуляции иммунной системы. Кишечные бактерии производят специальные соединения, которые поддерживают целостность кишечного барьера – важнейшего компонента иммунной защиты. Нарушение этого барьера может привести к развитию пищевых аллергий, аутоиммунных заболеваний и хронических воспалительных процессов. Важно помнить и о стрессе, который может существенно влиять на иммунитет. Хронический стресс приводит к выбросу кортизола и других гормонов стресса, которые изменяют среду обитания кишечных бактерий и могут способствовать размножению потенциально опасных микроорганизмов.
Роль микробиома в регуляции иммунитета оказалась намного значительнее, чем считалось ранее. Исследования последних лет показывают, что кишечные бактерии не просто помогают переваривать пищу, но и активно тренируют нашу иммунную систему с первых дней жизни. Они учат иммунные клетки различать безопасные и опасные микроорганизмы, регулируют воспалительные процессы и даже влияют на эффективность вакцинации.
Особенно интересна роль короткоцепочечных жирных кислот в иммунной регуляции. Эти вещества, производимые бактериями при переработке пищевых волокон, стимулируют производство регуляторных Т-клеток – особых иммунных клеток, предотвращающих чрезмерные воспалительные реакции и аутоиммунные процессы. Именно поэтому люди, потребляющие много клетчатки, реже страдают от аллергических и аутоиммунных заболеваний.
Связь между состоянием микрофлоры и психическим здоровьем становится все более очевидной. Новейшие исследования показывают, что определенные виды бактерий могут защищать от депрессии и тревожных расстройств. Например, бактерии родов Lactobacillus и Bifidobacterium способны снижать уровень кортизола – гормона стресса, а также увеличивать выработку противовоспалительных соединений, защищающих нервные клетки от повреждения.
Особенно интересны исследования, показывающие связь между составом микробиома и риском развития нейродегенеративных заболеваний. Некоторые виды бактерий способны производить соединения, защищающие нейроны от гибели и снижающие образование токсичных белковых агрегатов, характерных для болезней Альцгеймера и Паркинсона.
Последние исследования в области микробиома и долголетия открывают захватывающие перспективы. Ученые обнаружили, что у долгожителей, особенно у тех, кто перешагнул столетний рубеж, наблюдается уникальный состав микрофлоры. Их кишечник населен особыми видами бактерий, способными эффективно подавлять воспалительные процессы и защищать от возрастных заболеваний.
Особый интерес представляют исследования, показывающие, что трансплантация микробиоты от молодых особей мышей старым может замедлять процессы старения и улучшать когнитивные функции. Хотя большинство этих экспериментов пока проведены только на животных, они открывают новые перспективы для разработки методов продления здорового долголетия.
Микробиом также играет ключевую роль в метаболизме различных соединений, связанных с долголетием. Например, некоторые бактерии способны производить уникальные молекулы, активирующие сиртуины – белки, известные своей способностью замедлять старение.
Новейшие исследования подчеркивают важность индивидуального подхода к поддержанию здоровья микробиома. То, что полезно для одного человека, может оказаться неэффективным для другого. Это связано с генетическими особенностями, образом жизни, составом микробиома, историей приема антибиотиков и многими другими факторами.
Развитие технологий секвенирования ДНК позволяет точно определять состав микрофлоры и отслеживать его изменения. На основе этих данных можно разрабатывать персонализированные рекомендации по питанию и образу жизни, направленные на оптимизацию состава микробиома для каждого конкретного человека.
Будущее исследований микробиома обещает множество новых открытий. Ученые работают над созданием умных пробиотиков, способных целенаправленно воздействовать на определенные процессы в организме. Разрабатываются новые методы анализа взаимодействия между различными видами бактерий и их влияния на здоровье человека. Все это приближает нас к пониманию того, как использовать потенциал микробиома для продления здоровой жизни.
Глава 4
Меньше ешь – дольше проживешь
В современном мире, где искусственное освещение позволяет человеку быть активным круглосуточно, а доступность пищи создает соблазн постоянных перекусов, естественные циклы питания и отдыха часто нарушаются. Это приводит к серьезным последствиям для здоровья: от метаболических нарушений до ускоренного старения. Однако наука предлагает различные подходы к восстановлению здорового режима питания, и один из наиболее изученных – это практика голодания в различных его формах.
История научного изучения влияния ограничительных диет на здоровье и долголетие началась в 1934 году со знаменитого эксперимента в Корнелльском университете. Исследователи обнаружили удивительный факт: лабораторные мыши могли жить вдвое дольше ожидаемого срока при условии содержания на низкокалорийной диете, сбалансированной по питательным веществам, чтобы избежать недостатков микронутриентов. Это открытие положило начало масштабным исследованиям влияния различных режимов питания на продолжительность жизни и здоровье.
В последующие десятилетия ученые подтвердили положительное влияние умеренного ограничения калорий (20–40 % от нормы) на множестве модельных организмов: от одноклеточных дрожжей до приматов. Механизмы этого явления многообразны: снижение температуры тела и темпов метаболизма, уменьшение образования свободных радикалов, повышение чувствительности тканей к инсулину, перезапуск самообновления стволовых клеток, оптимизация работы нейроэндокринной и симпатической нервной систем.
Современные исследования показывают, что ограничительная диета запускает целый каскад позитивных метаболических и клеточных изменений. Снижается уровень окислительных повреждений и воспаления, оптимизируется энергетический метаболизм – организм переключается с утилизации глюкозы на использование жировых запасов. Активизируются защитные механизмы клеток, включая аутофагию – процесс разрушения старых и поврежденных клеточных структур (рис. 2).
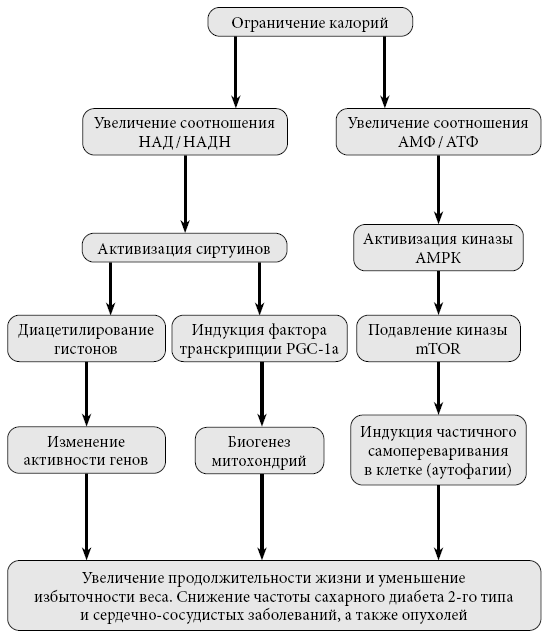
Рис. 2. Механизмы влияния ограничительной диеты на здоровье и долголетие
Особую роль в эффектах низкокалорийной диеты играет печень, которая при голодании выделяет фактор роста фибробластов-21 (FGF-21). Этот гормон привлек внимание исследователей после обнаружения его способности значительно продлевать жизнь подопытных мышей при искусственном повышении его уровня. Дополнительную пользу показала низкокалорийная диета, обогащенная полифенолами, которые содержатся в гранатах, помидорах, голубике и других ягодах. Они положительно влияют на сосуды и снижают уровни воспаления, стимулируют стрессоустойчивость клеток.
Влияние ограничения калорий на продолжительность жизни оказалось сложнее, чем предполагалось изначально. Масштабное исследование Национального института старения США поставило под сомнение универсальность этого эффекта. Анализ данных показал, что предполагаемые преимущества низкокалорийной диеты могли быть связаны не столько с самим ограничением, сколько с предотвращением вредных последствий переедания в контрольных группах.
Новое масштабное исследование The Jackson Laboratory 2024 года, охватившее почти тысячу генетически разнообразных мышей, внесло дополнительную ясность в этот вопрос. Ученые обнаружили, что именно сокращение калорийности рациона, а не периодическое голодание оказывает решающее влияние на продолжительность жизни. Особую ценность исследованию придает использование генетически разнообразной популяции мышей, что делает результаты более применимыми к реальным условиям. Интересно, что долгожители среди подопытных мышей демонстрировали меньшую потерю веса, сохраняя энергетический баланс и иммунитет. Это открытие указывает на возможную ключевую роль стрессоустойчивости в механизмах долголетия.
Прорыв в нашем понимании эффектов голодания совершил Джозеф Такахаши. Его эксперименты подтвердили, что 30-процентное сокращение калорий увеличивает продолжительность жизни мышей на 10 %. Однако еще более впечатляющий результат – увеличение продолжительности жизни на 35 % – был достигнут при комбинации ежедневного периода голодания с приемом пищи в определенное время суток. Примечательно, что эти эффекты не зависели от массы тела животных, что указывает на фундаментальную роль циркадных ритмов в процессах старения.
Однако вернемся к человеку. Влияние возрастных изменений на метаболизм человека требует особенно тщательного подхода к вопросам питания после 40 лет. В этом возрасте происходят существенные изменения на клеточном уровне: увеличивается количество дисфункциональных митохондрий – клеточных органелл, отвечающих за производство энергии. Это приводит к замедлению метаболизма и, как следствие, к повышенной склонности к накоплению жировой ткани даже при сохранении привычного режима питания.
Поддержание здоровой массы тела в этот период становится более сложной задачей. Простое сохранение прежнего рациона уже неэффективно – организм нуждается в пересмотре общей калорийности питания. При этом критически важно сохранить полноценность рациона, обеспечивая поступление всех необходимых нутриентов: белков, жиров, углеводов, витаминов и минералов в оптимальных пропорциях.
Однако снижение калорийности требует исключительно выверенного подхода. Слишком резкое или чрезмерное ограничение питания может запустить нежелательные процессы катаболизма, при которых организм начинает расщеплять не только жировые запасы, но и мышечную ткань. Более того, недостаточное питание может негативно повлиять на минеральную плотность костной ткани, что особенно опасно в возрасте, когда естественные процессы костного ремоделирования уже замедлены.
Таким образом, оптимальная стратегия заключается в постепенном контролируемом снижении калорийности при обязательном сохранении достаточного количества белка для поддержания мышечной массы и необходимого уровня кальция и витамина D для здоровья костной ткани. Этот подход позволяет достичь здорового баланса между снижением избыточного веса и сохранением важнейших структур организма.
В современной практике выделяют несколько основных видов ограничительного питания. Периодическое голодание подразумевает полный отказ от пищи (но не от воды) на определенное время. Интервальное голодание ограничивает время приема пищи в течение суток. Существует также практика ограничения калорийности питания в определенные дни недели и различные вариации постной диеты.
Исследователь Вальтер Лонго из Университета Южной Калифорнии, посвятивший многие годы изучению влияния ограничительных диет на здоровье и долголетие, выделяет два основных типа голодания. Прерывистое голодание предполагает отказ от пищи примерно на сутки с последующим нормальным питанием в течение 1–2 дней. Периодическое (пролонгированное) голодание длится от двух и более дней с перерывами между циклами не менее недели.
Современные исследования на грызунах показали множество положительных эффектов прерывистого голодания: активизация нервных связей, улучшение когнитивных функций, повышение чувствительности тканей к инсулину, снижение артериального давления и частоты сердечных сокращений. Также отмечено замедление развития опухолей, предотвращение воспалительных заболеваний, включая дерматиты, стимуляция регенерации клеток крови и укрепление иммунной системы.
Одно из важных преимуществ прерывистого голодания перед постоянной низкокалорийной диетой – способность уменьшать долю жировой массы тела без потери мышечной массы. После 24-часового голодания в организме млекопитающих и человека происходит метаболический сдвиг: ткани начинают меньше использовать глюкозу и больше полагаться на кетоновые тела, образующиеся при расщеплении жировых запасов.
Новейшие исследования показывают эффективность более щадящих режимов питания, не требующих полного отказа от еды, таких как употребление 500–600 ккал в день на протяжении двух дней в неделю. У людей с избыточной массой тела, следовавших такому режиму в течение шести месяцев, наблюдалось снижение количества висцерального жира, артериального давления и увеличение чувствительности к инсулину. Схожие результаты были получены при голодании через день на протяжении двух-трех недель.
В такие постные дни (например, вторник и пятница) рацион на 500–600 ккал можно построить следующим образом.
Завтрак (200 ккал): овсяная каша на воде с добавлением льняного масла (1 чайная ложка), горсть ягод и половина банана. Можно добавить корицу для вкуса. Такой завтрак обеспечит медленные углеводы и полезные жиры для длительного чувства сытости.
Обед (250 ккал): тарелка постного борща или овощного супа с фасолью, заправленного небольшим количеством оливкового масла. К супу можно добавить ломтик цельнозернового хлеба. Бобовые в составе супа обеспечат необходимый растительный белок.
Ужин (150 ккал): большая порция салата из свежих овощей (помидоры, огурцы, болгарский перец, листовые салаты) с добавлением нута или чечевицы, заправленный лимонным соком и небольшим количеством оливкового масла. Нут или чечевица добавят белок, который особенно важен даже в разгрузочные дни.
На протяжении дня можно пить воду без ограничений, травяные чаи, зеленый чай. При сильном чувстве голода допустимо съесть яблоко или грушу между основными приемами пищи, но нужно учитывать эти калории в общем подсчете.
В последние годы особое внимание привлекает так называемая диета римского воина, или one meal a day (OMAD), при которой все дневное потребление калорий происходит в течение одного приема пищи. Исследования показывают, что такой режим может способствовать улучшению метаболических показателей и снижению воспалительных процессов в организме, хотя требуются дополнительные исследования для подтверждения его долгосрочной безопасности и эффективности.
Научный консенсус относительно оптимального времени единственного приема пищи склоняется в пользу раннего употребления основной части калорий. Исследования циркадных ритмов показывают, что чувствительность к инсулину и скорость метаболизма достигают пика в первой половине дня. Употребление большей части калорий до 15:00 способствует более эффективному усвоению питательных веществ и лучшему контролю уровня глюкозы в крови.
Вечерний прием пищи, особенно после захода солнца, может нарушать естественные метаболические ритмы организма. Исследования демонстрируют, что поздний прием пищи связан с повышенным риском набора веса и метаболических нарушений даже при соблюдении того же калоража. Это объясняется снижением активности ферментов пищеварения и замедлением метаболизма в вечерние часы.
Однако важно учитывать индивидуальные особенности образа жизни и рабочего графика. Если утренний прием пищи невозможен по объективным причинам, рекомендуется максимально приблизить время единственного приема пищи к середине дня, избегая позднего вечернего питания.
Циклы пролонгированного голодания (от двух дней и более) с недельными перерывами между ними показали эффективность в защите клеток от токсинов, повышении чувствительности опухолей к терапии и улучшении регуляции уровней глюкозы и инсулина. Важный эффект такого голодания состоит в активизации аутофагии – процесса очищения клеток от накопившегося мусора.
Хотя пролонгированное голодание приводит к временному снижению общей массы тела, массы печени и количества лейкоцитов в крови, возобновление питания запускает мощные процессы регенерации как в печени, так и в иммунной системе. Клинические исследования показали эффективность такого подхода при лечении ревматоидного артрита, где голодание продолжительностью 1–3 недели значительно уменьшало симптомы заболевания.
Отдельного внимания заслуживает временное ограничение приема пищи, или time-restricted feeding (TRF). При этом подходе прием пищи ограничивается определенным временным окном (обычно менее 12 часов) без изменения качественного или количественного состава рациона. Исследования на мышах показали, что даже при высокожировой диете ограничение времени приема пищи 8–12 часами в день приводило к улучшению суточных ритмов и предотвращало развитие метаболических заболеваний.
Современные исследования демонстрируют, что при временном ограничении питания наблюдаются позитивные изменения в обмене веществ: улучшается выведение избытка холестерина с желчными кислотами, активизируется бурая жировая ткань, усиливается бета-окисление жирных кислот, снижается выработка глюкозы печенью и уменьшаются воспалительные процессы в белой жировой ткани.
Важный аспект изучения различных форм голодания – роль кетоновых тел. Эти соединения не только служат маркерами расщепления жиров, но и обладают противовоспалительными и нейропротекторными свойствами. Наряду с глюкозой это единственные молекулы, способные обеспечивать энергией нейроны, что объясняет их положительное влияние на работу мозга и противодействие депрессии.
Недавние исследования показали, что один из видов кетоновых тел – бета-гидроксибутират – способен увеличивать продолжительность жизни экспериментальных животных. Интересно, что наиболее быстро кетоновые тела образуются из среднецепочечных насыщенных жирных кислот, которыми богато кокосовое масло, что частично объясняет его положительное влияние на нервную систему.
Современная наука также обратила внимание на влияние различных макронутриентов на здоровье и долголетие. При ограничительных стилях питания дело может быть не в калориях как таковых, а в ограничении определенных нутриентов. Масштабное исследование, изучившее влияние 25 различных диет на мышей, показало, что наилучшие показатели продолжительности жизни и метаболического здоровья наблюдались при диетах с низким содержанием белка и высоким содержанием медленных углеводов.






