
Полная версия
О строении вещества простым языком

Сергей Гермаковский
О строении вещества простым языком
Предисловие автора
Нам говорили, что физика и химия – 2 разные науки. А что, если это неправда? В школе нас учили, что есть химия и физика. Химия – наука о веществах, а физика – наука о неживой природе. Однако, если копнуть глубже, это одна и та же наука.
В основе всего лежит физика. Она объясняет механизмы всех окружающих нас явлений. Химия базируется на физике, но рассматривает вещи, которые не рассматривает физика.
Изучая в школе физику и химию, часто встречал противоречия. Например, строение атома на уроках физики и химии преподавали по-разному. На физике учат, что электроны вращаются вокруг ядра. На химии – атом состоит из орбиталей и энергетических уровней, а электрон вообще волна. Где правда? А правда на пересечении этих наук. Эта книга – попытка объединить физику и химию.
Книга начинается с базовых понятий: агрегатных состояний и атомно-молекулярного учения. Вероятно, вы уже знакомы с этим, но прочитать рекомендую. Скорее всего найдете много новых фактов.
Далее мы рассматриваем строение атома. Начиная с его открытия и заканчивая квантовыми представлениями о его строении. Чтобы облегчить понимание квантового строения вещества, есть глава, где коротко разбираются основные понятия квантовой механики.
После рассмотрения атома мы переходим к рассмотрению строения веществ: молекул и твердых тел.
Заканчивается книга описанием физических свойств веществ. Мы не только разберем какие они бывают, но и рассмотрим их природу и связь со строением вещества.
Приятного прочтения!
Агрегатные состояния
Все объекты, которые нас окружают, называют физическими телами. Тела состоят из веществ. Вещества состоят из частиц. Любые вещества могут находиться в 3 агрегатных состояниях: газообразное, жидкое, твердое. Также выделяют отдельное агрегатное состояние – плазма.
Агрегатное состояние тела зависит от давления и температуры.
Температура – это степень нагретости тела. Температуру измеряют в градусах. Нам привычнее пользоваться градусами Цельсия. Кроме градусов Цельсия существуют градусы Кельвина, Фаренгейта и другие. Минимально возможная температура – 0 К (ноль Кельвинов). Эту температуру называют абсолютным нулём. Если выразить её в градусах Цельсия получится минус 273,16°С. В лабораториях удалось получить только температуру на несколько миллионных долей выше абсолютного нуля. Термодинамические законы гласят, что невозможно получить температуру равную абсолютному нулю.
Давление – сила, давящая на 1 м2 поверхности тела. Давление измеряют в Паскалях (Па), Барах (бар) или в Миллиметрах ртутного столба (мм рт. ст.). Когда говорят про атмосферное давление, имеют ввиду силу, с которой атмосфера давит на поверхность Земли. Нормальное атмосферное давление при температуре 0°C равно 101 325 Па, 1,01 бар или 760 мм. рт. ст.
Изменение давления и/или температуры влияет на агрегатное состояние тела. Разберем, чем эти агрегатные состояния отличаются друг от друга.
Газообразное состояние
Газообразные вещества мы встречаем каждый день. Воздух – смесь разных газов: азота (N2), кислорода (O2), аргона (Ar) и углекислого газа (CO2).
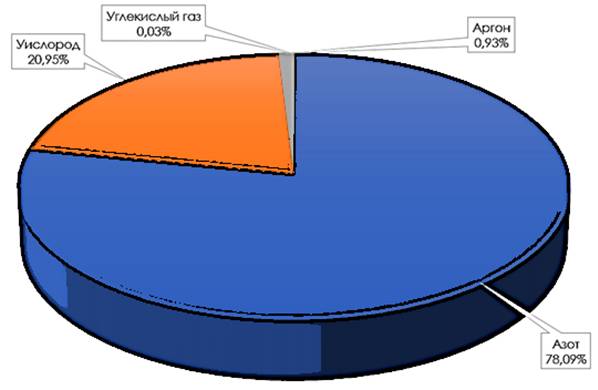
Состав воздуха
Газовая плита на кухне работает на природном газе, состоящем в основном из метана (CН4) и других газов.
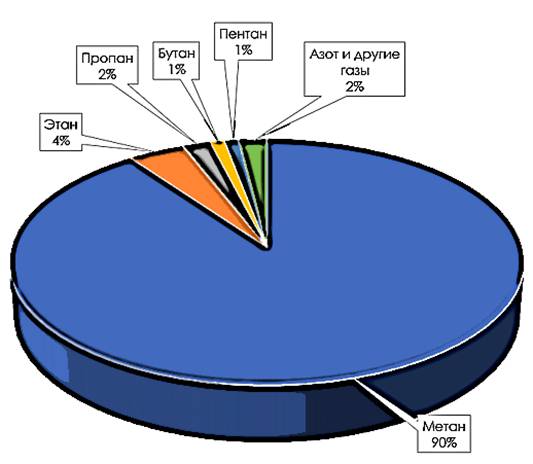
Состав природного газа
Вещества состоят из частиц. Частицы притягиваются друг к другу, это называют взаимодействием между частицами.
Агрегатные состояния отличаются расположением частиц, взаимодействием между частицами и их подвижностью.
Частицы в газообразных веществах расположены далеко друг от друга. Расстояние между двумя ближайшими частицами гораздо больше размера самих частиц. Взаимодействие между частицами слабое. Движутся эти частицы беспорядочно и с очень большой скоростью. Такое строение газов придает им определенные свойства.
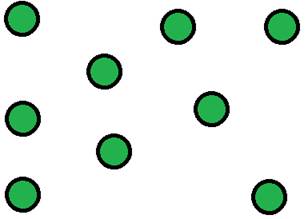
Движение и расположение частиц в газах
Газы не имеют ни объема, ни формы, и занимают всё пространство, в которое они попадают. Вспомните запах горелых спичек. Если зажечь спичку и потушить, воздух какое-то время будет иметь специфический запах. Это запах сернистого газа (SO2).
Расстояние между частицами в газах велико, поэтому газы сжимаемы.
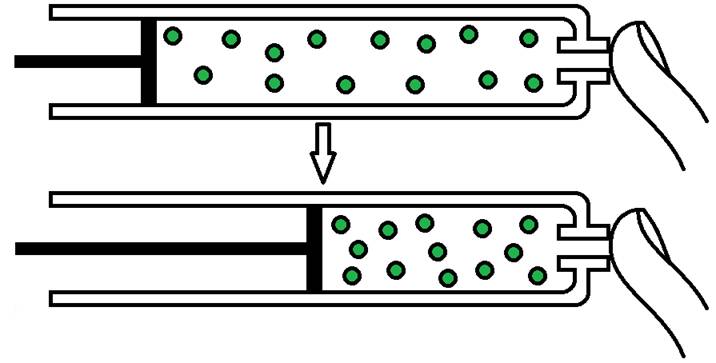
Сжимание газов с помощью поршня
Жидкое состояние
Вода, ртуть, медицинский спирт, ацетон – примеры жидких веществ.
Как и в газах частицы в жидкостях двигаются, свободно, но медленнее. Расстояния между частицами соизмеримы с размерами самих частиц. Силы притяжения между частицами сильнее чем в газах, но слабее, чем в твердых веществах. Такое строение жидкостей придает им характерные свойства.

Расположение частиц в жидкостях
Как и газы, жидкости не имеют формы, поэтому принимают форму сосуда, в который их наливают. В отличие от газов, жидкости имеют объем, поэтому 1 литр воды будет оставаться 1 литром воды в сосуде любого объема.
Жидкости текучие, поэтому растекаются, если их вылить на поверхность. Бывают текучие и вязкие жидкости. К текучим можно отнести воду, к вязким – шампуни и гели для душа.
В отличие от газов, жидкости практически несжимаемы. Расстояния между частицами настолько мало, что сжать их еще сильнее практически нельзя.
Твердое состояние
Соль, сахар, железо, дерево – твердые тела.
Частицы в твердых телах расположены близко друг к другу. Между частицами сильные силы притяжения. Расстояние между частицами значительно меньше размера самих частиц. Частицы не перемещаются, а только колеблются, как маятник. Такое строение придает твердым телам их характерные свойства.

Расположение частиц в твердых телах
Твердые тела имеют не только объем, но и форму. Они бывают хрупкие (стекло) и пластичные (металлы).
Твердые тела несжимаемы. Давление на поверхность такого тела приведет к изменению его формы (деформации) или его разрушению.
Плазма
Существует также 4 агрегатное состояние вещества – плазма. О нём мы поговорим позже.
Фазовые переходы
Из жизни мы знаем, что вода существует во всех трех агрегатных состояниях – газообразном (пар), жидком (обычная вода) и твердом (лёд). Эти состояния могут переходить друг в друга при определенных условиях. При 0°С вода превращается в лёд. При этой же температуре лёд становится жидкостью. При 100°С вода превращается в пар.
Многие вещества существуют во всех агрегатных состояниях. Даже газы можно перевести в жидкое или твердое состояние.
Рассмотрим кислород. В обычных условиях кислород – бесцветный газ. В жидком состоянии кислород голубого цвета, в твердом – это кристаллы синего цвета.

Твердая форма кислорода
Переход одного агрегатного состояния в другое происходит при изменении температуры и/или давления. При уменьшении температуры частицы снижают свою скорость. При повышении температуры – увеличивают.
При повышении давления расстояние между частицами уменьшается. При понижении давления расстояние – увеличивается.
Жидкий кислород получают из воздуха. Сначала увеличивают давление и снижают температуру, чтобы перевести воздух в жидкость. Этот процесс называют сжижение газа. Воздух состоит в основном из азота и кислорода. Температура кипения жидкого азота меньше, чем жидкого кислорода. Получив жидкий воздух нужно отделить азот. Для этого немного повышают температуру так, чтобы азот перешёл в газообразное состояние, а кислород остался в жидком. Газообразный азот отправляют в один сосуд, а жидкий кислород – в другой. Так происходит разделение воздуха на кислород и азот.
Переходы из одного агрегатного состояния в другое называют фазовыми переходами.
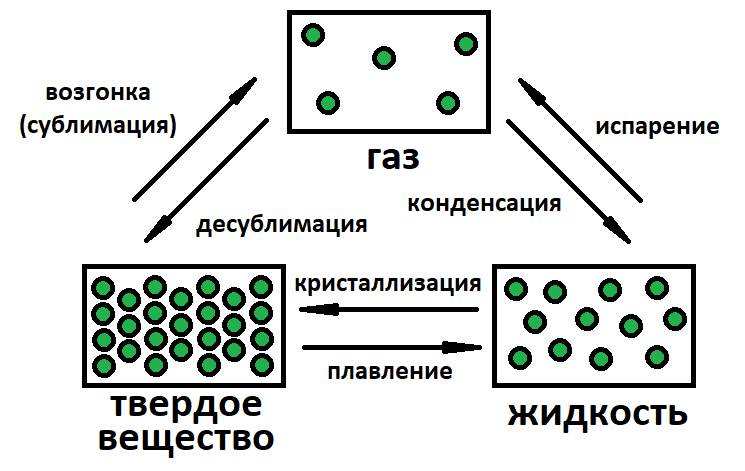
Фазовые переходы
Плавление
Плавление – переход вещества из твердого состояния в жидкое.
У некоторых веществ температура вещества строго определенная: у льда 0°С, у железа 1538°С, у поваренной соли 801°С и т.д. Другие вещества размягчаются и плавятся в интервале температур – пластилин (80 – 85°С), стекло (1200 – 1400°С) и т.д.
В процессе плавления температура вещества постоянна до тех пор, пока вещество не расплавится.
Разберем еще одну важную физическую величину – внутреннюю энергию вещества. Энергия – одно из основных свойств материи. Энергия – это мера движения материи. Внутренняя энергия тела – это сумма всех энергий движения частиц и всех взаимодействий между этими частицами.
Поскольку для плавления тела его необходимо нагреть, то внутренняя энергия тела увеличивается. Это значит, что частицы начинают двигаться с большей скоростью, расстояние между ними увеличивается и вещество переходит в жидкое состояние.
Температура плавления у разных веществ разная. Ее величина зависит от силы притяжения частиц друг к другу. Чем притяжение сильнее, тем большую энергию нужно дать телу, чтобы ослабить силы притяжения и частицы друг от друга отдалились. Нагревая тело, мы передаем ему тепловую энергию, частицы начинают двигаться интенсивнее, это приводит к переходу твердого состояния в жидкое.
Давление мало влияет на температуру плавления и этот переход в целом, так как при плавлении объем тела изменяется не сильно.
Кристаллизация
Кристаллизация – переход из жидкого состояния в твердое. Кристаллизация – процесс обратный плавлению и поэтому происходит при охлаждении тела.
При снижении температуры внутренняя энергия тела уменьшается и частицы замедляются. Их взаимодействие усиливается и тело затвердевает.
Кристаллизация происходит с выделением энергии в виде тепла.
Температура кристаллизации совпадает с температурой плавления. Температура тела при кристаллизации постоянная и не меняется пока вещество не затвердеет полностью.
Давление не оказывает сильного влияния при кристаллизации.
Парообразование
Парообразование – переход вещества из жидкого состояния в газообразное.
Чтобы твердое вещество перешло в газообразное состояние нужно заставить его частицы отдалиться друг от друга. Для этого нужно ослабить их взаимодействие и заставить двигаться быстрее. Как и при плавлении это достигается путем нагревания тела и увеличения его внутренней энергии.
Различают испарение и кипение.
Испарение – это парообразование с поверхности жидкости. Испарение происходит при любой температуре, но зависит от нее.
Испарение – процесс самопроизвольный. Его можно рассматривать как отрывание поверхностного слоя частиц от их общей массы. Частица за частицей отрываются с поверхности тела, пока вся жидкость не перейдет в газообразное состояние.
Хоть испарение происходит и всегда, но оно происходит не всегда одинаково. Его скорость зависит от нескольких факторов:
1) площадь поверхности (чем поверхность больше, тем быстрее с нее испаряется жидкость);
2) температура (чем температура выше, тем вещество испаряется быстрее);
3) движение воздуха и его скорость над поверхностью жидкости (сильный быстрый поток воздуха способствует испарению жидкости);
4) природа жидкости (жидкость, в которой слабое взаимодействие между частицами испаряется быстрее).
Кипение – парообразование по всему объему жидкости. В отличие от испарения, кипение происходит при определенной температуре. У воды температура кипения 100°С, у железа – 2862°С, у поваренной соли – 1465°С, у кислорода – минус 183°С. Температура вещества остается постоянной, пока всё вещество не перейдет в газообразное состояние.
На температуру кипения влияет давление. Увеличение давления приводит к увеличению температуры кипения и наоборот. Сила, давящая на поверхность тела условно мешает частицам отрываться и улетать. Если давление уменьшить, частицам проще отдалиться от друг от друга.
Конденсация
Конденсация – переход вещества из газообразного в жидкое состояние.
Конденсация – обратный процесс парообразования.
Конденсация происходит при охлаждении газа и уменьшении его энергии. Снижение температуры приводит к замедлению частиц и усилению их взаимодействия друг с другом. Температура газа при конденсации не меняется до тех пор, пока весь газ не перейдет в жидкость.
Сублимация (возгонка)
Сублимация – это переход твердого тела в газообразное, без перехода в промежуточное жидкое состояние.
Некоторые вещества способны переходить в газообразное состояние прямо из твердого. Кристаллы йода будут возгоняться и образовывать фиолетовые пары. Твердый углекислый газ, называемый сухим льдом, будет преобразовываться в газообразное состояние при температуре -79°С. Даже обычный лёд способен сублимировать. Доказательством этого может служить факт, что одежда после стирки высыхает на улице даже зимой при морозе.
Сублимацию используют в пищевой промышленности для получения некоторых продуктов питания. На этом явлении основан метод сублимационной сушки при пониженном давлении, которым получают растворимый кофе.
Обратный сублимации процесс – десублимация.
Атомно-молекулярное учение
В прошлой главе мы опирались на термин "частица". Давайте введем более точные определения. Существуют атомы и молекулы.
Идея, что всё состоит из мельчайших неделимых частиц (атомов) возникла еще в Античности. Так называемый Атомизм возник в Древней Греции философами Левкиппом и Демокритом.
Левкипп искал ответ на вопрос "Можно ли мельчайшую частицу материи разделить на еще более мелкие и в итоге прийти к такой частице, разделить которую будет невозможно?". Его ученик Демокрит назвал такие неделимые частички "Атомы". Это слово происходит от греческого слова "Атомос", что переводится как "Неделимый". Демкорит считал, что существует четыре вида атомов: атомы земли, воды, воздуха и огня.
Античные философы дали начало Атомно-молекулярному учению. Основу этого учения заложил М.В. Ломоносов. Он разработал теории строения вещества. Развитие этой теории происходит до сих пор.
Молекулярная теория
Все вещества состоят из молекул. Молекула – мельчайшая частица вещества, определяющая его свойства.
Вещества состоят из молекул. Молекулы состоят из атомов. Стакан воды, содержащий триллионы молекул воды, и одна молекула воды будут обладать одинаковыми свойствами. Если раздробить молекулу, то образованные частицы (атомы) потеряют свойства исходного вещества.
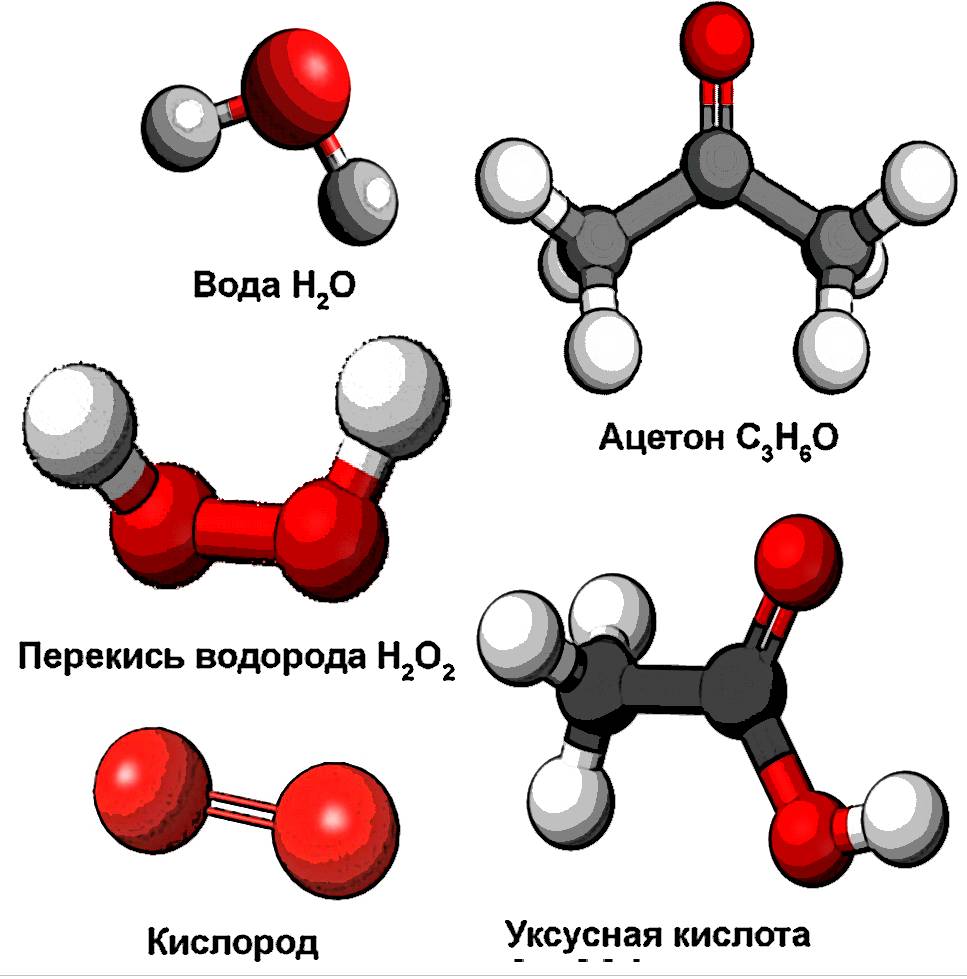
Молекулы некоторых веществ и их строение.
Атомная теория
Атомы – наименьшие химически неделимые частицы вещества. Фразу «Химически неделимые» разберем позже.
Большинство атомов неспособны к самостоятельному существованию, поэтому объединяются в группы атомов – молекулы.
Атомы бывают разные. Они отличаются строением, размерами, массой и другими свойствами. В рамках Атомно-молекулярного учения считается, что эти характеристики определяют свойства атома. Позже стало известно, что главная характеристика атома – заряд ядра. Совокупность атомов с одинаковым зарядом ядра называют химическим элементом.
Движение частиц
Молекулы и атомы находятся в непрерывном беспорядочном движении. Они движутся хаотично. Интенсивность и скорость движения зависит от агрегатного состояния вещества, которое зависит от температуры и давления.
Степень нагретости тела (температура) – результат интенсивности движения этих частиц. Каждая частица обладает энергией и благодаря ей движется. Если запас этой энергии растет, растет и скорость движения частиц. Если запас энергии уменьшается, уменьшается и их скорость. Чем частицы движутся быстрее, тем температура тела выше.
Энергия существует в разных формах: тепловой, световой, звуковой, электрической и т.д. Энергия постоянно перемещается от одного тела к другому. Одни формы энергии переходят в другие. Солнечная энергия переходит в тепловую, когда солнечные лучи нагревают асфальт. В двигателе внутреннего сгорания тепловая энергия переходит в энергию движения (механическую). Механическая энергия переходит в тепловую, когда ладони нагреваются, если их потереть друг об друга. Ядерная энергия переходит в электрическую на атомных электростанциях.
Явления, происходящие с веществами
С веществами происходят физические и химические явления.
При физических явлениях молекулы вещества сохраняются. Обычно при таких явлениях изменяется агрегатное состояние вещества и/или его форма. Лёд тает, вода испаряется, камень рассыпается, проволока гнётся, запах духов распространяется – всё это физические явления.
При химических явлениях разрушаются одни молекулы и образуются другие. Такие явления называются химическими реакциями.
При химической реакции несколько молекул сталкиваются между собой и рассыпаются на атомы. Эти атомы собираются в другие молекулы. Так, одни вещества превращаются в другие.
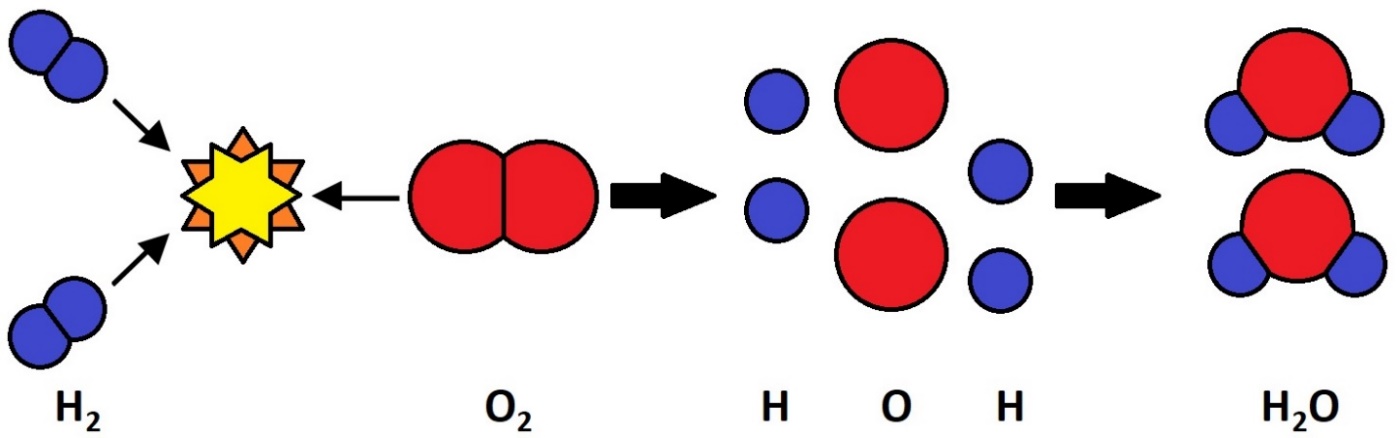
Реакция образования молекулы воды
Разберем пример. С большой скоростью 2 молекулы водорода Н2 врезаются в 1 молекулу кислорода О2. Все 3 молекулы рассыпаются на 4 атома водорода Н и 2 атома кислорода О, после чего объединяются в 2 молекулы воды Н2О.
Важно! Ни при физических, ни при химических явлениях сами атомы не разрушаются. Раздробить атомы можно только в ходе ядерных и термоядерных реакций.
Вещества молекулярного и немолекулярного строения
Читая книгу, вы узнаете о строении различных веществ. Пока что запомните, что одни вещества состоят из молекул (многоатомных или одноатомных), другие из атомов или частиц, называемых ионами. Ионами называют заряженные частицы, которые образуются из атомов или групп атомов. Подробнее о них поговорим, когда будем разбирать строение атома.
Если вещество состоит из молекул, его строение называют молекулярным.
К веществам молекулярного строения относят воду, сахар, кислород, спирт, ацетон. Они состоят из многоатомных молекул, т.е. молекул, образованных двумя и более атомами.
Молекулы газов гелий, неон, аргон, криптон, ксенон, радон состоят из молекул, состоящих из одного атома – одноатомных молекул.
Если вещество состоит не из молекул, а из атомов или ионов, его строение называют немолекулярным.
Одни вещества состоят из одинаковых атомов, другие – из разных. К веществам, состоящим из одинаковых атомов, можно отнести большинство неметаллов: алмаз, графит, сажа, сера. Некоторые вещества состоят из разных атомов, например, горный хрусталь SiO2.
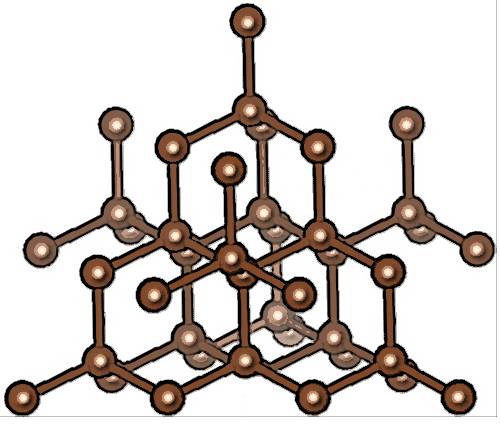
Строение алмаза
Большинство минералов состоят из ионов: мрамор CaCO3, поваренная соль NaCl.
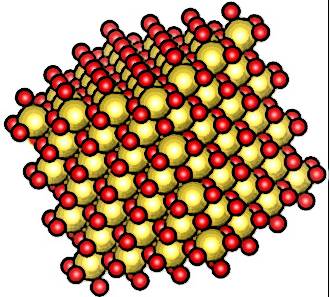
Строение поваренной соли NaCl
Большую часть Атомно-молекулярного учения развил М.В. Ломоносов, но большой вклад внесли и другие физики и химики: Дж. Дальтон, А. Лавуазье, Ж. Пруст, А. Авогадро, Й. Берцелиус, Д. И. Менделеев, А. М. Бутлеров.
Исторические модели атома
Чтобы понимать, как устроен атом, нужно рассмотреть историю его открытия.
Термин «Атом» был введен Демокритом еще во времена античности. Название этой частицы происходит от греческого слова «Атомос», что означает «Неделимый».
Античные философы считали атом неделимой частицей. Это мнение опровергли в конце IX – начале ХХ века.
В конце IX века открыли явление фотоэффекта – испускания частиц (электронов) веществом под действием света. Оказалось, что атом состоит из других частиц, а значит он делимый.
Кроме фотоэффекта в конце IX века была открыта радиоактивность – самопроизвольное испускание частиц и лучей некоторыми атомами. Вывод тот же: атом делимый.
Открытие электронов
В 1749 году Бенджамин Франклин выдвинул гипотезу, что электрический ток – это поток заряженных частиц. В его работах впервые появляются понятия положительных и отрицательных зарядов, батарей, частиц электричества и т.д.
Научное сообщество скептически относилось к существованию электронов. Чтобы развеять этот миф, нужно было провести опыты, доказывающие существование электронов. Для этого нужно было отделить отрицательно заряженные электроны от атомов. Атомы, которые лишились электрона и приобрели положительный заряд стали называть ионами.
Впервые провести такой эксперимент удалось случайно немецкому физику Юлиусу Плюккеру в 1859 году. Он сконструировал установку. В вакуумной трубке по оба конца впаяны проводники – электроды. если к ним приложить электрическое напряжение произойдет интересное явление. От отрицательно заряженного электрода (катода) к положительно заряженному (аноду) будет протекать электрический ток. При этом анод и часть вакуумной трубки вокруг него начинают светиться.
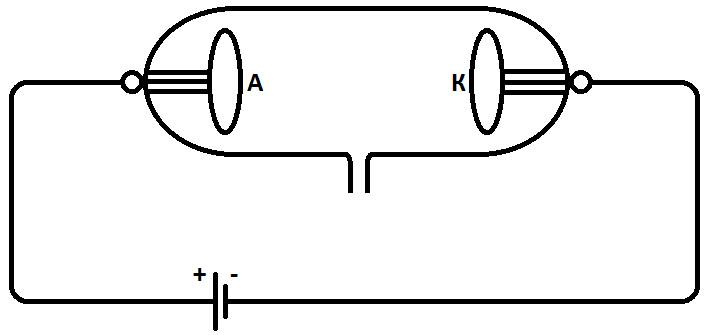
Вакуумная трубка с катодом и анодом
Немецкие ученные Иоганн Гитторф и Эуген Гольдштейн провели такой же опыт и назвали это излучение катодными лучами. В этом же году на основе этого явления была сконструирована первая электронно-лучевая трубка.
В 1874 году английский химик и физик Уильям Крукс выдвинул идею, что катодные лучи – поток отрицательно заряженных частиц. Термин "электрон" был введен ирланским физиком и математиком Джорджем Стони.
В 1897 году английский физик Джозеф Джон Томсон обнаружил, что катодные лучи откланяются электрическим полем. Он измерил массу и заряд этих частиц – электронов.
Опыт Милликена – Иоффе
Опыт Милликена – важный эксперимент по открытию заряду электрона.
В 1909 году Роберт Милликен построил установку. Установка состоит из камеры, в которой находится две металлические пластины, над которыми пульверизатор распылял машинное масло в нутри камеры. В камере появлялся масляной туман.
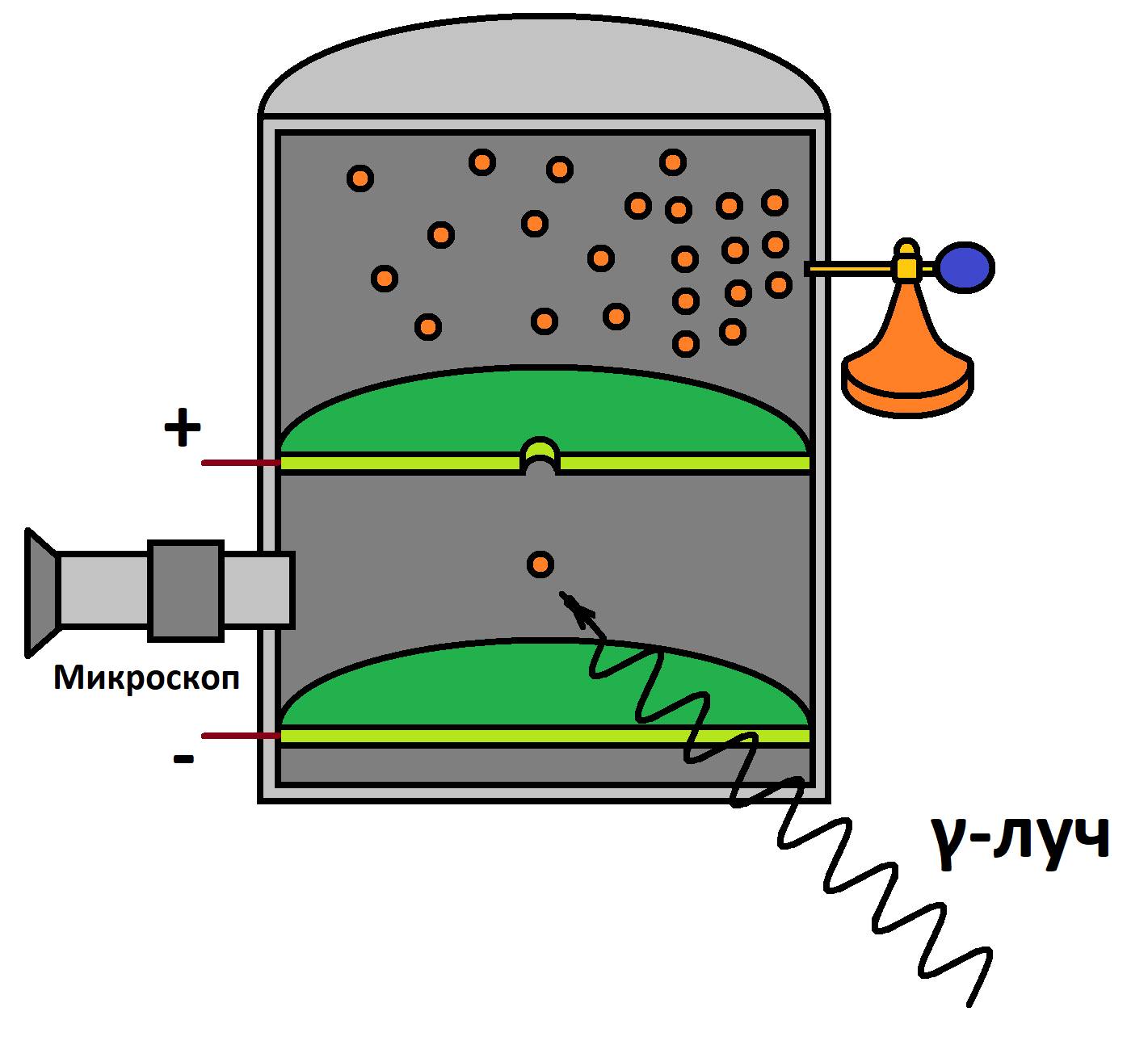
Схема опыта Милликена
В верхней пластине было отверстие, через которое некоторые капли проникали в пространство между пластинами. Милликен наблюдал за каплями с помощью микроскопа. Под действием силы тяжести капли опускались на дно камеры.
Камеру облучали радиоактивными лучами и капли масла приобретали электрический заряд.
Если на пластины подавать напряжение, между ними возникает электрическое поле. Заряженные капли масла реагировали на возникшее электрическое поле и снижали свою скорость.
Используя разность этих скоростей Милликен рассчитал заряд этих капель. Для разных капель были получены разные значения. Наименьшее из этих значений минус 1,6 × 10-19 Кл (Кулон). Заряды остальных капель кратны этому наименьшему заряду. Милликен подтвердил делимость (дискретность) электрического заряда и рассчитал элементарный заряд.
Первая модель атома
Уже было известно, что атом содержит отрицательные электроны, но сам атом не имеет заряда. Объяснить это противоречие можно было тем, что сумма отрицательных зарядов уравновешивается положительным зарядом.
На основании этого предположения Джозеф Джон Томсон в 1904 г. предложил первую модель атома "Булка с изюмом".
Согласно этой модели, атом – положительно заряженная часть пространства с включенными в нее отрицательно заряженными электронами. Эта модель внешне напоминает булку с изюмом поэтому и получила соответствующее название.

