
Полная версия
От водорода до мейтнерия: неорганика на ладони. Книга первая: металлы и неметаллы главных подгрупп таблицы Менделеева
Фтор очень токсичный газ. В малых концентрациях его запах напоминает запах хлора, иногда озона. На предприятиях обязательно контролируют предельно допустимую концентрацию фтора в воздухе.
Глава 6
Плавиковая кислота. «Стекло, берегись!»
Каким образом мастера на производстве делают надписи на стекле или наносят на него рисунки? В этом им помогает плавиковая кислота – «гроза» всех стекол. Как у нее это получается?
Плавиковая, или, химически говоря, фтористоводородная кислота с формулой HF, – одноосновная кислота, состоит из одного атома водорода и одного атома фтора. Водород и фтор соединены между собой ковалентной полярной связью, общая электронная пара смещена к атому фтора (мы помним, что фтор – «чемпион» по электроотрицательности среди всех элементов). При этом молекулы HF объединяются в димеры, образуя молекулярную кристаллическую решетку, каркас из молекул.
Название «плавиковая» появилось от плавикового шпата, фторида кальция – минерала, из которого получают фтороводород. При растворении фтороводорода в воде выделяется тепло. Плавиковая кислота – бесцветная жидкость с резким запахом, тяжелее воды, затвердевает при температуре ниже минус 75 градусов. Не горюча. Если в воду добавить небольшое количество плавиковой кислоты, то такая «вода» замерзнет при более низких температурах.
По степени диссоциации плавиковую кислоту можно отнести к слабым кислотам. Она реагирует с большинством металлов, кроме платины, палладия и золота. Свинец также не растворяется в плавиковой кислоте благодаря образующейся защитной пленке фторида свинца. Фториды щелочных металлов растворимы в воде, щелочно-земельных – малорастворимы.
Плавиковая кислота разъедает стекло и другие силикатные материалы (кварц, фарфор).
Мастера предварительно покрывают стекло парафином, а потом прорезают на парафине отверстия (контур) будущего рисунка. Эти отверстия обрабатывают плавиковой кислотой, остальное стекло под слоем парафина в безопасности (парафин устойчив к плавиковой кислоте). Логично, что хранят плавиковую кислоту в полиэтиленовой таре.
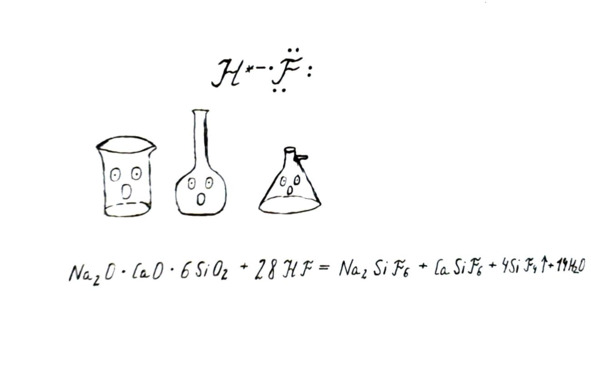
Стеклянная химическая посуда «боится» присутствия поблизости плавиковой кислоты
Плавиковая кислота в промышленности:
– катализатор в органическом синтезе;
– реактив для растворения силикатов;
– реактив для получения фторидов и фторорганических соединений.
Плавиковая кислота очень ядовита, обладает раздражающим действием, вызывает ожоги. Кроме того, фториды способны связывать кальций в крови, это ведет к нарушению сердечной деятельности, серьезным сбоям в организме человека. Опасность состоит еще и в том, что пагубное действие плавиковой кислоты имеет отложенный эффект, человек поздно обращается за помощью, когда патологический процесс уже запустился. Поэтому так важно работать с кислотой в защитной одежде, респираторе, очках, перчатках и в помещении с хорошей вытяжкой. В случае внештатных ситуаций плавиковую кислоту осторожно дезактивируют, основываясь на свойствах кислот нейтрализовываться щелочами (гашеной известью или содой).
Глава 7
Хлор. «Кто тут главный? Я тут главный!»
Наш следующий герой – любимец учебников по химии и заданий ЕГЭ, «звезда» группы галогенов – хлор.
Элемент хлор располагается в 3 периоде VIIA группе периодической системы Д. И. Менделеева. Атом хлора имеет в своем составе 17 протонов и, соответственно, 17 электронов, а вот число нейтронов варьируется. В природе наиболее широко распространены изотопы с массовыми числами 35 и 37 (массовое число = количество протонов + количество нейтронов). Исходя из процентного соотношения изотопов, относительную атомную массу хлора высчитали как равную 35,5. Этот момент необходимо помнить при решении задач.
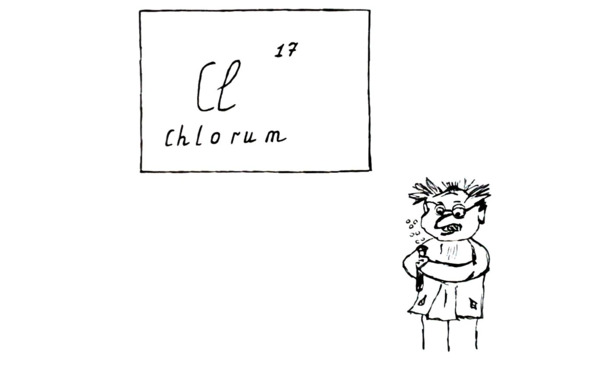
На внешнем энергетическом уровне у атома хлора – 7 электронов. Принимая еще один электрон, атом приобретает степень окисления -1. Но у атома хлора, в отличие от «соседа сверху» – фтора, есть дополнительные орбитали, а именно – пять d-орбиталей. Хлор ведь в третьем периоде находится. Поэтому при определенных условиях электроны с р- и даже s-подуровней способны «перебегать» на d-орбитали и занимать там единолично «вакантные» места. Электроны – они ведь, как люди, в душе немного эгоисты. Каждому хочется иметь свою комнату, свое жизненное пространство. Одиночные электроны – возможность разнообразить степени окисления и образовать различные соединения с другими атомами.
Хлору проще принять один электрон, довести свой энергетический уровень до завершенности и получить степень окисления, равную -1 (самая распространенная в соединениях). Хлор – сильный окислитель.

Возможные степени окисления для хлора: -1 (принимает электрон), +1, +3, +5 и +7 (отдает свои электроны)
Молекулярный хлор состоит из двух атомов и представляет собой ядовитый газ желто-зеленого цвета с резким запахом, растворимый в воде. Значительно тяжелее воздуха. Легко сжижается, ведь его температура кипения всего -34 градуса. Кстати слово «хлор» с греческого языка переводится как «зеленый».
Получение хлора
По традиции рассмотрим отдельно лабораторные и промышленные способы получения.
Впервые хлор удалось получить немецкому химику Карлу Шееле в 1774 году путем воздействия соляной кислоты на минерал пиролюзит (оксид марганца (IV)). Шееле заметил, что образовавшееся вещество обладает отбеливающими свойствами и имеет запах царской водки. Помимо способа Шееле в лаборатории хлор получают по реакции соляной кислоты с каким-нибудь сильным окислителем, например, с перманганатом или дихроматом калия. Соляная кислота выступает в роли восстановителя.
В заводских условиях хлор получают электролизом раствора поваренной соли. Хлор собирается на аноде, на катоде восстанавливается водород, а в растворе остается гидроксид натрия.
Полученный хлор хранят в стальных баллонах.

Применение хлора
Для чего же мы его получали? А вот для чего:
– синтез хлорорганических соединений;
– отбеливание тканей, бумаги, картона. Правда, здесь есть один нюанс: отбеливает не сам хлор, а хлорноватистая кислота, которая образуется после растворения хлора в воде. Об этом мы еще поговорим;
– обеззараживание воды;
– производство неорганических соединений (соляная кислота, хлориды металлов, удобрения).
Хлор сам по себе очень токсичен, да еще и тяжелее воздуха, первым делом поражает дыхательную систему человека, вызывая ожоги и удушье. Поэтому спецодежда, противогаз и перчатки – неотъемлемый атрибут для сотрудников на производстве. При внештатной ситуации на короткое время защититься от воздействия хлора поможет ткань, смоченная раствором сульфита или тиосульфата натрия.
Химические свойства хлора
1. Реакции с неметаллами
Хлор активно вступает в реакции с неметаллами, с водородом и вовсе – вплоть до взрыва. Но с углеродом, азотом, кислородом и благородными газами хлор непосредственно не реагирует!
2. Реакции с металлами
Хлор реагирует почти со всеми металлами и выступает в роли сильного окислителя, приобретая отрицательную степень окисления. При этом продуктом взаимодействия являются различные соли. Такой порядок характерен не только для хлора, а для группы галогенов вообще. Недаром «галоген» означает «рождающий соль».
3. Реакции со сложными веществами
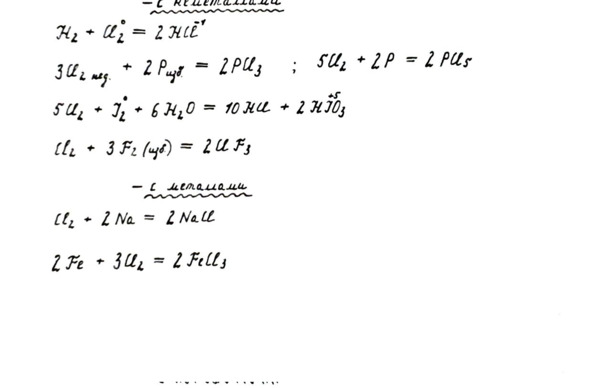
В реакции с более электроотрицательным фтором хлор выступает как восстановитель (не окисляет, а окисляется сам)
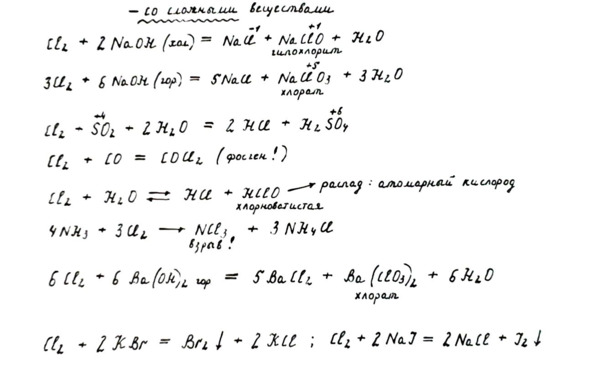
Взаимодействие хлора со щелочью – классический пример реакций самовосстановления-самоокисления (диспропорционирования). Ух, неужели напечатала без ошибок, от букв аж в глазах рябит! Иначе говоря, хлор свою степень окисления одновременно и понижает, и повышает. Вид продукта реакции зависит от температуры раствора щелочи.
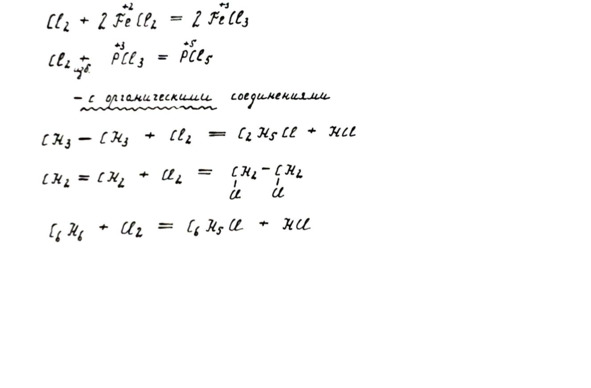
Раствор хлора в воде дает начало двум кислотам: соляной и хлорноватистой. Хлорноватистая кислота распадается, выделяя атомарный кислород – сильный окислитель, который и «отвечает» за отбеливающий эффект. Подобный механизм с выделением атомарного кислорода мы упоминали в главе про газ озон.
Каждый «выше стоящий» в группе галоген способен замещать собой в соединениях «ниже стоящий». Так на примерах реакций видно, что хлор вытесняет бром и йод из солей и становится на их место.
Отдельную группу составляют реакции хлора с органическими веществами. Здесь возможны вариации в зависимости от строения органической молекулы. Один из атомов хлора способен замещать атом водорода в насыщенных соединениях (где все связи одинарные). Молекула хлора может присоединяться целиком по кратным (двойным) связям. Хлор реагирует и с ароматическими соединениями.
Конец ознакомительного фрагмента.
Текст предоставлен ООО «ЛитРес».
Прочитайте эту книгу целиком, купив полную легальную версию на ЛитРес.
Безопасно оплатить книгу можно банковской картой Visa, MasterCard, Maestro, со счета мобильного телефона, с платежного терминала, в салоне МТС или Связной, через PayPal, WebMoney, Яндекс.Деньги, QIWI Кошелек, бонусными картами или другим удобным Вам способом.


