Полная версия
Механизмы неорганических реакций выплавки чугуна и стали

Константин Ефанов
Механизмы неорганических реакций выплавки чугуна и стали
Введение
В монографии по-видимому впервые затронута тема описания механизмов неорганических реакций железа, происходящих в процессах выплавки чугуна и стали.
В существующей литературе по физике металлов приводятся только структурные формулы железоуглеродистых сплавов и оксидов железа, а также подробно описаны физические взаимодействия перегруппировки атомов железа при перестройке кристаллической решетки.
В литературе по выплавке чугуна и стали реакции железа описаны химическими брутто-формулами, не показывающими механизм химического взаимодействия.
В неорганической химии существует описание механизмов реакций для координационных соединений железа – для отдельных молекул, окруженных жидким растворителем. А химические реакции оксидов железа железа при выплавке чугуна описываются как в литературе по металлургии только брутто-формулами.
__
В монографии выполнено обоснование механизмов химических реакций выплавки чугуна и стали на основании междисциплинарного анализа данных литературного обзора разделов металлургии, физики металлов, квантовой химии, теоретической неорганической химии,
Работа является первой попыткой рассмотреть с химической точки зрения указанную тематику и выполнить общее теоретическое основание. Работа не является классической публикацией с квантово-механическими расчетами и обсуждением экспериментальных данных.
Цель работы достигнута, результаты изложены в разделе заключения.
__
Работа посвящается БОГУ ТВОРЦУ ТРОИЦЕ,
выражаю благодарность моей маме, работавшей инженером нефтяного машиностроения.
Конфигурация атома железа
Электронная оболочка атома железа в основном состоянии [1]:

Энергетический уровень элемента (значение энергии квантовой системы) – N, терм – 5D4 (обозначение символами спектров).
Как видно их схемы, энергия 3d-орбиталей ниже, чем 4p-орбиталей. В соответствии с правилом Хунда суммарное спиновое число должно быть максимальным, то есть при заполнении одним электроном одной орбитали, а затем заполнение вторым электроном орбиталей, имеющий один электрон. На основании этого правила в атоме железа 3d-орбитали имеют по 1 электрону.
Конфигурация орбиталей атома железа:

К Eg конфигурациям относятся
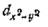

Наложением d-орбиталей получается без s- и p-получается следующая графика:

Орбиталью является решение квантово-механического уравнения. Орбиталь является областью пространства с наиболее вероятным расположением электрона. Электрон является одновременно частицей и волной, что присутствует в квантово-механических расчетах.
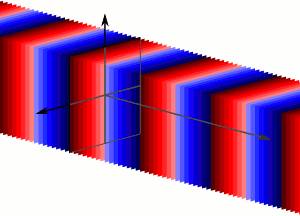
Квантово-механический расчет металлической связи для модели свободных электронов приведен в работе А. Зоммельфельда [2]. Орбиталь металлической связи получена в виде плоской волны, как показано на рисунке ниже:
Кристаллическая решетка железа [7]:

Схема перестройки решеток подробно рассмотрена в монографии Уманского [3]. Так, например, показана схема изменения конфигурации гранецентрированной решетки на объёмно-центрированную решетку то есть при γ→α превращении [3,с.244]:
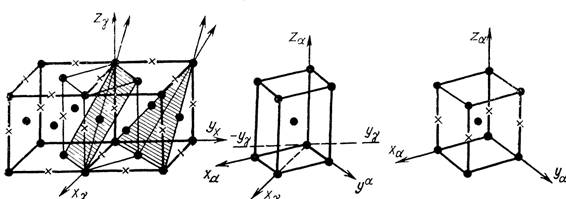
На рисунке слева приведена сдвоенная ячейка γ-фазы (аустенита). Такая схема показывает, что выделенные узлы перейдут в конфигурацию решетки α-фазы (мартенсита). Для превращения решеток требуется выполнения условия одинакового количества атомов железа и минимальные суммы квадратов деформаций по главным осям.
Уманский в работе [24,с.71] приводит данные об отклонении d-орбиталей от симметрии в поле вокруг атома железа в кристаллической решетке. Так заряд d-орбиталей распределяется по Уманскому в виде конфигурации Eg с концентрацией вдоль ребер куба и в виде конфигурации Т2g с концентрацией вдоль диагоналей куба. Плотности магнитных электронов не обладают сферической симметрией по отношению к ядру железе [24,с.72].
Уманский приводит диаграммы распределения плотности магнитных спинов вдоль граней куба и вдоль диагонали [24,с.77]:

Как видно из рисунка, контурные линии одинаковой спиновой плотности вокруг ядра не являются окружностями. Малая плотность посередине показывает о наличии сжатия плотности в направлении пространственной диагонали в куба.
Уманский приводит диаграммы разности магнитной плотности между теоретической сферической конфигурацией и измеренной экспериментально [24,с.78]:
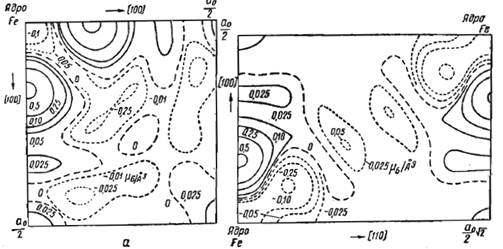
На диаграммах видна малая плотность посередине между атомами железа. На грани куба плотность избыточная, в диагональном направлении плотность недостаточная.
Уманский отмечает [24,с.14], что представление о расщеплении d-орбитали под действием кристаллической решетки на Eg и T2g уровни является ошибочным. Так как экспериментальная полоса для 3d-уровня получается существенно шире, чем расщепление от одного кристаллического поля. Экранирование свободными электронами полосы проводимости ионных полей уменьшаем симметричную часть локального потенциала решетки.
Распределение электронной плотности и заряда d-электронов в металле почти такое же как в изолированном атоме железа [24,с.15]. В т.ч. по причине электростатического равновесия. Волновые функции у нижнего края d-полосы сильно гибридизированы волновыми функциями полосы проводимости. За счет этого объясняется уменьшение числа электронов с семи в изолированном атоме до шести в металле. Истинная полоса проводимости содержит один электрон на один атом.
__
Механизмы реакций в неорганической химии описываются наглядно только для структуры веществ, описываемой орбиталями гантелевидной формы. Под механизмом реакции понимается последовательность промежуточных частиц от сырья до продукта реакции.
Можно увидеть два непротиворечащих друг другу подхода – физический, описывающий свойства металла (проводимость и др.) и химический. Объяснение механизмов реакций возможно только при использовании химического подхода с описанием структур молекул и химической связи с использованием гантелевидных орбиталей. Такой подход применен Полингом [1].
Отметим, что при описании процессов органических реакций на металлическом катализаторе в нефтепереработке, используют описание структур гантелеобразными орбитами. То есть для атомов металла, на которые адсорбируется органическая молекула, применяется орбиталь как в координационном соединении. За счет связи с орбитой металла, связи в органической молекуле ослабляются и становится возможной протекание химической реакции.
По первой модели металлической связи Друда можно сделать резюме, что валентные электроны атомов железа становятся общими для всей решетки. То есть атом теряет индивидуальные свойства. Для химических реакций необходим обратный процесс восстановления индивидуальных свойств, то есть валентных электронов и гантелевидных орбиталей.
Полинг отмечает [1,с.395], что металлические связи являются резонирующими ковалентными связями на основании сравнения длин октаэдрических гибридизованных связей и атомных радиусов в решетке металла. Таким образом, можно сделать вывод о возможности выхода из резонансной структуры орбиты в ковалентную связь с органическими или неорганическими молекулами.
__
Химические реакции при выплавки стали происходят в жидкой фазе после нагрева. Механизмы реакций должны описываться как механизмы реакций в растворе.
Механизмы реакций соединений железа в растворе относятся к химии координационных соединений.
Для описания структуры координационных соединений в неорганической химии используют четыре подхода [4]:
– теория кристаллического поля,
– теория валентных связей (теория Полинга [1]),
– теория молекулярных орбиталей,
– теория поля лигандов.
В настоящей монографии для описания химии координационных соединений железа используем теорию валентных связей как теорию с наиболее наглядными результатами для понимания химизма процесса.
В теории валентных связей обитали комплекса железа рассматриваются в виде гибридизованных орбиталей центрального атома железа.
Рассмотрим проблему гибридизации атомных орбиталей.
Полинг отмечает, что для атомов железа [1,с.100] разница в энергии 3d-, 4s-, 4p-орбиталей небольшая и поэтому эти орбитали могут комбинироваться для образования прочных связывающих орбит. По Полингу прочность d-орибитали равна 2,236, гибридизованной орбитали d-s-p равна 3, что выше максимальной прочности гибридизованной s- и p- орбит, равной 2.
Пример октаэдрической гибридизованной орбитали, образованной s- и p- орбитами и двумя d-орибиталями [1,с.101]:
Пример гибридизованной тетраэдрической орбитали углерода [1,с.88]:

В работе [10,с.138] указывается о описания пространственной структуры металлической решетки с помощью направленных гибридных связей, аналогично описанию связей в алмазе. Авторы считают, что объёмно-центрированная ячейка металла получается за счет гибридных sd3-орбиталей, в гранецентрированной упаковке (кубической плотноупакованной в терминах авторов) за счет гибридных p3d3-орбиталями, гексагональные плотноупакованные структуры за счет гибридных sd2-, pd5- и spd4-орбиталей. Перечисленные гибридные орбитали определяются различным участием в гибридизации d-орбиталей, имеющихся у атома железа, которые железо предоставляет для выполнения гибридизации.
Такой подход соответствует подходу описания структур в неорганической и органической химии и по-видимому является справедливым для образования геометрии в ячейке металла. Однако, после этого, валентные электроны делокализуются по всей решетке металла, при этом за счет близкого расстояния между атомами, электронные орбитали существенно перекрываются. В методе молекулярных орбиталей, применяемом для отдельных молекул, считается, что атомы теорияют индивидуальность и электроны образуют общую для молекул орбиталь. В металле электроны образуют общий для всей решетки металла электронный газ.
В случае перекрывания орбиталей N атомов в твердом теле, образуются N новых орбиталей, относящихся к твердому телу. Уровни энергий орбиталей в металле расположены близко и образуют энергетические полосы [10,с.138]:

На этой схеме на каждом уровне находятся 2 электрона и при общем количестве N электронов, нижние уровни N/2 будут дважды занятыми.
Электрический ток является упорядоченным движением электронов. Приведем описание на основании метода молекулярных орбиталей [10,с.138]. Движение электронов может происходить, если электроны получают энергию и переходят на высокие незанятые уровни. То есть структуры металлов содержат незанятые верхние энергетические уровниъ. Для полупроводников незанятая зона близко расположена с занятой и переход возможет только при повышении энергии с повышением температуры.
Взаимодействующие в решетке атомы железа являются квантовой системой, для которой выполняется запрет Паули, т.е. на каждом энергетическом уровне в кристалле не может быть более двух электронов на одном энергетическом уровне. При одинаковой энергии нескольких g энергетических уровней (квантовых состояний), т.е. при вырождении, на каждом уровне может находится только 2g электронов (g – степень вырождения). 2N электронов индивидуальных атомов железа с высшего уровня разместятся попарно на N уровне полосы в криталлической решетке.
Энергия электронов в металле квантуется, т.е. занимает определенные уровни энергии (или дискретные значения). Каждый уровень индивидуального атома железа расщепляется в кристаллической решетке из N атомов – на N близкорасположенных уровней, составляющих или зону [11,с.247]. Валентные электроны на внешних электронов больше возмущаются, чем электроны на внутренних орбиталях атома. Схема расщепления уровней для внешних валентных электронов и внутренних в зависимости от расстояния между атомами железа показана на рисунке:

Как видно из рисунка перекрывание внутренних орбиталей практически отсутствует. Расщеплению подвергаются орбитали, занятые валентными электронами и свободные орбитали высшего уровня.
Величины энергетических уровней валентных электронов в кристаллической решетке металла объединяются в зоны, которые разделяются запрещенными зонами (промежутками) без разрешенных значений энергии, т.е. в которых электроны находиться не могут [11,с.248]. Ширина разрешенной зоны составляет несколько электронвольт [11,с.249]. Уровни в зоне располагаются максимально близко с ростом числа атомов железа в решетке.
Конец ознакомительного фрагмента.
Текст предоставлен ООО «ЛитРес».
Прочитайте эту книгу целиком, купив полную легальную версию на ЛитРес.
Безопасно оплатить книгу можно банковской картой Visa, MasterCard, Maestro, со счета мобильного телефона, с платежного терминала, в салоне МТС или Связной, через PayPal, WebMoney, Яндекс.Деньги, QIWI Кошелек, бонусными картами или другим удобным Вам способом.









