
Полная версия
Химические элементы

Александр Иванов, Игорь Гордий
Химические элементы
© Иванов А.Б., Гордий И.В., текст, 2018
© Чукавин А.А., ил., 2018
© ООО «Издательство АСТ», 2018
* * *От авторов

Приветствуем тебя, дорогой читатель! В руках ты держишь книгу, в которой рассказывается о том, из каких химических элементов состоит окружающий нас мир, об их свойствах, о том, по какому принципу они расположены в таблице Менделеева, удивительные истории их открытия и многое другое. Вместе мы погрузимся в прекрасный мир химии и сделаем акценты на самых интересных, самых важных и самых необычных явлениях, с которыми мы можем встретиться при изучении химии.
Нет, это не занудный школьный учебник – гораздо лучше! Эта книга станет для тебя первым серьезным, но при этом легким шагом в мир самой удивительной и прекрасной науки – химии. Ведь она присутствует во всех сферах нашей жизни, а мы об этом даже не задумываемся.
Да, у многих возникают проблемы с химией, но мы постараемся сделать так, чтобы твое путешествие через эту книгу было максимально комфортным и полезным. Для этого мы объясним тебе все термины, с которыми ты можешь встретиться впервые.
Данная книга написанаАлександром Ивановым, создателем и автором проекта «Химия – просто» и Игорем Гордием – ответственным за научный контент в социальных сетях проекта «Химия – просто». Мы очень рады, что у нас есть возможность вместе с тобой окунуться в эту восхитительную науку. И не забудь подписаться на наш YouTube-канал, группу вконтакте, а также в других социальных сетях. В конце книги ты найдёшь QR-коды, с помощью которых ты легко найдешь наши аккаунты:

youtube.com/c/ChemistryEasy
vk.com/chemistryeasyru
Ну все, скорее перелистывай страницу и читай дальше! Книга сама себя не прочтет!
P.S.: а школьный учебник сдай в макулатуру. Береги природу!
Введение
«Вся гордость учителя в учениках, в росте посеянных им семян».
Д. И. МенделеевКогда мы говорим о химии, то в первую очередь на ум нам приходит таблица химических элементов Дмитрия Ивановича Менделеева. В 1869 году, в первом ее варианте, она отличалась от ныне существующей. В ней было меньше элементов, так как их было открыто всего 63, а сейчас в таблице содержится 118 элементов. Причем последний из них получил свое название совсем недавно в 2016 году в честь Юрия Цолаковича Оганесяна.
Постепенно наука развивалась, и сам Менделеев модернизировал свое творение. Были открыты инертные газы, и таблица пополнилась новыми элементами. Также Дмитрий Иванович поменял расположение элементов в таблице из столбцов в строчки. Да-да, в самом первом варианте химические элементы располагались по столбцам, а не по строчкам, как мы привыкли.
Элементы в таблице располагались в порядке увеличения их массы. Водород – самый легкий, значит, он стоит в начале, за ним идут все остальные более тяжелые элементы. Если взглянуть в старую таблицу и в новую, то можно заметить принципиальное отличие, которым пользуются современные лжеученые. В старой таблице инертные газы стоят в первой колонке (химики называют колонки – группами), а в новой – в последней. Логика была проста: это же газы, значит, они должны быть легче остальных. Вроде бы логично, но нет. По этой логике все элементы в самом начале таблицы должны быть газами, так как они самые легкие. Например, газообразными должны быть как минимум литий, бериллий, бор, углерод. Но это неверно: они твердые при обычных условиях, а вот следующие за ними азот, кислород, фтор и неон – газообразные. Чувствуете, что что-то здесь не так?!
На самом деле, логика расположения элементов в таблице была не совсем правильной. Но при этом, волею случая, она совпала с современным принципом расположения элементов в таблице. Тем, кто хочет подробно разобраться в данном вопросе, советую открыть YouTube-канал «Химия – Просто» и посмотреть видео «Урок 1» и «Как пользоваться таблицей Менделеева». В них мы досконально разобрали принцип построения таблицы.
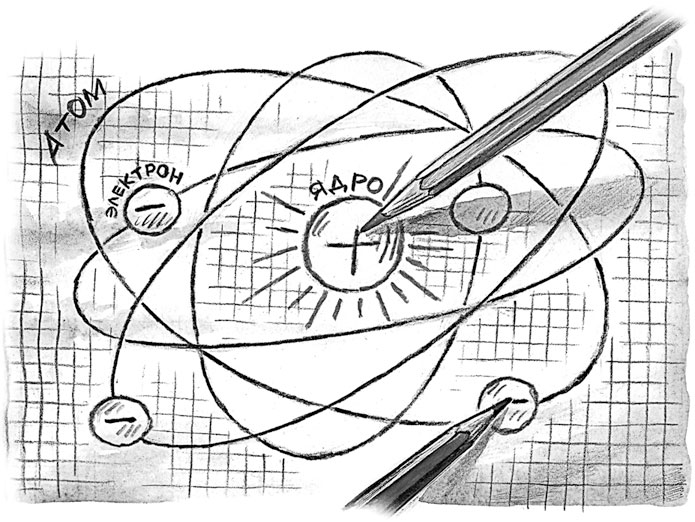
Однако вкратце все равно ответим на возникшие вопросы. Раньше элементы в таблице располагались в порядке увеличения их массы. Но тогда не знали, как устроен атом. Обратите внимание, что он состоит из ядра и электронов. Ядро в свою очередь состоит из протонов и нейтронов.
В современной таблице элементы расположены в порядке увеличения количества протонов в ядре атома. Поясним: в ядре любого атома водорода всегда один протон. В ядре атома гелия всегда два протона. Возьмем любой другой элемент, например полоний, в его ядре 84 протона. Порядковый номер элемента равен количеству протонов в ядре этого элемента. Все просто! Поэтому все инертные газы отправились в последнюю колонку, то есть группу. Так как оказалось, что, например, у аргона в ядре восемнадцать протонов, а у хлора семнадцать протонов, значит, аргон должен находиться в таблице после хлора.
Поздравляю, вы только что прошли полгода школьного курса за 8 класс. Можете собой гордиться!
В следующие полгода школьной химии нам обычно рассказывают, что какие-то там элементы имеют похожие свойства, что еще сам Дмитрий Иванович, зная свойства одних элементов, предсказывал свойства других. Обычно в такие моменты у всех возникает вопрос: «Как он это делал? Он что, экстрасенс?»
На самом деле все просто! Иначе бы не было такого проекта, как «Химия – Просто». Как мы уже сказали выше, в атоме, кроме ядра, еще есть электроны. Их количество равно количеству протонов в ядре и порядковому номеру элемента в таблице. Где же они находятся? На самом деле эти самые электроны до сих пор никто не видел и это плод буйной фантазии ученых. Так существуют ли они на самом деле?! Давайте посмотрим вокруг себя. У нас есть мобильные телефоны, компьютеры, мы ездим на машинах, чистим воду фильтрами, летаем на самолетах, а особо удачливые вообще в космос летают. Для всего это необходимы различные материалы, которые создали химики. Не могли же они так ошибаться и создать столько всего, чем мы каждый день пользуемся и все это работает?! Конечно не могли. Поэтому считается, что электроны вращаются где-то вокруг ядра атома. Конечно, ты сам можешь стать ученым и все перепроверить или посвятить свою жизнь тому, чтобы сделать фотографию электрона. Или наоборот доказать, что все ошибались. Это точно будет величайшим достижением человечества, а ты будешь его автором.
Конец ознакомительного фрагмента.
Текст предоставлен ООО «Литрес».
Прочитайте эту книгу целиком, купив полную легальную версию на Литрес.
Безопасно оплатить книгу можно банковской картой Visa, MasterCard, Maestro, со счета мобильного телефона, с платежного терминала, в салоне МТС или Связной, через PayPal, WebMoney, Яндекс.Деньги, QIWI Кошелек, бонусными картами или другим удобным Вам способом.





