
Полная версия
Сезонные заболевания. Зима
Суточная потребность в тиамине в зависимости от интенсивности труда и возраста и составляет для мужчин 1,5–2,6 мг, для женщин 1,3–1,9 мг; при беременности и кормлении грудью – 1,7–1,9 мг. Потребность повышается при высокоуглеводном питании. Значительно увеличивается потребность в тиамине при болезнях желудочно-кишечного тракта, острых и хронических инфекциях, хирургических операциях, ожоговой болезни, сахарном диабете, лечении некоторыми антибиотиками.
Витамин В2 (рибофлавин) входит в состав ферментов, регулирующих важнейшие этап обмена веществ. Он улучшает остроту зрения на свет и цвет, положительно влияет состояние нервной системы, кожи и слизистых оболочек, функцию печени, кроветворение.
При обычном питании до 60 % витамина В2 поступает с продуктами животного происхождения и около 40 % – с растительными. При кулинарной обработке содержание рибофлавина в пище снижается на 15–30 %. Недостаток в рационе белков ухудшает усвоение рибофлавина организмом.
Суточная потребность в рибофлавине в зависимости от интенсивности труда и возраста составляет для мужчин 1,8–3 мг, для женщин – 1,5–2,2 мг; при беременности и кормлении грудью – 2–2,2 мг. Потребность возрастает при анацидном (со сниженной кислотностью) гастрите и хроническом энтерите, гепатите и циррозах печени, некоторых болезнях глаз и кожи, анемиях.
Витамин В6 участвует в обмене белков, жиров, углеводов. Он необходим для усвоения организмом аминокислот, образования арахидоновой кислоты из линолевой и витамина РР из триптофана. Витамин В6 участвует в регуляции жирового обмена в печени, обмена холестерина, образовании гемоглобина.
Большое содержание витамина В6 (0,3–0,5 мг в 100 г съедобной части продукта) характерно для мяса животных и птиц, некоторых рыб (палтус, сельдь), икры, гречневой, перловой и ячневой крупы, пшена, хлеба из муки 2-го сорта, картофеля. Особенно богаты этим витамином (0,7–0,9 мг) печень, скумбрия, фасоль. Умеренное содержание витамина (0,15—0,29 мг) отмечается в большинстве рыб, яйцах, овсяной и манной крупе, рисе, хлебе из муки высшего сорта, макаронах, горохе.
Малое содержание витамина В6 (0,05—0,14 мг) характерно для молочных продуктов, овощей, фруктов, ягод. При кулинарной обработке теряется 20–30 % витамина В6. Потребность организма в витамине В6 удовлетворяется за счет е поступления с пищей и образования микрофлорой кишечника. Чем больше поступает с пищей белков, тем больше требуется витамина В6.
Суточная потребность в витамине В6 для мужчин составляет 1,8–3 мг, для женщин – 1,5–2,2 мг; при беременности и кормлении грудью – 2–2,2 мг. Потребность увеличивается при атеросклерозе, болезнях печени, токсикозах беременных, анацидных гастритах, энтеритах, анемиях, длительном приеме антибиотиков и противотуберкулезных препаратов.
Витамин В12 необходим для нормального кроветворения. Он играет важную роль в использовании организмом аминокислот и фолацина, образовании холина и нуклеиновых кислот, нормализации жирового обмена в печени.
Содержание витамина В12 в мкг на 100 г съедобной части продуктов: печень говяжья – 60, свиная – 30, язык говяжий – 4,7, мясо кролика – 4,1, говядина, баранина – 2,6–3, мясо кур – 0,5; яйца – 0,52 (белок – 0,08, желток – 2,0); рыба – 1,5–2,5 (сельдь, скумбрия, сардины – 10–12); молоко, кефир, сметана – 0,4, творог – 1,3, сыр – 1,5. Витамин В12 отсутствует в растительных продуктах и дрожжах.
Поступающий с пищей витамин В12 всасывается из кишечника после соединения в желудке с так называемым внутренним фактором и накапливается в печени. Суточная потребность его составляет 3 мкг; при беременности и кормлении грудью – 4 мкг. Дефицит витамина В12 в организме возможен при длительном строго вегетарианском (без молока, яиц, мяса, рыбы) питании и нарушении усвоения витамина при атрофическом гастрите, после резекции желудка или кишечника, при тяжелых энтероколитах, глистных инвазиях (широкий лентец и др.). При указанных заболеваниях потребность в витамине возрастает.
Витамин Е предохраняет от окисления ненасыщенные жирные кислоты мембран клеток, влияет на функцию половых и других эндокринных желез, стимулирует деятельность мышц, участвует в обмене белков и углеводов, способствует усвоению жиров, витаминов А и D. Потребность в нем – 12–15 мг в день. Она повышается при возможном нарушении усвоения витамина Е при заболеваниях печени (гепатиты, цирроз), поджелудочной железы, кишечника, а также при длительном приеме линетола (концентрат полиненасыщенных жирных кислот). Имеются данные о повышении потребности при заболеваниях половой и нервно-мышечной системы, кожи, атеросклерозе.
Витамина Е больше всего в растительных маслах. Он устойчив при кулинарной обработке, но разрушается при прогоркании жиров и под действием солнечных лучей, что следует учитывать при хранении растительных масел.
Содержание витамина Е в мг на 100 г съедобной части продуктов: масло хлопковое – 99, кукурузное – 93, подсолнечное – 67, сливочное – 2,2; мука, крупы, хлеб – 2–3,5 (гречневая крупа – 6,6); горох – 9,1, фасоль – 3,8; яйца – 2,0; молочные продукты – 0,1–0,5; мясо – 0,2–0,6 (печень – 1,3); рыба – 0,4–1,2; овощи, фрукты, ягоды – 0,1–0,7 (горошек зеленый и шпинат – 2,5; лук зеленый, абрикосы, персики – 1–1,5).
В настоящее время у нас в стране выпускают препараты «Гексавит», «Декамевит» и «Ундевит» и многие другие с оптимальным соотношением витаминов С, А и группы В. Их рекомендуется принимать в зависимости от возраста по 0,5–1 драже 2–3 раза в день после еды курсами продолжительностью 20–30 дней с повторением через 1–2 месяца.
Ультрафиолетовое облучение организмаВ комплексе профилактических мероприятий ультрафиолетовое облучение (УФО) является одним из доступных и эффективных методов, повышающих адаптационные и защитные функции организма. Облучение проводится с помощью длинноволновых ультрафиолетовых лучей в диапазоне 400–280 нм. Именно эта область УФ-спектра является биологически наиболее активной, близкой к естественному излучению солнца. Обычно в качестве источников такого излучения используются люминесцентные лампы типа ЛЭ-15, ЛЭ-30, ЛЭР-30, ЛЭР-40 либо ртутно-кварцевые лампы типа ДРТ-220, ДРТ-400, ДРТ-1000. Следует отметить, что УФ-лучи не только активно стимулируют иммунобиологическую реактивность, но и способствуют образованию витамина D, нормализуют фосфорно-кальциевый обмен, активизируют функции симпатико-адреналиновой системы, способствуют повышению обмена веществ в организме человека.
В организационно-тактическом плане метод УФО осуществляется в 2 вариантах:
1) кратковременное (несколько минут) ежедневное облучение нарастающими дозами (от 1/4 до 3 биодоз) – до 30 сеансов;
2) ежедневное длительное (4–8 ч) облучение несколько меньшими дозами в течение 5–6 месяцев – в этих условиях пациенты ежедневно получают от 1/8 до 3/4 биодозы. У каждого варианта есть свои положительные стороны. С помощью первого – строго дозированного и целенаправленного – чаще решаются медицинские задачи, в том числе и по профилактике ОРЗ; второй вариант более физиологичен и менее трудоемок (лампы обычно монтируются в осветительную сеть) – с его помощью легче проводить общегигиенические мероприятия по повышению адаптационных функций организма. Некоторое разделение методик обоих вариантов – здесь чисто условное понятие. При необходимости они с успехом используются для решения и той и другой задачи.
В практических условиях применение УФО по первому варианту осуществляется с помощью большого набора схем в зависимости от цели и задачи проводимого мероприятия, условий применения метода.
Для предупреждения заболевания верхних дыхательных путей, а также для профилактики их обострения в период ремиссии начинать облучение с 1/4 биодозы на переднюю и заднюю поверхности тела, увеличивая дозу каждой последующей процедуры (или через одно облучение) на 1/4 биодозы до 3–4 биодоз. Курс – 16 процедур. Оптимальный вариант применения такой схемы облучения – 2 раза в год.
При остром катаре верхних дыхательных путей – УФО области шеи, лица, груди (до уровня сосков), верхней трети спины до углов лопаток по 1–1,5 биодозы (3–4 процедуры); УФ-облучение слизистой оболочки носа через тубус, начиная с 0,5 биодозы, увеличивая дозу последующих облучений на 0,5 биодозы – до 2 биодоз (4–5 процедур).
При остром фарингите – УФО задней стенки глотки через тубус, от 0,5 до 2–3 биодоз (3–5 процедур).
При остром трахеобронхите – облучение передней и задней поверхности шеи 2–3 биодозами – курс 5–6 облучений. Облучение по такой схеме оказывает противовоспалительное, десенсибилизирующее действие, способствующее уменьшению отека слизистой оболочки бронхов.
Для групповых УФ-облучений после перенесенного ОРВИ в восстановительном периоде применяется методика, которая предусматривает облучение малыми, постепенно возрастающими дозами (от 1/8 до 1/2 биодозы) и предназначена исключительно для использования в восстановительном периоде после ОРЗ с целью повышения иммунобиологической реактивности организма. Облучение рекомендуется производить через день; обычный курс для часто болеющих – 20 сеансов, для редко болеющих – 12–15.
Таким образом, ультрафиолетовое облучение организма человека в настоящее время можно отнести к наиболее доступным и эффективным методам неспецифической профилактики острых респираторных инфекций.
РефлексопрофилактикаВ качестве средств неспецифической профилактики гриппа и ОРЗ все более широкое распространение получает направление рефлексопрофилактики (акупунктура, акупрессура, фармакопунктура). Одним из таких направлений является метод точечного пальцевого самомассажа биологически активных зон кожи. Преимущество этого метода перед всеми остальными заключается в том, что он основан исключительно на мобилизации собственных функциональных резервов организма и их адекватном использовании, имеет минимальное число противопоказаний и малую вероятность побочных эффектов, экономичен и технически прост в реализации.
Сущность метода состоит в том, что биологически активные зоны кожи, обладая множеством прямых и обратных связей между собой, с различными внутренними органами и их участками, обеспечивают связь биологически активной внутренней системы организма и ее подсистем с окружающей средой. Воздействие на эти зоны позволяет производить своего рода «настройку» внутренней среды организма, вышедшей по тем или иным причинам из своего физиологически оптимального уровня. В ответ на воздействие на биологически активные участки кожи увеличивается поступление в кровь биологически активных веществ типа интерферона, иммуноглобулинов и др.
Механическое раздражение зон кожи производится путем надавливания на нее пальцем или твердым телом, напоминающим форму пальца. Делается 9—10 вращательных движении по часовой стрелке и против нее – 3 вращения в 1 секунду (на счет «раз, два, три»).
Для массажа определены 9 основных зон кожи:
1 – в центре тела грудины, на уровне прикрепления IV ребра;
2 – в центре яремной вырезки;
3 – симметричная, на уровне верхнего края щитовидного хряща, у переднего края мышцы;
4 – симметричная, в углублении кзади от основания мочки уха;
5 – одиночная точка между VII шейным и I грудным позвонками;
6 – симметричная, между носогубной складкой и серединой крыла носа;
7 – в центре надпереносья, в углублении между надбровными дугами, симметричная, у внутреннего края надбровной дуги;
8 – симметричная, в углублении кпереди от козелка уха;
9 – между указательным и большим пальцами, ближе к запястью, на тыльной поверхности кисти.
Процедуру следует выполнять не реже 2–3 раз в день в течение 1–2 мин. Метод точечного массажа применим в любом возрасте, с первого дня жизни и на всем ее протяжении; очень важен для профилактики ОРЗ у беременных и лиц с аллергическими реакциями на введение лекарственных средств. Высокая эффективность указанного мероприятия достигается только при его регулярном и систематическом проведении. Первоначальное обучение технике самомассажа следует пройти у врача-специалиста. В настоящее время методы рефлексопрофилактики находят все более широкое применение для защиты от ОРВИ как взрослого, так и детского населения.
Закаливание организмаЗакаливание – система мероприятий, направленная на повышение устойчивости организма человека к действию разнообразных природно-климатических факторов – холода, тепла, атмосферного давления, солнечной радиации и других, которые в свою очередь влияют на его устойчивость к различным заболеваниям. В качестве основных средств закаливания используют: воздух, воду, солнце. Сущность закаливания состоит в тренировке терморегуляторного аппарата, выработке условных рефлексов.
Схематично механизм закаливания заключается в следующем: термическое воздействие воспринимается специальными холодовыми и тепловыми рецепторами, заложенными в коже, и трансформируется в центр терморегуляции в гипоталамусе, следствием чего является включение преимущественно физической или химической формы терморегуляции. В терморегуляторные реакции вовлекаются сердечно-сосудистая, дыхательная система, система кровообращения и др. При этом повышается обмен веществ (так, подъем температуры тела на 1 °C увеличивает интенсивность основного обмена на 7 %) и усиливается активность иммунной системы.
Эффективность закаливающих процедур зависит от соблюдения следующих основных правил:
1) постепенность увеличения дозы закаливающих воздействий;
2) регулярность повторения процедур на протяжении жизни;
3) использование комбинированных воздействий физических агентов (холод, тепло, солнечные лучи, вода);
4) проведение закаливания с учетом состояния здоровья, выносливости и других индивидуальных особенностей организма;
5) предварительная санация организма лиц, страдающих различными воспалительными процессами;
6) осуществление общих (когда закаливающий фактор воздействует на всю поверхность тела) и местных (только на ограниченную часть: лицо, шею, ноги) процедур;
7) применение полиградационного закаливания – назначение сильных, слабых, а также замедленных и быстрых закаливающих агентов в течение дня и на всем протяжении закаливания.
Его необходимо проводить во все сезоны года. Постоянных противопоказаний нет. Временными являются лихорадочные состояния, травмы, заболевания со значительным нарушением функций нервной, сердечно-сосудистой, дыхательной и других систем. После перенесенной болезни можно приступить к закаливанию в начальном режиме при использовании местных процедур.
Для определения режима закаливания необходимо провести пробы (их несколько) на устойчивость к холоду. Суть одной из них заключается в анализе изменений частоты сердечных сокращений (ЧСС) при охлаждении стоп водой (обычная водопроводная вода) 14–17 °C в течение 3 мин.
Для оценки результатов имеется специальная таблица.
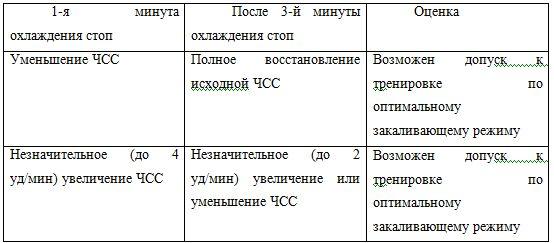
Если же восстановления ЧСС на 3-й минуте холодовой пробы не наступает и субъективно неприятные ощущения, то таким лицам следует рекомендовать закаливание по начальному режиму.
Исследования специалистов и многочисленные публикации по закаливанию и комплексам физических упражнений свидетельствуют о том, что арсенал этих процедур обширен и настоятельно рекомендуется для применения в организованных коллективах детей и подростков. Существует дифференцировка закаливающих процедур, используемых для профилактики ОРЗ, на 3 группы.
1. Закаливание воздухом:
1) прогулки на открытом воздухе 2 раза в день 2 ч или не менее 4 ч в день;
2) воздушные ванны с утренней гимнастикой (10–15 мин);
3) дневной сон на свежем воздухе или в постоянно проветриваемом помещении;
4) хождение босиком в помещении или на открытом воздухе (сочетание процедур).
2. Закаливание водой:
1) ежедневные влажные обтирания тела по 2–4 мин с помощью влажных полотенца, рукавички или губки;
2) умывание водой (14–16 °C) шеи, верхней части груди, рук до плеч;
3) полоскание горла холодной водой;
4) обливание – начинать лучше летом водой 34–36 °C;
5) душ, контрастный душ – действуют не только температурные факторы, но и механические; начинать следует со слабо контрастного душа (разность температур менее 10 °C);
6) водные ванны;
7) обливание стоп;
8) контрастные ножные ванны или обливание стоп;
9) сауна или русская баня;
10) купание в бассейне;
11) купание в открытых водоемах.
3. Закаливание солнечными лучами.
Опыт исследований в области закаливающих процедур с целью снижения заболеваемости ОРВИ свидетельствует о том, что при методически правильном, регулярном их применении достигается высокая эффективность мероприятий.
Ценность всех рассматриваемых процедур – в неспецифическом характере воздействия на организм человека, поэтому они должны занять свое важное место в системе защиты от ОРЗ населения и особенно детей.
ИНФЕКЦИИ ДЫХАТЕЛЬНОЙ СИСТЕМЫ
Ангина
Ангина – острое инфекционное заболевание, относящееся к группе аэрозольных инфекций, имеющее преимущественно стрептококковую этиологию, характеризующееся относительно кратковременной лихорадкой, явлениями общей интоксикации, воспалительными изменениями в лимфоидных образованиях глотки (чаще всего – в небных миндалинах) и регионарных к ним лимфатических узлах. Ангина сопровождается развитием аутоиммунных процессов, приводящих при отсутствии адекватного лечения к ревматизму, острому гломерулонефриту и некоторым другим иммунопатологическим заболеваниям.
До 90 % заболеваний ангиной вызываются бета-гемолитическими стрептококками группы А. Стрептококки попадают в воздух с мелкими каплями слюны и слизи, образующимися при различных экспираторных актах (кашель, чихание, громкий разговор). После их высыхания (в течение нескольких секунд или минут) возбудитель теряет патогенность и способность вызывать острый инфекционный процесс. Однако их жизнеспособность сохраняется во внешней среде длительное время, и стрептококки могут высеиваться из пыли через несколько недель и месяцев после удаления источника инфекции. Возможно, что такие варианты возбудителя способны формировать носительство стрептококка в зеве, а также вызывать болезни кожи.
Стрептококки группы А могут размножаться в некоторых продуктах питания (молоко, салаты, компот, мясной фарш), что имеет существенное эпидемиологическое значение. Оптимальная температура роста составляет 37 °C. При температуре ниже 20 °C и выше 42 °C размножение возбудителя прекращается. При нагревании до 56 °C стрептококки погибают в течение 30 мин.
Чувствительность стрептококков группы А к дезинфектантам не отличается от чувствительности к ним возбудителей других бактериальных аэрозольных инфекций с основной локализацией воспалительного процесса в верхних дыхательных путях (менингококковая инфекция, дифтерия и др.). Стрептококки группы А высокочувствительны к антибиотикам пенициллинового ряда и не способны вырабатывать к ним устойчивость, что определяет особую роль этих препаратов в лечении и профилактике стрептококковых инфекций у людей.
Источниками инфекции при ангине являются больные различными клиническими формами острых стрептококковых заболеваний и носители патогенных стрептококков. Наибольшее эпидемиологическое значение имеют больные с локализацией микробного очага в области верхних дыхательных путей (ангина, скарлатина, ОРЗ стрептококковой этиологии, гингивиты, кариес и др.). Такие больные обладают высокой степенью заразности, поэтому заражение восприимчивых лиц от указанных больных наиболее часто заканчивается развитием у них ангины. Лица, у которых очаги колонизации и размножения стрептококка располагаются вне дыхательных путей (стрептококковые пиодермиты, отиты, мастоидиты, остеомиелиты и т. д.), имеют меньшее эпидемиологическое значение в связи с менее активным выведением возбудителя из организма больного.
Продолжительность заразного периода у больных острой стрептококковой инфекцией зависит в основном от способа их лечения. Рациональная терапия больных скарлатиной и ангиной с использованием антибиотиков пенициллинового ряда, к которым стрептококки высокочувствительны, приводит к быстрому освобождению организма от возбудителя (в течение 1,5–2 суток). Наоборот, применение для этой цели препаратов, к которым стрептококки группы А полностью или частично потеряли чувствительность (сульфаниламиды, тетрациклины) обусловливает формирование носительства у 40–60 % переболевших.
Механизм передачи возбудителя.
Распространение патогенных стрептококков осуществляется в основном с помощью аэрозольного механизма передачи. Выведение возбудителя, локализованного в дыхательных путях, из организма источника инфекции обеспечивается экспираторными актами (разговор, кашель, чихание); заражение происходит при вдохе. Передача стрептококков осуществляется преимущественно воздушно-капельным путем. Этот путь передачи возбудителя обусловливает заражение восприимчивых лиц, находящихся главным образом в условиях тесного и достаточно продолжительного общения с источником инфекции (детские сады, детские дома, школы-интернаты, воинские коллективы).
Воздушно-капельный путь передачи патогенных стрептококков наиболее эффективно осуществляется в ночное время в спальных помещениях, особенно при скученном размещении в них. При этом в первую очередь заражаются лица, кровати которых расположены в непосредственной близости от кроватей источников стрептококковой инфекции. На расстоянии более 2 м этот путь передачи практически не реализуется. Дополнительными факторами, способствующими передаче патогенных стрептококков, являются низкая температура и высокая влажность воздуха в помещениях, так как при этих условиях дольше сохраняется капельная фаза, в которой возбудитель содержится в патогенном состоянии, а также запыленность помещений. Стрептококки группы А, попадая в пищевые продукты (молоко, молочные продукты, мясной фарш, вареные овощи, компоты, кисели, картофельное пюре), способны размножаться и длительно находиться в них.
Поэтому при определенных условиях может наблюдаться и алиментарный (пищевой) путь передачи возбудителя. Алиментарные вспышки ангины возникают при недостаточном медицинском контроле за работниками питания и связаны с заражением пищи больными острыми стрептококковыми заболеваниями, и прежде всего ангиной или носителями вирулентных стрептококков. В отдельных случаях возможно заражение продуктов при попадании возбудителя с кожных покровов из гнойно-воспалительных очагов стрептококковой инфекции. Большую роль в эпидемиологии алиментарных заражений возбудителями ангины играют нарушения технологии приготовления и хранения готовой пищи (недостаточная термическая обработка, хранение при температурах, способствующих размножению стрептококков).
ЭпидемиологияВ годовой динамике заболеваемости ангиной можно выделить 2 уровня: круглогодичную (спорадическую) и эпидемическую заболеваемость. Эпидемическая заболеваемость проявляется в виде сезонного повышения или отдельных эпидемических вспышек.
Наибольшую значимость в практическом отношении представляет сезонная заболеваемость, так как в коллективах, особенно учебных, на нее приходится 50–80 % заболеваний, зарегистрированных на протяжении года. Сезонный подъем заболеваемости ангиной достигает максимальной выраженности, как правило, в зимние месяцы.
Интенсификации сезонных подъемов заболеваемости ангиной способствуют скученность в помещениях, недостаточная вентиляция, некачественная уборка помещений, длительное пребывание людей в закрытых помещениях, поздняя изоляция и нерациональное лечение больных. Основными параметрами, влияющими при прочих равных условиях на заболеваемость, являются объем воздуха, приходящегося на 1 человека, количество людей в помещениях, рациональность использования всей площади спальных помещений и расстановки коек.
Входными воротами стрептококковой инфекции являются верхние дыхательные пути. Основным местом размножения служат небные миндалины и реже – другие лимфоидные образования ротоглотки (язычные миндалины, боковые валики задней стенки глотки и т. д.). Преодолев местные защитные барьеры миндалин, стрептококки начинают размножаться и продуцировать различные вещества, вызывающие воспалительный процесс. Проникновение стрептококков и продуктов их жизнедеятельности по лимфатическим путям в регионарные лимфатические узлы вызывает их острое воспаление. При благоприятном течении болезни распространение микроорганизмов ограничивается лимфоидными образованиями ротоглотки и регионарными лимфатическими узлами. При недостаточности барьерной функции тканей, окружающих миндалины, стрептококки могут проникать в околоминдалиновую клетчатку и вызывать ее воспаление (перитонзиллит, перитонзиллярный абсцесс), а при проникновении в кровеносное русло – приводить к развитию сепсиса.












